циклим аланин и клималанин в чем разница
«Быстрый эффект» клималанина (бета-аланина) при приливах: сравнительное исследование взаимодействий бета-аланина, таурина и глицина с глициновыми рецепторами
Опубликовано:
Гинекология, том 14, №2
Rapid effect of beta-alanine in the therapy of hot flashes: a comparative biophysical modeling of interactions beta-alanine, taurine and glycine with the glycine receptors
Введение
Cпецифические вегетативно-сосудистые пароксизмы – так называемые приливы – быстро развивающийся вазомоторный симптомокомплекс в перименопаузе. Субъективно «прилив» можно описать как внезапную волну интенсивного тепла и даже жара по телу, сопровождающуюся профузным потоотделением, тахикардией и у многих пациенток подъемом артериального давления.
Препараты для «быстрого» купирования возникающих пароксизом практически неизвестны. Наиболее часто в терапии приливов используется заместительная гормональная терапия (ЗГТ) препаратами эстрогенов. Эффекты синтетических эстрогенов развиваются постепенно, в течение недель и месяцев [1, 2]. Кроме того, пероральная ЗГТ может приводить к головной боли и повышает риск рака молочной железы, яичников, матки, венозной тромбоэмболии [3–6], что простимулировало проведение многочисленных исследований альтернативных видов терапии приливов [7].
Накапливающиеся клинические данные позволяют утверждать, что бета-аланин может купировать приливы в течение нескольких минут. Молекулярно-физиологический механизм развития столь «быстрого» эффекта бетааланина не вполне ясен. Фармакологическое действие бета-аланина объяснимо с точки зрения гормонально-нейротрансмиттерного подхода [8] через воздействие на терморегуляторное ядро в преоптической области гипоталамуса. В терморегуляторном ядре содержатся многочисленные типы рецепторов, которые могут влиять на терморегуляцию: рецепторы гамма-аминомасляной кислоты (ГАМК) [9], гистаминовые [10], альфа-адренергические [11], допаминовые [12], простагландиновые [13, 14], глутаматные, холинергические [15] и глициновые рецепторы [16].
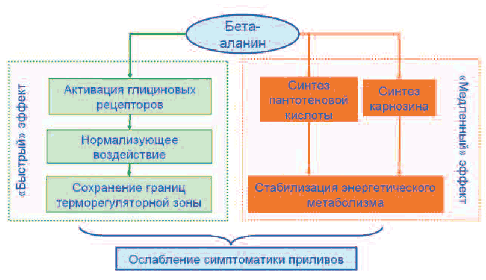
В настоящей работе рассматриваются молекулярно-биофизические механизмы глициновых рецепторов. Интерес к глициновым рецепторам обусловлен тем, что среди вышеперечисленных рецепторов взаимодействие бета-аланина было достоверно доказано только для глициновых рецепторов [8]. Взаимодействуя с глициновыми рецепторами, бета-аланин может способствовать «быстрой» нормализации активности терморегуляторной зоны гипоталамуса, а через синтез пантотената (витамин В5) и накопление карнозина бета-аланин способствует стабилизации энергетического метаболизма, что также соответствует ослаблению симптоматики приливов (рис. 1).
Рис. 1. Механизмы терапевтического воздействия бетааланина при приливах.
Заметим, что «медленные» эффекты бета-аланина (днинедели), обусловленные воздействием на энергетический метаболизм (синтез карнозина и пантотената), не менее важны, чем «быстрые» эффекты бета-аланина (минуты), обусловленные взаимодействиями с глициновыми рецепторами (и, возможно, с рецепторами других типов). Стабилизация энергетического метаболизма способствует уменьшению симптоматики приливов [16–19].
Прием бета-аланина постепенно увеличивает уровни карнозина в мышцах, уменьшает утомляемость женщины во время приливов и увеличивает ресурс мышечной системы [20]. В конечном итоге долговременная обеспеченность карнозином нормализует работу гладкой мускулатуры сосудов и тем самым способствует нормализации терморегуляции организма.
Взаимодействие бета-аланина с глициновыми рецепторами является одним из наиболее вероятных объяснений «быстрого» эффекта клималанина. Активированные глициновые рецепторы (глицинуправляемые хлоридные каналы) опосредуют процессы торможения в стволе головного мозга и в спинном мозге. Связываясь с рецептором, нейротрансмиттер глицин и бета-аланин открывают канал рецептора, который пропускает внутрь постсинаптических нейронов ионы хлора. Активация глициновых рецепторов оказывает нормализующее (в случае повышенного нервного возбуждения) действие[21]. В частности, глициновые рецепторы воздействуют на терморегуляторное ядро гипоталамуса [22], активирующее механизмы для поддержания температуры тела в нормальном диапазоне, называемом терморегуляторной зоной. Как известно, у женщин с приливами имеет место сужение границ терморегуляторной зоны [23, 24].
В настоящей работе было проведено сравнительное биофизическое моделирование взаимодействия бета-аланина, таурина и глицина с глициновыми рецепторами. На основе полученных моделей глициновых рецепторов оценивалось сродство (энергия связывания) глицина, бета-аланина и таурина с рецепторами.
Материалы и методы
Модели пространственной структуры глициновых рецепторов человека были приготовлены по методике, описанной в работе [25]. Затем были исследованы возможности размещения молекул лигандов в связывающих карманах рецепторов. Для этого проводилась минимизация энергии при различных начальных расположениях молекулы относительно кармана рецептора [26]; для анализа данных расчетов использовался метод молекулярных энергетических профилей [25], позволяющий анализировать энергетический вклад (dGост) каждого аминокислотного остатка белка.
Результаты и обсуждение
В ходе настоящего исследования были получены различные пространственные структуры глицинового рецептора и рассчитаны значения энергий связывания (отражающих степень сродства к рецептору) рецепторов с глицином, бета-аланином, таурином. Полученные данные были сравнены с имеющимися литературными данными по структурефункции глициновых рецепторов.
Модель пространственной структуры глицинового рецептора
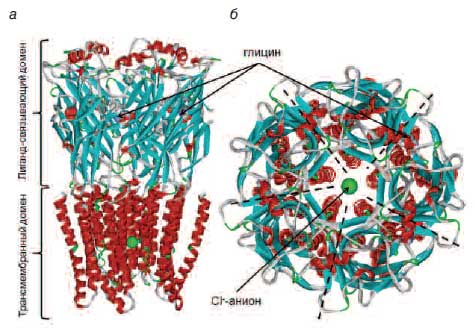
Рецептор глицина является трансмембранным белком, состоящим из пяти белковых субъединиц (рис. 2), образующих центральный канал для селективного проведения ионов хлора [27, 28]. Каждая субъединица состоит из трансмембранного домена (который, собственно, и образует хлоридный канал) и лигандсвязывающего домена (опосредует взаимодействия рецептора с агонистами: глицином, бета-аланином, таурином). К настоящему времени известны 5 типов субъединиц глициновых рецепторов – 4 субъединицы типа альфа (α1, α2, α3, α4) и одна β-субъединица, так что молекула глицинового рецептора может быть образована различными комбинациями этих 5 типов субъединиц.
Рис. 2. Пространственная структура глициновых рецепторов.
Показан ион хлорида в центре канала (зеленая сфера) и участки (участки) связывания молекул глицина (сферические модели): а – Вид сбоку; б – Вид сверху (снаружи нейрона, т.е. со стороны синапса). Штрихпунктирными линиями показано расположение контактов между пятью субъединицами рецептора.
Расчет энергий связывания бета-аланина с глициновыми рецепторами
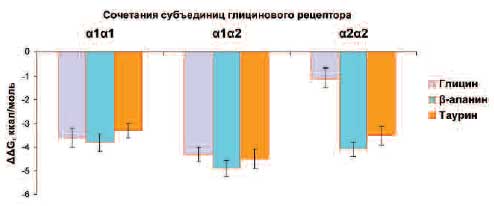
Отметим, что вследствие существования пяти взаимозаменяемых субъединиц (α1, α2, α3, α4 и β), может существовать множество (тысячи) разновидностей глициновых каналов, различающихся как по количественному набору субъединиц (например, 3α1 и 2β и т.д.), так и по порядку включения субъединиц в состав канала (например, α1α2α3α4β, α1α1α2α3β, α1α2α1ββ и десятки других) [28]. Состав субъединиц весьма важен, так как участки связывания глицина и других агонистов расположены в контактах между субъединицами [29], что делает необходимым оценку энергий связывания для разных сочетаний субъединиц (α1α1, α1α2, α2α2 и др.). Так как субъединицы α1 и α2 обнаруживаются наиболее часто [30], в настоящей работе расчет энергий связывания агонистов с глициновыми рецепторами проводился для трех сочетаний субъединиц – α1α1, α1α2 и α2α2 (рис. 3).
Рис. 3. Энергии связывания глицина, бета-аланина и таурина с различными типами контактов субъединиц рецепторов.
ΔΔG (ккал/моль), энергия связывания лиганда, отражающая сродство лиганда к рецептору: чем более отрицательно значение ΔΔG, тем выше сродство.
Молекулярные детерминанты ионной селективности глициновых рецепторов
Аминокислоты-агонисты глициновых рецепторов образуют следующий порядок по степени активации каналов глициновых рецепторов: глицин>бета-аланин>таурин>ГАМК [31–33]. Следует отметить, что определяемая в биохимических экспериментах «степень активации каналов» не отражает «сродства» (т.е. степени связывания) агониста к каналам. Большая энергия связывания (большее сродство) агониста к каналам, даже при более низкой активации, обеспечивает более пролонгированное воздействие агониста на рецептор. Это имеет прямое отношение к результату, полученному в настоящей работе: рассчитанная энергия связывания бета-аланина с глициновым рецептором выше, чем энергия связывания самого глицина с рецептором (или, по крайней мере, сравнима с энергией связывания глицина).
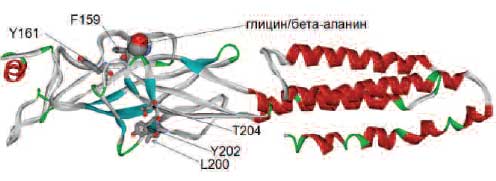
Поэтому клималанин может характеризоваться более продолжительным эффектом воздействия на глициновые рецепторы, чем сам глицин. Подобно глицину бета-аланин в составе клималанина активирует глициновые рецепторы и в коре больших полушарий головного мозга, что в той или иной мере может положительно влиять на когнитивные функции (память и концентрацию внимания). Это открывает еще одну очень интересную перспективу изучения препарата клималанин на когнитивные возможности, как правило, подавленные при патологическом течении периклимактерического периода. Более пролонгированное воздействие бета-аланина на глициновый рецептор при приливах соответствует более продолжительному воздействию препаратов на основе бета-аланина на процессы нормализации работы терморегуляторного ядра. Этот вывод представляется важным для понимания фармакологических эффектов препарата клималанин. Иначе говоря, клималанин может способствовать продолжительной стабилизации функционирования терморегуляторного ядра гипоталамуса. Нами была уточнена структура участка связывания глицина и бета-аланина глициновым рецептором. По данным биохимических исследований, остатки N102, G160, L200, Y202 и T204 (нумерация по последовательности a1 субъединицы) образуют участок связывания агонистов и определяют чувствительность рецептора [34]; лейцин-200 (L200), тирозин-202 (Y202) и треонин-204 (T204) играют особую роль в чувствительности рецептора к глицину [35]. В соответствии с полученными данными, аминокислоты L200, Y202 и T204 поддерживают структуру всего глицинсвязывающего участка (рис. 4). В то же время остатки фенилаланина F159 и тирозина Y161, специфически влияющие на чувствительность к агонистам, расположены в непосредственной близости с молекулами глицина и бета-аланина. Замены аминокислот F159Y и Y161F приводили к увеличению чувствительности к глицину в 12 раз, а чувствительности к бета-аланину – в 120 раз (!) [35].
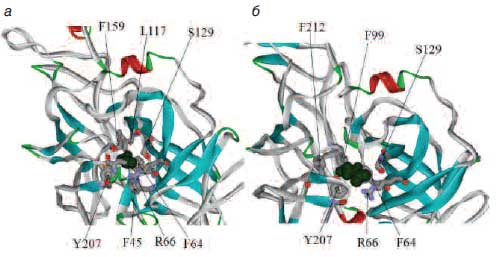
Рис. 4. Пространственные структуры комплексов 1-субъединицы с глицином и бета-аланином.
Следует отметить, что полученные модели комплексов позволяют подробно рассмотреть молекулярные механизмы воздействия ионов цинка и кислотности среды (рН) на активность глициновых рецепторов. Модуляция активности глициновых рецепторов посредством связывания ионов цинка весьма важна для активности рецептора. Как известно, ионы Zn2+ концентрируются в прозрачных пресинаптических пузырьках и секретируются в синаптическую щель одновременно с секрецией соответствующего нейротрансмиттера. Цинк повышает сродство глицина к рецептору, но повышенные концентрации цинка (более 10 мкмоль/л) способствуют снижению сродства [36].
Участок связывания цинка образован аминокислотными остатками H107 и H109, расположенными в лигандсвязывающем домене рецептора (рис. 5). Связывание данными остатками цинка стабилизирует структуру агонистсвязывающего участка, образованного F159 и другими остатками, что и способствует повышению сродства рецептора к агонистам. Избыточные уровни цинка соответствуют связыванию второго иона цинка непосредственно в участке связывания агониста, что и будет приводить к снижению сродства рецептора к глицину и бета-аланину.
Рис. 5. Участки связывания лигандов глицина и бета-аланина на границе между двумя субъединицами типа 1. Показаны молекулы лигандов (сферы темно-зеленого цвета) и аминокислоты, непосредственно участвующие в связывании молекул: а – глицин; б – бета-аланин.
Отметим, что у 80–90% женщин в климактерическом периоде развивается дефицит цинка, связанный со снижением кислотности желудка, сокращением микробиоты кишечника и диетарным дефицитом (в частности, вследствие углеводного типа питания). Дефицит цинка является диетарным фактором риска развития инсулинорезистентности, глюкозотолерантности, метаболического синдрома и сахарного диабета [37]. Поэтому эффективность терапии приливов бета-аланином может повышаться при нормальной обеспеченности пациентки цинком. При этом не следует превышать физиологических суточных потребностей в цинке (10–15 мг/сут). Отметим, что в климактерическом периоде дефицит цинка встречается в сотни раз чаще, чем избыточное потребление цинка.
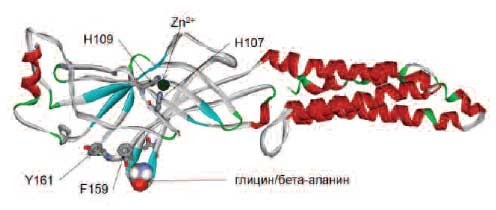
Эффекты кислотности (рН) внеклеточной среды на активность рецепторов обусловлены взаимодействиями протонов с регуляторным цинк связывающим участком рецептора, образованным остатками гистидина H107 и H109 (рис. 6). Чувствительность рецепторов к глицину значительно уменьшается по мере понижения рН спинномозговой жидкости [38].
Рис. 6. Расположения участка связывания цинка в пространственной структуре 1-субъединицы глицинового рецептора.
С клинической точки зрения, более низкие уровни рН соответствуют метаболическому ацидозу. Нарушения углеводного обмена способствуют формированию метаболического ацидоза и чаще сопровождаются симптоматикой приливов. Так как при снижении рН сродство лигандов к глициновым рецепторам снижается, для повышения эффективности терапии бета-аланином следует также принять комплекс мер по снижению метаболического ацидоза (снижение потребления углеводов, прием пищевых продуктов, способствующих ощелачиванию крови и др.).
Заключение
Требованием времени является поиск негормональных, но высокоэффективных фармакологических средств для патогенетического лечения приливов. Терапия приливов препаратом клималанин характеризуется «быстрым» эффектом. Одним из наиболее вероятных механизмов «быстрого» воздействия бета-аланина на купирование приливов является активация глициновых рецепторов.
Проведенное в настоящей работе сравнительное моделирование взаимодействий клималанина и глицина с пространственной структурой глициновых рецепторов показало, что энергия связывания рецептором бета-аланина превышает энергию связывания самого глицина. Последнее соответствует пролонгированному воздействию препаратов бета-аланина на глициновые рецепторы, что позволяет предположить, что при применении препарата клималанин возможно улучшение когнитивных функций. Анализ молекулярных детерминант селективности глициновых рецепторов показал, что при планировании терапии приливов бета-аланином целесообразно оценивать наличие у пациентки дефицита цинка и метаболического ацидоза.
Следует подчеркнуть, что способ приема препарата клималанин может оказывать существенное влияние на то, какой эффект будет более выражен – «быстрый» или «медленный». Так, рассасывание таблетки под языком будет способствовать быстрому поступлению бета-аланина в относительно высоких концентрациях непосредственно в кровь со слизистой подъязычного пространства, оказывая воздействие на головной мозг (терморегуляторная зона гипоталамуса) через связывание с глициновыми рецепторами и приводя к «быстрому эффекту» воздействия на терморегуляторное ядро гипоталамуса.
Литература
Медикаментозные методы лечения пациенток с вазомоторными симптомами климактерия
Опубликовано:
Российский вестник акушера-гинеколога 6, 2010
Д.м.н., проф. Т.В. Овсянникова, д.м.н., проф. И.О. Макаров, к.м.н., доц. Е.И. Боровкова, к.м.н., доц. Н.А. Шешукова
Кафедра акушерства и гинекологии факультета послевузовского профессионального обучения врачей (зав. — проф. И.О. Макаров) 1-го Московского государственного медицинского университета им. И.М. Сеченова
Medicament treatments in patients with vasomotor symptoms of the climacterium
The paper gives data on the treatment the nonhormonal drug Klimalanin (β-alanine) in women with vasomotor manifestations (hot flushes) of the climacteric syndrome. It shows the efficacy and benefits of the drug that may be given if there are any contraindications to hormonal therapy or if the therapy-associated adverse effects occur.
Key words: climacteric syndrome, vasomotor symptoms, Klimalanin.
Климактерический период (климактерий) — естественный биологический процесс перехода женщины от активного репродуктивного периода к периоду старости. Климактерий занимает длительный отрезок времени и включает постепенное угасание функции яичников, снижение уровня эстрогенов, наступление последней самостоятельной менструации и развитие симптомов, характерных для менопаузы.
Вопросы выбора метода терапии в климактерии обсуждаются достаточно широко, ввиду стойкой тенденции к увеличению продолжительности жизни женщины на протяжении последних десятилетий [2, 6]. Так, если средняя продолжительность жизни женщины составляла в 1990 г. 62 года, то после 2000 г. она увеличилась до 80 лет. Это означает, что при наступлении менопаузы у большинства женщин в 50 лет она значительную часть своей жизни проводит в условиях дефицита эстрогенов.
Общие изменения, сопровождающие процессы старения на фоне значительного снижения уровня эстрогенов, ассоциируются со следующим:
Климактерический период включает в себя 3 периода: пременопаузу, менопаузу и постменопаузу [6].
Пременопауза начинается в 45—47 лет и включает промежуток времени от появления первых симптомов до прекращения самостоятельных менструаций. Только 5—10% женщин не ощущают наступления менопаузы: до прекращения менструаций у них сохраняется регулярный ритм менструаций и отсутствуют ранние вазомоторные и психоэмоциональные симптомы.
Диагноз менопаузы ставится ретроспективно, в отсутствие самостоятельных менструаций в течение 1 года. Для женщин Центральной Европы и Российской Федерации возраст менопаузы составляет 50—51 год.
Постменопауза (menopauzal transition) — период с момента начала менопаузы и до смерти женщины.
Перименопауза — хронологическое определение промежутка времени угасания функции яичников включает период с появления первых симптомов климактерия + 2 года после последней менструации.
Климактерический синдром — комплекс патологических симптомов, развивающихся в период угасания репродуктивной функции и сопровождающих климактерический период. Различают 3 группы симптомов: ранние, средневременные и поздние (отдаленные).
Ранние и средневременные симптомы климактерия появляются у большинства женщин в пременопаузе и у 50% из них продолжаются более 10 лет. Наибольшая частота и интенсивность этих симптомов наблюдаются в пременопаузе и в первые годы постменопаузы. Поздние симптомы постменопаузы (органические и метаболические изменения) развиваются постепенно на протяжении 15 лет.
Ранние симптомы менопаузы в основном проявляются в виде «приливов» жара и повышенной потливости, тахикардии, лабильности АД, экстрасистолии, головокружения.
«Приливы» и повышенная потливость имеют вазомоторную природу и характеризуются повышением температуры кожных покровов, расширением периферических сосудов, транзиторным учащением сердцебиения. Периодически возникающее чувство жара появляется внезапно в области лица и в виде волн распространяется на шею, грудь и верхние конечности. У большинства женщин «приливы» сочетаются с покраснением кожи и появлением пота на лице и шее. В результате термографических исследований было установлено, что во время «прилива» температура кожи повышается приблизительно на 5 °С, но ощущается только в области лица и верхней половины грудной клетки. Чаще всего «приливы» провоцируются эмоциональным стрессом, возбуждением, страхом [3]. Продолжительность «приливов» колеблется от нескольких минут до получаса. Частота «приливов» варьирует от нескольких раз в месяц до 5—20 эпизодов в течение суток. У 25—30% женщин они сопровождаются сердцебиением и повышением АД. Ночные «приливы» вызывают нарушение сна, а впоследствии раздражительность и снижение работоспособности [4].
У большинства женщин вазомоторные симптомы появляются за несколько лет до наступления менопаузы и впервые регистрируются при задержке менструации. Пик «приливов» приходится на 2—3-й год постменопаузы, а затем их частота и интенсивность постепенно уменьшаются. У 75—80% женщин «приливы» сохраняются от 1 года до 7 лет, а у 15% из них — более 10 лет.
Механизмы возникновения «приливов» до настоящего времени окончательно не изучены [1, 4]. Многочисленные исследования, демонстрирующие связь между резким падением уровня эстрогенов и появлением вазомоторных симптомов у женщин в климактерии, позволяют считать, что в основе этих нарушений лежит нарушение нейроэндокринных механизмов регуляции менструального цикла. В настоящее время феномен «приливов» рассматривается как типичное проявление гипоталамической дисфункции. Известно, что между нейронами аркуатных ядер гипоталамуса, секретирующих гонадолиберин, и нейронами преоптических ядер, регулирующих температуру в организме женщины, существует тесная взаимосвязь. Таким образом, не исключено, что нарушение циркадного ритма секреции гонадолиберина, повышение его уровня и активности нейротрансмиттеров влияет на терморегулирующие центры [1]. Если в норме каждая женщина имеет определенные границы терморегуляторной зоны, то у женщин с «приливами» наблюдается их значительное сужение. В результате даже незначительное повышение температуры тела вызывает расширение сосудов и гипертермическую реакцию организма. В ряде исследований показано, что снижение уровня эстрогенов приводит к изменению уровня норадреналина, который является нейротрансмиттером, ответственным за сужение терморегуляторной зоны. Учитывая, что секреция норадреналина в ядре гипоталамуса подавляется эндорфинами и катехолэстрогенами, становится понятным, почему снижение содержания последних вызывает нарушение терморегуляции и появление «приливов». Еще одним нейротрансмиттером, участвующим в процессах терморегуляции, считают серотонин, уровень которого снижается одновременно со снижением концентрации эстрогенов у женщин после двусторонней овариэктомии и в постменопаузе [5].
В последние годы внимание ученых было обращено на кальцитониноподобный пептид (КПП), который определяется в центральной и периферической нервной системе и дает выраженный сосудорасширяющий эффект [8]. Показано, что прием эстрогенов увеличивает уровни КПП и метионинэнкефалина в организме женщины. Сравнительное исследование экскреции КПП показало достоверное повышение суточной экскреции КПП с мочой у женщин с «приливами» по сравнению с таковым у здоровых женщин. Эти данные нашли свое подтверждение при суточном мониторинге женщин, у которых на фоне «приливов» выявлено повышение КПП и нейропептида Y.
Согласно данным опросов и клинических исследований, более 70% женщин при наступлении климактерия, особенно при появлении первых признаков вазомоторных симптомов, хотели бы по-прежнему хорошо себя чувствовать, оставаться привлекательными и активными. В настоящее время для лечения климактерического синдрома предлагаются различные методы. Наряду с соблюдением диеты, занятиями спортом рекомендуются различные медикаментозные методы терапии. Патогенетически обоснованными и максимально эффективными считают гормональные препараты (эстрогены, комбинированные эстроген-прогестагенные препараты, тиболон). Тем не менее существует ряд проблем, ограничивающих назначение этой терапии в постменопаузе, и главное — наличие противопоказаний к гормональным препаратам [6]. К альтернативным методам терапии относятся фитопрепараты, селективные ингибиторы серотонина и др.
Одним из препаратов, недавно зарегистрированных в России, для лечения женщин в климактерии с вазомоторными симптомами является негормональный лекарственный препарат Клималанин (β-аланин). Во Франции препарат известен под названием абуфен.
Клималанин является β-аминокислотой, которая синтезируется в организме человека и необходима для синтеза карнозина и пантотеновой кислоты. Карнозин максимально концентрируется в головном мозге и в мышечной ткани, регулирует уровень внутриклеточного кальция и силу мышечных сокращений. Предполагают, что достаточное количество карнозина нормализует работу мышечного слоя сосудов и способствует нормализации терморегуляции.
Пантотеновая кислота (витамин В5) необходима для синтеза ацилкоэнзима А — центрального кофермента биохимическох процессов, вовлеченных в метаболизм белков, жиров и углеводов. Симптомы дефицита витамина В5 — астения, раздражительность, утомляемость, апатия, парестезии, спазм мышц и др. Клималанин способствует накоплению пантотеновой кислоты, вызывая стабилизацию энергетического метаболизма, что приводит к регуляции терморегуляции и уменьшению «приливов».
Этот препарат, назначаемый непосредственно во время «приливов», противодействует резкому высвобождению гистамина и брадикинина из тучных клеток, способствующих быстрому расширению сосудов кожи и покраснению. При этом β-аланин не блокирует Н1-рецепторы к гистамину [1, 4, 7].
Таким образом, комплексное воздействие негормонального препарата клималанина (β-аланин), которое он оказывает в организме человека (синтез пантотената и накопление карнозина, активация глициновых рецепторов), способствует сохранению границ терморегуляторной зоны, стабилизации энергетического метаболизма и торможению выброса гистамина и брадикинина.
Клималанин выпускается в таблетках по 400 мг и назначается по 1—2 таблетки, а при выраженных «приливах» — 3 таблетки в сутки. Терапия проводится курсами от 5—10 дней до исчезновения клинических проявлений вазомоторных нарушений. Эффективность клималанина изучена в ряде клинических исследований. Первое исследование было проведено Y. Barre в 1964 г. Под наблюдением находились 70 женщин с естественной, хирургической менопаузой и пациентки после оперативного лечения рака молочной железы и женских половых органов. Доза препарата составляла 400—800 мг, длительность терапии колебалась от 5 дней до 1—2 мес. Эффективность терапии оценивалась по снижению частоты «приливов» и составляла 70% в группе женщин, получавших β-аланин, и 33% в группе получавших плацебо. Авторы отмечают, что β-аланин может назначаться пациенткам с вазомоторными симптомами до начала заместительной гормональной терапии. Заслуживает внимания возможность применения негормонального препарата β-аланина у пациенток после оперативного вмешательства по поводу онкологических заболеваний женских половых органов и молочных желез, когда гормональные препараты категорически противопоказаны. Побочные эффекты β-аланина не выявлены ни у одной женщины.
Двойное слепое контролируемое исследование (P. Delaroix, 1978) проведено у женщин с естественной и искусственной менопаузой и вазомоторными симптомами различной частоты и интенсивности. Клималанин в дозе 1200 мг/сут (3 таблетки) и плацебо назначали в течение 60 дней. При оценке клинической эффективности терапии учитывались снижение частоты, интенсивности, переносимость «приливов», а также снижение степени тяжести климактерического синдрома. Частота и интенсивность «приливов» к концу 1-го месяца лечения была достоверно ниже в группе женщин, получавших β-аланин, по сравнению с группой пациенток, получавших плацебо, и этот уровень эффективности сохранялся в течение 2 мес. Выводы данного исследования свидетельствуют о том, что хорошие и очень хорошие результаты были отмечены у женщин с вазомоторными симптомами на фоне терапии β-аланином (84%). В группе женщин, получавших плацебо, положительный эффект составил лишь 3%.
В другом двойном слепом плацебо-контролируемом исследовании J. Roueche и соавт. (1991) продемонстрировали эффективность применения β-аланина по сравнению с плацебо у женщин с климактерическим синдромом и выраженными «приливами». Клималанин в дозе 400 мг 3 раза в сутки или плацебо назначали в течение 8 нед. Эффективность терапии оценивали по результатам еженедельного изменения частоты и интенсивности «приливов» в обеих группах женщин. Достоверное снижение частоты «приливов» было отмечено на 4-й неделе приема β-аланина, и этот эффект сохранялся на протяжении последующих 8 нед проводимой терапии. У женщин, принимавших плацебо, снижение частоты «приливов» на фоне терапии было статистически недостоверным по отношению к исходным показателям. Полное исчезновение «приливов» отмечено на 8-й неделе терапии у 40% женщин, принимавших β-аланин, и у 12% пациенток, принимавших плацебо, причем различия между группами по данному показателю были статистически достоверными уже на 7-й неделе лечения.
Таким образом, в результате клинических исследований показана способность клималанина (β-аланина) оказывать патогенетическое воздействие на основные звенья развития вазомоторных симптомов климактерия. Клималанин положительно влияет на периферическую вазодилатацию, которая является причиной вегетативных реакций у женщин с климактерическим синдромом. Противодействуя резкому высвобождению гистамина, препарат не обладает антигистаминной активностью и не вызывает такие побочные реакции, как сонливость, слабость, снижение работоспособности. Клималанин не взаимодействует с половыми гормонами, не приводит к задержке жидкости и прибавке массы тела и не нуждается в постоянном приеме.
Клималанин показан женщинам с вазомоторными симптомами при естественной и искусственной менопаузе. Клималанин может быть назначен в следующих клинических ситуациях:
Курсы лечения клималанином могут назначаться на протяжении от 5—10 дней до исчезновения вазомоторных нарушений у женщины в климактерии.