Можно ли давать детям амбробене перед сном
Амбробене (Ambrobene) инструкция по применению
Владелец регистрационного удостоверения:
Произведено:
Контакты для обращений:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Амбробене
Сироп прозрачный, от бесцветного до слегка желтого цвета, с запахом малины.
| 5 мл | 1 фл. | |
| амброксола гидрохлорид | 15 мг | 300 мг |
× дополнительно могут быть нанесены защитные наклейки.
Фармакологическое действие
Муколитический и отхаркивающий препарат.
После приема внутрь действие наступает через 30 мин и продолжается в течение 6-12 ч (в зависимости от принятой дозы). Доклинические исследования показали, что амброксол стимулирует серозные клетки желез слизистой оболочки бронхов. Активируя клетки реснитчатого эпителия и снижая вязкость мокроты, улучшает мукоцилиарный транспорт.
Амброксол активирует образование сурфактанта, оказывая прямое воздействие на альвеолярные пневмоциты 2 типа и клетки Клара мелких дыхательных путей.
Исследования на клеточных культурах и исследования in vivo на животных показали, что амброксол стимулирует образование и секрецию вещества (сурфактанта), активного на поверхности альвеол и бронхов эмбриона и взрослого.
Также при доклинических исследованиях был доказан антиоксидантный эффект амброксола. Амброксол при совместном применении с антибиотиками (амоксициллин, цефуроксим, эритромицин и доксициклин) увеличивает их концентрацию в мокроте и бронхиальном секрете.
Фармакокинетика
Всасывание, распределение, метаболизм
При приеме внутрь амброксол практически полностью всасывается из ЖКТ. C max достигается через 1-3 ч после приема внутрь. Из-за пресистемного метаболизма абсолютная биодоступность амброксола после приема внутрь снижается приблизительно на 1/3. Образующиеся в связи с этим метаболиты (такие как дибромоантраниловая кислота, глюкурониды) элиминируются почками.
Связывание белками плазмы составляет около 85% (80-90%).
Амброксол проникает в спинномозговую жидкость и через плацентарный барьер, а также выделяется с грудным молоком.
Учитывая высокое связывание с белками плазмы, большой V d и медленное перераспределение из тканей в кровь, существенного выведения амброксола при диализе или форсированном диурезе не происходит.
Фармакокинетика в особых клинических случаях
У пациентов с тяжелыми заболеваниями печени клиренс амброксола уменьшается на 20-40%.
У пациентов с тяжелыми нарушениями функции почек T 1/2 метаболитов амброксола увеличивается
Показания препарата Амбробене
Режим дозирования
Длительность лечения подбирается индивидуально в зависимости от течения заболевания. Не рекомендуется принимать Амбробене без назначения врача более чем в течение 4-5 дней. Муколитический эффект препарата проявляется при приеме большого количества жидкости. Поэтому во время лечения рекомендуется обильное питье.
Сироп следует принимать после еды, используя прилагаемый мерный стаканчик.
Детям в возрасте до 2 лет следует принимать по 1/2 мерного стаканчика (2.5 мл сиропа) 2 раза/сут (15 мг амброксола/сут).
Детям в возрасте от 2 до 6 лет следует принимать по 1/2 мерного стаканчика (2.5 мл сиропа) 3 раза/сут (22.5 мг амброксола/сут).
Детям возрасте от 6 до 12 лет следует принимать по 1 мерному стаканчику (5 мл сиропа) 2-3 раза/сут (30-45 мг амброксола/сут).
Взрослым и детям старше 12 лет в первые 2-3 дня лечения следует принимать по 2 мерных стаканчика (10 мл сиропа) 3 раза/сут (90 мг амброксола/сут). При неэффективности терапии взрослым можно увеличить дозу до 4 мерных стаканчиков (20 мл сиропа) 2 раза/сут (120 мг амброксола/сут). В последующие дни следует принимать по 2 мерных стаканчика (10 мл сиропа) 2 раза/сут (60 мг амброксола/сут).
Побочное действие
Аллергические реакции: редко (от ≥0.1% до Со стороны пищеварительной системы: редко (от ≥0.1% до Общие нарушения: редко (от ≥0.1% до Прочие: редко (от ≥0.1% до осторожностью следует применять препарат у пациентов с нарушением моторной функции бронхов и повышенным образованием мокроты (при синдроме неподвижных ресничек), при язвенной болезни желудка и двенадцатиперстной кишки в фазе обострения, во II и III триместрах беременности, в период лактации.
Применение при беременности и кормлении грудью
Недостаточно данных относительно применения амброксола при беременности, особенно в первые 28 недель. Применение Амбробене во II и III триместрах беременности возможно только по назначению врача, после тщательной оценки ожидаемой пользы терапии для матери и потенциального риска для плода.
Применение препарата у женщин в период лактации изучено недостаточно, поэтому прием Амбробене возможен только по назначению врача, после тщательной оценки соотношения ожидаемой пользы терапии для матери и потенциального риска для грудного ребенка.
В экспериментальных исследованиях на животных не выявлено тератогенного эффекта; показано, что амброксол выделяется с грудным молоком.
Применение при нарушениях функции печени
Применение при нарушениях функции почек
Применение у детей
Препарат в форме таблеток и раствора для инъекций противопоказан к применению у детей в возрасте до 6 лет.
Препарат в форме капсул ретард противопоказан к применению у детей в возрасте до 12 лет.
Лечение детей в возрасте до 2 лет следует проводить только под контролем врача.
Особые указания
Не следует комбинировать с противокашлевыми лекарственными средствами, затрудняющими выведение мокроты.
Крайне редко наблюдались кожные реакции в тяжелой форме, такие как синдром Стивенса-Джонсона и синдром Лайелла, при применении амброксола. При изменении кожных покровов или слизистых оболочек пациент должен срочно обратиться к врачу и прекратить прием препарата.
При применении Амбробене в форме сиропа следует учитывать, что калорийность составляет 2.6 ккал/г сорбитола. Сорбитол может оказывать легкое слабительное действие. 1 мерный стаканчик (5 мл сиропа) содержит 2.1 г сорбитола, что соответствует 0.18 ХЕ.
Использование в педиатрии
У детей в возрасте до 2 лет применение препарата Амбробене в форме сиропа возможно только по назначению врача.
Влияние на способность к управлению транспортными средствами и механизмами
Влияние на способность к вождению транспорта и управлению машинами и механизмами до настоящего времени не известно.
Передозировка
Симптомы: симптомов интоксикации при передозировке амброксола не выявлено. Имеются сведения о нервном возбуждении и диарее. Амброксол хорошо переносится при приеме внутрь в дозе до 25 мг/кг/сут. В случае тяжелой передозировки возможны повышенное слюноотделение, тошнота, рвота, снижение АД.
Лечение: методы интенсивной терапии, такие как вызывание рвоты, промывание желудка, следует применять только в случаях тяжелой передозировки, в первые 1-2 ч после приема препарата. Показано симптоматическое лечение.
Лекарственное взаимодействие
При одновременном применении амброксола и противокашлевых средств из-за подавления кашлевого рефлекса может возникнуть застой секрета. Поэтому подобные комбинации следует подбирать с осторожностью.
При совместном приеме амброксола и антибиотиков амоксициллина, цефуроксима, эритромицина и доксициклина концентрация последних в мокроте и бронхиальном секрете увеличивается.
Условия хранения препарата Амбробене
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Амбробене
После вскрытия флакона препарат пригоден для применения в течение 1 года.
Условия реализации
Препарат разрешен к применению в качестве средства безрецептурного отпуска.
Контакты для обращений
ТЕВА (Израиль)
 | 115054 Москва, Валовая ул. 35 Амбробене (Ambrobene) инструкция по применению⚠️ Регистрационное удостоверение данного продукта заменено Владелец регистрационного удостоверения:Произведено:Лекарственная формаФорма выпуска, упаковка и состав препарата АмбробенеРаствор для приема внутрь и ингаляций прозрачный, от бесцветного до светло-желтого с коричневым оттенком цвета, без запаха.
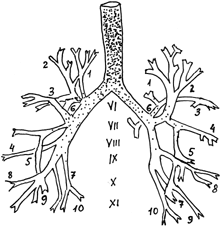
Фармакологическое действиеМуколитический и отхаркивающий препарат. После приема внутрь действие наступает через 30 мин и продолжается в течение 6-12 ч (в зависимости от принятой дозы). Доклинические исследования показали, что амброксол стимулирует серозные клетки желез слизистой оболочки бронхов. Активируя клетки реснитчатого эпителия и снижая вязкость мокроты, улучшает мукоцилиарный транспорт. Амброксол активирует образование сурфактанта, оказывая прямое воздействие на альвеолярные пневмоциты 2 типа и клетки Клара мелких дыхательных путей. Исследования на клеточных культурах и исследования in vivo на животных показали, что амброксол стимулирует образование и секрецию вещества (сурфактанта), активного на поверхности альвеол и бронхов эмбриона и взрослого. Также при доклинических исследованиях был доказан антиоксидантный эффект амброксола. Амброксол при совместном применении с антибиотиками (амоксициллин, цефуроксим, эритромицин и доксициклин) увеличивает их концентрацию в мокроте и бронхиальном секрете. ФармакокинетикаВсасывание, распределение, метаболизм При приеме внутрь амброксол практически полностью всасывается из ЖКТ. C max достигается через 1-3 ч после приема внутрь. Из-за пресистемного метаболизма абсолютная биодоступность амброксола после приема внутрь снижается приблизительно на 1/3. Образующиеся в связи с этим метаболиты (такие как дибромоантраниловая кислота, глюкурониды) элиминируются почками. Связывание белками плазмы составляет около 85% (80-90%). Амброксол проникает в спинномозговую жидкость и через плацентарный барьер, а также выделяется с грудным молоком. Учитывая высокое связывание с белками плазмы, большой V d и медленное перераспределение из тканей в кровь, существенного выведения амброксола при диализе или форсированном диурезе не происходит. Фармакокинетика в особых клинических случаях У пациентов с тяжелыми заболеваниями печени клиренс амброксола уменьшается на 20-40%. У пациентов с тяжелыми нарушениями функции почек T 1/2 метаболитов амброксола увеличивается. Показания препарата АмбробенеРежим дозированияДлительность лечения устанавливается индивидуально в зависимости от течения заболевания. Не рекомендуется принимать Амбробене без назначения врача более чем в течение 4-5 дней. Муколитический эффект препарата проявляется при приеме большого количества жидкости. Поэтому во время лечения рекомендуется обильное питье. Раствор для приема внутрь и ингаляций принимают внутрь после еды, добавляя в воду, сок или чай с помощью мерного стаканчика. 1 мл раствора для приема внутрь содержит 7.5 мг амброксола. Детям в возрасте до 2 лет назначают по 1 мл раствора 2 раза/сут (15 мг/сут). Детям в возрасте от 2 до 6 лет назначают по 1 мл раствора 3 раза/сут (22.5 мг/сут). Детям в возрасте от 6 до 12 лет назначают по 2 мл раствора 2-3 раза/сут (30-45 мг/сут). При применении Амбробене в виде ингаляций используют любое современное оборудование (кроме паровых ингаляторов). Перед ингаляцией препарат следует смешать с 0.9% раствором натрия хлорида (для оптимального увлажнения воздуха можно развести в соотношении 1:1) и подогревается до температуры тела. Ингаляции следует проводить в режиме обычного дыхания, чтобы не спровоцировать кашлевые толчки. Пациентам с бронхиальной астмой рекомендуется проведение ингаляции после приема бронхолитиков. Детям в возрасте до 2 лет ингалируют по 1 мл раствора 1-2 раза/сут (7.5-15 мг/сут). Детям в возрасте от 2 до 6 лет ингалируют по 2 мл раствора 1-2 раза/сут (15-30 мг/сут). Взрослым и детям в возрасте старше 6 лет ингалируют по 2-3 мл раствора 1-2 раза/сут (15-45 мг/сут). Побочное действиеПротивопоказания к применениюС осторожностью следует применять препарат у пациентов с нарушением моторной функции бронхов и повышенным образованием мокроты (при синдроме неподвижных ресничек), при язвенной болезни желудка и двенадцатиперстной кишки в фазе обострения, во II и III триместрах беременности, в период лактации. Применение при беременности и кормлении грудьюНедостаточно данных относительно применения амброксола при беременности, особенно в первые 28 недель. Применение Амбробене во II и III триместрах беременности возможно только по назначению врача, после тщательной оценки ожидаемой пользы терапии для матери и потенциального риска для плода. Применение препарата у женщин в период лактации изучено недостаточно, поэтому прием Амбробене возможен только по назначению врача, после тщательной оценки соотношения ожидаемой пользы терапии для матери и потенциального риска для грудного ребенка. В экспериментальных исследованиях на животных не выявлено тератогенного эффекта; показано, что амброксол выделяется с грудным молоком. Применение при нарушениях функции печениПрименение при нарушениях функции почекПрименение у детейПрепарат в форме таблеток и раствора для инъекций противопоказан к применению у детей в возрасте до 6 лет. Лечение детей в возрасте до 2 лет следует проводить только под контролем врача. Особые указанияНе следует комбинировать с противокашлевыми лекарственными средствами, затрудняющими выведение мокроты. Крайне редко наблюдались кожные реакции в тяжелой форме, такие как синдром Стивенса-Джонсона и синдром Лайелла, при применении амброксола. При изменении кожных покровов или слизистых оболочек пациент должен срочно обратиться к врачу и прекратить прием препарата. Использование в педиатрии У детей в возрасте до 2 лет применение препарата Амбробене в форме раствора для приема внутрь и ингаляций возможно только по назначению врача. Влияние на способность к управлению транспортными средствами и механизмами Исследований по изучению влияния Амбробене на способность к управлению транспортом и работу с техникой не проводилось. При развитии побочных эффектов пациенты должны соблюдать осторожность при выполнении действий, требующих повышенной концентрации внимания и быстроты психомоторных реакций. ПередозировкаСимптомы: симптомов интоксикации при передозировке амброксола не выявлено. Имеются сведения о нервном возбуждении и диарее. Амброксол хорошо переносится при приеме внутрь в дозе до 25 мг/кг/сут. В случае тяжелой передозировки возможны повышенное слюноотделение, тошнота, рвота, снижение АД. Лечение: методы интенсивной терапии, такие как вызывание рвоты, промывание желудка, следует применять только в случаях тяжелой передозировки, в первые 1-2 ч после приема препарата. Показано симптоматическое лечение. Лекарственное взаимодействиеПри одновременном применении амброксола и противокашлевых средств из-за подавления кашлевого рефлекса может возникнуть застой секрета. Поэтому подобные комбинации следует подбирать с осторожностью. При совместном приеме амброксола и антибиотиков амоксициллина, цефуроксима, эритромицина и доксициклина концентрация последних в мокроте и бронхиальном секрете увеличивается. Условия хранения препарата АмбробенеПрепарат следует хранить в недоступном для детей месте при температуре не выше 25°С. Срок годности препарата АмбробенеУсловия реализацииПрепарат разрешен к применению в качестве средства безрецептурного отпуска. Амбробене (сироп) : инструкция по применениюЛекарственная формаСироп, 15 мг/5 мл, 100 мл Состав5 мл сиропа содержат активное вещество: амброксола гидрохлорид 15,0 мг, вспомогательные вещества: сорбитол 70%, пропиленгликоль, ароматизатор малиновый, сахарин, вода очищенная. ОписаниеПрозрачный от бесцветного до слегка желтоватого цвета раствор с запахом малины. Фармакотерапевтическая группаПрепараты для устранения симптомов простуды и кашля. Отхаркивающие препараты. Муколитики. Амброксол. Фармакологическое действиеВсасывание. Абсорбция высокая и почти полная, линейнозависима от терапевтической дозы. Максимальная плазменная концентрация достигается в течение 1-2,5 часов. Распределение. Распределение быстрое и обширное, с наивысшими концентрациями в ткани легких. Объем распределения примерно 552 л. Связь с белками плазмы крови составляет приблизительно 90 %. Метаболизм и выведение. Примерно 30 % принятой внутрь дозы подвергается эффекту «первого прохождения» через печень. CYP3A4 – основной фермент, ответственный за метаболизм амброксола, под действием которого, преимущественно в печени, образуются конъюгаты. Выведение снижается при нарушениях функции печени, что приводит к повышению уровня в плазме крови в 1,3-2 раза, но не требует коррекции дозы. Пол и возраст не оказывают клинически значимого влияния на фармакокинетику амброксола и не требуют коррекции дозы. Прием пищи не оказывает влияния на биодоступность амброксола гидрохлорида. Амбробене® обладает секретолитическим и отхаркивающим действием; стимулирует серозные клетки желез слизистой оболочки бронхов, увеличивает содержание слизистого секрета и выделение поверхностно-активного вещества (сурфактанта) в альвеолах и бронхах; нормализует нарушенное соотношение серозного и слизистого компонентов мокроты. Активируя гидролизующие ферменты и усиливая высвобождение лизосом из клеток Клара, снижает вязкость мокроты. Повышает двигательную активность ресничек мерцательного эпителия, увеличивает мукоцилиарный транспорт мокроты. Повышение секреции и мукоцилиарного клиренса улучшает отделение мокроты и облегчает кашель. Доказано, что местноанестезирующее действие амброксола обусловлено дозозависимой блокадой натриевых каналов нейронов. Под воздействием амброксола значительно снижается высвобождение цитокинов из крови, а также из тканевых мононуклеаров и полиморфонуклеарных клеток. Клинические исследования на пациентах с болью в горле показали значительное уменьшение боли и покраснения в горле. нормализует измененную бронхолегочную секрецию, улучшает реологические показатели мокроты, уменьшая ее вязкость, облегчает выведение мокроты из бронхов. Амбробене® способствует активации системы поверхностно активных веществ через прямое воздействие на пневмоциты типа 2 в альвеолах и Клара-клетки, стимулирует образование и выведение поверхностно активного материала (сурфактанта) в альвеолярной и бронхиальной области зародышевых и взрослых легких. Помимо этого, установлены антиоксидантные эффекты амброксола. После применения Амбробене® увеличивается концентрация антибиотиков в мокроте и бронхиальном секрете. Показания к применению— секретолитическая терапия острых и хронических бронхолегочных заболеваний, характеризующихся нарушением секреции и затрудненным отхождением мокроты Способ применения и дозыАмбробене® сироп принимают внутрь после еды с достаточным количеством теплой жидкости (например, вода) с помощью прилагаемого мерного стаканчика. Взрослые и дети старше 12 лет: в первые 2-3 дня по 10 мл 3 раза в сутки, затем по 10 мл 2 раза или по 5 мл 3 раза в сутки. Дети с 6 до 12 лет: по 5 мл 2-3 раза в сутки. Дети с 2 до 5 лет: по 2,5 мл 3 раза в сутки. Длительность лечения зависит от особенностей течения заболевания. Не рекомендуется применять Амбробене® сироп без врачебного назначения более 4-5 дней. Побочные действияПротивопоказания— повышенная чувствительность к амброксолу и/или другим компонентам препарата — редкая наследственная непереносимость фруктозы — тяжелая почечная недостаточность — тяжелая печеночная недостаточность — I триместр беременности — детский возраст до 2-х лет Лекарственные взаимодействияНе сообщалось о клинически значимых неблагоприятных взаимодействиях с другими препаратами. Совместное применение с противокашлевыми препаратами приводит к затруднению отхождения мокроты на фоне подавления кашля. Увеличивает проникновение и концентрацию в бронхиальном секрете амоксициллина, цефуроксима и эритромицина. Особые указанияЗарегистрированы очень редкие случаи тяжелых поражений кожи таких, как синдром Стивенса-Джонсона и токсический эпидермальный некролиз, при применении амброксола гидрохлорида. Главным образом они обусловлены тяжестью основного заболевания и сопутствующим лечением. Кроме того на ранней стадии синдрома Стивенса-Джонсона и токсического эпидермального некролиза у пациентов могут проявляться признаки начала неспецифического заболевания, со следующими симптомами: повышение температуры тела, боль во всем теле, ринит, кашель и боль в горле. Появление этих признаков может привести к ненужному симптоматическому лечению противопростудными препаратами. В случае появления кожных поражений – пациент немедленно осматривается врачом, прием амброксола гидрохлорида прекращается. Необходимо принимать во внимание для больных, страдающих сахарным диабетом, что в 1 мерном стаканчике Амбробене® сиропа содержится 2,1 г сорбита (эквивалентно 0,18 CEU). При ограничении функциональной способности почек и/или при тяжелых заболеваниях печени Амбробене® нужно применять с особой осторожностью, уменьшая применяемую дозу и увеличивая время между приемами препарата. Беременность и период лактации Амброксола гидрохлорид проникает через плацентарный барьер. Доклинические исследования не показали прямого или косвенного отрицательного воздействия на беременность, развитие плода, роды и постнатальное развитие. Не рекомендуется применять Амбробене® в период I триместра беременности. Несмотря на то, что до настоящего времени нет достоверных данных отрицательного влияния на плод и младенцев, использование препарата во II и III триместрах беременности и в период лактации возможно после тщательного анализа соотношения польза/риск лечащим врачом. Особенности влияния лекарственного средства на способность управления транспортным средством или потенциально опасными механизмами ПередозировкаСимптомы: возбуждение, тошнота, повышенная саливация, рвота, диарея, диспепсия, гипотензия СУХОЙ НЕПРОДУКТИВНЫЙ КАШЕЛЬ У ДЕТЕЙКашель (от лат. tussis) — защитный сложнорефлекторный акт, характеризующийся резким нарастанием внутригрудного давления (за счет синхронного напряжения дыхательной и вспомогательной мускулатуры) при закрытой голосовой щели с последующим ее открытием и Кашель (от лат. tussis) — защитный сложнорефлекторный акт, характеризующийся резким нарастанием внутригрудного давления (за счет синхронного напряжения дыхательной и вспомогательной мускулатуры) при закрытой голосовой щели с последующим ее открытием и толчкообразным форсированным выдохом, при котором из дыхательных путей удаляется их содержимое. Физиологическое значение кашля состоит в очищении дыхательных путей от веществ, попавших в них извне (некоторые запахи, холодный или сухой воздух, дым, пыль, различные микроорганизмы, инородные тела и т. п.), и от эндогенных компонентов (частички бронхиального эпителия, слизь и др.). Важно помнить, что возникновение кашля при удалении из дыхательных путей их содержимого происходит в том случае, если перистальтические движения мелких бронхов и деятельность реснитчатого эпителия оказываются не в состоянии обеспечить необходимый дренаж трахеобронхиального дерева. Кашлевой рефлекс начинается с раздражения в дыхательных путях чувствительных окончаний блуждающего нерва или с рецепторов плевры. Это раздражение передается в дыхательный центр, расположенный в продолговатом мозгу. Здесь при участии полисинаптических связей ретикулярной формации формируется сложнокоординированная реакция мышц бронхов, гортани, диафрагмы, грудной клетки, живота. Начальной фазой кашля является глубокий вдох. Затем следует фаза напряженного выдоха при сокращенных бронхах и закрытой голосовой щели. В этот период внутригрудное давление достигает очень больших величин (140 мм рт. ст. и более). На фоне повышенного внутригрудного давления голосовые связки размыкаются и происходит толчкообразный стремительный выдох через рот (носовая полость в этот момент закрыта мягким небом и небным язычком (uvula palatina). Скорость движения воздуха в дыхательных путях в период толчкообразного выдоха в 20–30 раз превышает таковую при обычном дыхании. Вместе со струей воздуха при кашле из дыхательных путей в полость рта увлекаются слизь, скопления элементов, образующих мокроту, и различные чужеродные вещества, попавшие в дыхательные пути. В фазе выдоха кашель может быть прерывистым, состоящим из нескольких толчков. В таком случае в дыхательных путях происходит быстрая смена давления и скорости движения воздуха. Динамика давления и скорости движения воздуха способствует отрыву от стенок бронхов прикрепившихся к ним частиц мокроты и чужеродных компонентов и удалению их из дыхательных путей. По завершении фазы стремительного выдоха заканчивается одиночный акт кашля. Иногда такие одиночные акты могут повторяться несколько раз подряд. В таком случае говорят о кашлевой репризе (от фр. reprise — возобновление, повторение). При сильном судорожном кашле может возникать рвота, обусловленная иррадиацией раздражения на рвотный центр. Однако нужно иметь в виду, что кашель не только выполняет физиологически полезную дренажную функцию, но может оказывать и вредное воздействие на организм. Частый упорный кашель (особенно в виде длительных приступов) сопровождается повышением внутригрудного давления и может способствовать развитию гипертензии в малом круге кровообращения, эмфиземе легких, формированию легочного сердца. Повышение давления в венах большого круга кровообращения во время приступа кашля в ряде случаев сопровождается кровоизлияниями из сосудов склер, в системе бронхиальных вен. Приступ сильного кашля может осложниться обмороком, потерей сознания, нарушением ритма сердечной деятельности, эпилептиформным припадком, пневмотораксом. В подавляющем большинстве случаев кашель обусловлен раздражением рецепторов дыхательных путей и плевры. Однако он может быть связан с возбуждением центральной нервной системы, а также с раздражением рецепторов, расположенных вне органов дыхания (рис. 1). Частота и интенсивность кашля зависят от силы раздражителя, локализации этого раздражителя в органах дыхания, возбудимости кашлевых рецепторов, фазы течения болезни и, наконец, характера патологического процесса.
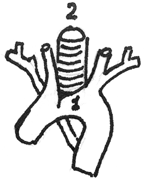
Наиболее чувствительными рефлексогенными зонами являются задняя поверхность надгортанника, передняя межчерпаловидная поверхность гортани, область голосовых связок и подсвязочного пространства, а также бифуркация трахеи и места ответвлений долевых бронхов. Количество рецепторов в бронхах убывает параллельно уменьшению их диаметра (рис. 2). Разветвления сегментарных бронхов мало- чувствительны к раздражению. При патологических процессах, ограниченных легочной паренхимой, кашель возникает только при попадании мокроты в достаточно крупные бронхи либо при вовлечении в патологический процесс плевры. Наиболее чувствительные рефлексогенные зоны плевры расположены в прикорневых участках и реберно-диафрагмальных синусах. Кашель не является специфическим симптомом какой-либо одной болезни. Для диагностики заболевания, послужившего причиной его возникновения, должны учитываться не только все сопутствующие симптомы и синдромы, выявленные у больного, но и история возникновения кашля, эпидемиологическое окружение пациента, результаты дополнительных методов исследования. Кашель имеет различный характер. Он может быть частым и редким, слабым и сильным, болезненным и безболезненным, постоянным и периодическим; он может различаться по звучности, тембру, времени возникновения в течение суток, по выделению мокроты или ее отсутствию. Наиболее мучительным бывает сухой непродуктивный кашель. Такой кашель может сохраняться несколько дней, но в некоторых случаях продолжается и в течение более длительного отрезка времени. Отрезок времени, в течение которого сохраняется кашель, может быть как относительно коротким (несколько дней), так и длительным. Относительно коротким период времени, в течение которого у детей наблюдается кашель, бывает при ряде вирусных инфекций, в том числе при гриппе, парагриппе, респираторно-синцитиальной инфекции, кори. Сухой непродуктивный кашель при некоторых заболеваниях у детейГрипп. Заболевание вызывается пневмотропными РНК-содержащими вирусами трех антигенно обособленных серологических типов (А, В и С), относящихся к семейству ортомиксовирусов. При этом заболевании кашель, как правило, возникает в среднетяжелых и тяжелых формах. Основной патологический процесс при этом разворачивается не только в эпителиальных клетках слизистой оболочки верхних дыхательных путей, но и в гортани, трахее, крупных бронхах. В этих отделах дыхательных путей выявляются дистрофические и некротические изменения эпителиальных клеток слизистой оболочки с последующим слущиванием эпителия. Кашель при гриппе характеризуется как сухой, надсадный, сопровождающийся болевыми ощущениями за грудиной. Помимо этого, при гриппе может развиться синдром крупа. В этом случае кашель становится грубым «лающим», появляются осиплость голоса и стенотическое дыхание. При диагностике основного заболевания учитывается весь комплекс его проявлений. Из клинических симптомов в первую очередь обращают внимание на минимально выраженные катаральные явления со стороны верхних дыхательных путей при наличии отчетливого токсического синдрома в виде озноба, высокой температуры тела, головной боли с преимущественной локализацией в области лба, висков, надбровных дуг, глазных яблок; у ряда детей выявляются миалгии, артралгии, явления менингизма. Конъюнктивит, ринорея при гриппе практически отсутствуют, однако заложенность носа относится к числу постоянных клинических признаков этого заболевания. Одним из осложнений гриппа может быть синдром крупа. Из лабораторных методов можно использовать экспресс-диагностику с помощью флюоресцирующих антител, способ определения ингибирующих антител к гемагглютинину вируса и реакцию нейтрализации в парных сыворотках (с интервалами между исследованиями в 8–14 дней). Парагрипп. Возбудителями заболевания являются пять типов РНК-содержащих вирусов, входящих в семейство парамиксовирусов (Paramyxoviridae). Как и вирусы гриппа, парамиксовирусы поражают эпителий верхних дыхательных путей, гортани, трахеи, крупных бронхов. Они вызывают дистрофические изменения в эпителиальных клетках указанных отделов респираторного тракта и их слущивание. Кашель при парагриппе упорный, грубый, сухой. Он может сопровождаться изменением тембра голоса. В отличие от гриппа, токсикоз при парагриппе выражен слабо, в то время как катаральные явления со стороны верхних дыхательных путей, напротив, носят отчетливый характер. Через 4–5 дней от начала заболевания может развиться стенозирующий ларингит, бронхит. В этом случае в легких выслушиваются грубые сухие хрипы. При парагриппе, как и при гриппе, может развиться синдром крупа. В этом случае появляется указанная выше триада симптомов: «лающий» кашель, осиплость голоса, стенотическое дыхание. Лабораторное подтверждение данного заболевания основывается на реакциях связывания комплемента, торможения гемагглютинации и нейтрализации антител в парных сыворотках. Сыворотки для исследования берут в начале заболевания и на 10–14-й день. Респираторно-синцитиально-вирусная инфекция (РС-инфекция). Заболевание вызывается респираторно-синцитиальными вирусами. Это РНК-содержащие вирусы семейства парамиксовирусов. Свое название данные вирусы получили в связи со способностью вызывать в культурах тканей образование синцития — структуры, возникающей в результате слияния клеток. Сухой непродуктивный кашель при респираторно-синцитиальной вирусной инфекции наиболее часто развивается у детей первого года жизни за счет вовлечения в процесс трахеи и бронхов, в том числе бронхиол. Развитие бронхиолита относится к числу характерных особенностей детей первого года (и особенно первых месяцев) жизни. Его частота среди данного контингента детей достигает 30–70%. Бронхиолит характеризуется выраженной одышкой смешанного характера, коробочным оттенком легочного звука и наличием большого количества мелких и среднепузырчатых хрипов, определяемых при аускультации грудной клетки. Рентгенологически при этой инфекции очаговые изменения в легких не выявляются, но обнаруживается острое вздутие легких и усиление рисунка корней. Синдром токсикоза при респираторно-синцитиально-вирусной инфекции выражен слабо. Температура тела, как правило, субфебрильная и повышение ее выше 38° С наблюдается редко. При диагностике РС-вирусной инфекции у детей следует учитывать такие клинические проявления, как поражение нижних дыхательных путей, несоответствие между тяжестью поражения органов дыхания и выраженностью токсикоза. Из лабораторных методов в практическом здравоохранении наибольшее диагностическое значение имеет метод экспресс-диагностики с помощью флюоресцирующих антител. Корь. Возбудитель кори также относится к группе парамиксовирусов. Как известно, постоянными проявлениями кори являются токсикоз и катар слизистой оболочки носа и верхнего отдела дыхательных путей. Часто возникают ларингиты, при которых возможно возникновение очагового некроза эпителия (нередко по краю голосовых связок). Не исключено вовлечение в патологический процесс бронхов, бронхиол и даже легочной ткани. Склонность воспалительного процесса захватывать всю толщу бронхиальной стенки и переходить на перибронхиальную ткань, а также прилежащую интерстициальную ткань легкого является отличительной особенностью кори. Кашель при кори появляется в начальный (катаральный) период. При этом заболевании он сухой, отрывистый, часто сочетается с чувством саднения в дыхательных путях. Может появиться охриплость голоса. С появлением этого симптома изменяется характер кашля: он становится грубым, хриплым. Очень важна правильная диагностика заболевания. Как известно, в катаральный период кори сыпь на коже отсутствует, и, если нет данных о наличии у пациента контактов с больным корью, заболевание расценивается как ОРВИ. Однако на 2–3-й день катарального периода кашель усиливается, становится резким и грубым, появляются гиперемия конъюнктив, пастозность (и даже отек) век, светобоязнь, энантема на мягком небе, а на слизистой оболочке щек (в области переходной складки) на уровне премоляров — мелкие беловатые точки (напоминающие манную крупу), окруженные венчиком гиперемии. Эти высыпания относятся к числу патогномоничных симптомов и известны как пятна Бельского–Филатова–Коплика. Указанные пятна обнаруживаются не только на слизистой оболочке щек, но и на слизистой губ, десен и даже конъюнктив. Они никогда не сливаются между собой, не снимаются тампоном или шпателем и представляют собой участки некротизированного эпителия. Помимо пятен Бельского–Филатова–Коплика, на слизистой оболочке десен можно обнаружить сплошные наложения серовато-белого цвета, возникающие в результате некроза и десквамации эпителия, пораженного вирусом. Диагностика кори в настоящее время большой трудности не представляет. При необходимости можно определить уровень специфических противокоревых антител. Риновирусная инфекция. Относительно сильный и непродолжительный по времени непродуктивный кашель может иметь место при риновирусной инфекции. Входя в семейство пикорнавирусов (Picornaviridae), риновирусы вызывают ОРВИ и известны как «простудные вирусы». Геном пикорнавирусов образует несегментированная молекула + РНК. Возбудитель риновирусной болезни входит в группу ЕСНО-вирусов. Это особая группа кишечных вирусов, не оказывающая патогенного действия на лабораторных животных. Их первоначально именовали «сиротскими» (Orphan) вирусами, а с 1955 г. стали называть кишечными (Enteric) цитопатическими (Cytopathogenic) человеческими (Нuman) «сиротскими» ЕСНО-вирусами. В группу пикорнавирусов, помимо ЕСНО-вирусов, входят полиовирусы I, II, III типов, вирусы Коксаки групп А и В, вирус бешенства. Риновирусы у человека вызывают легко протекающее острое респираторное заболевание. В начале этого заболевания у детей появляется познабливание, легкое недомогание, «царапание» в горле, чихание, иногда боль в ногах и головная боль. Затем добавляются заложенность носа и подкашливание. Температура тела в течение всего периода болезни остается субфебрильной. К концу первых суток дыхание через нос становится невозможным из-за полностью заложенного носа, после чего появляются обильные водянисто-серозные выделения. Вследствие обильных выделений из носа и частого использования носового платка в преддверии носа появляется мацерация кожи. Лицо обычно пастозно, склеры инъецированы, возможно появление слезотечения. В ряде случаев возникают такие симптомы, как набухание небных миндалин, легкая гиперемия передних дужек и задней стенки глотки, осиплость голоса, явления трахеита и трахеобронхита, следствием чего и является непродуктивный кашель. У детей первых 2–3 лет жизни риновирусная инфекция может осложниться синдромом крупа. Диагностика заболевания основывается на клинической картине. Для подтверждения диагноза в клинической практике используют метод экспресс-диагностики — иммунофлюоресценции, с помощью которого определяют антитела к вирусу в эпителиальных клетках, обнаруживаемых в слизи из нижних носовых раковин. Респираторный хламидиоз. Заболевание вызывается Chlamydia pneumoniae (Chl. pn.) и многими биоварами Chlamydia trachomatis (D, E, F, G, H и др.). Эти возбудители патогенны для человека. Хламидии относятся к числу облигатных внутриклеточных паразитов. Они способны выживать и размножаться только в цитоплазме инфицированных клеток. Вследствие облигатного внутриклеточного паразитирования хламидии долгое время считали крупными вирусами. В настоящее время их принято относить к бактериям. Семейство имеет один род — Chlamydia. Хламидии содержат РНК и ДНК и синтезируют собственный ДНК-протеин, имеют цитоплазматическую мембрану и клеточную стенку. Обеспечение метаболизма хламидий осуществляется преимущественно за счет жизнедеятельности клеток хозяина. Структура клеточной стенки хламидий подобна грамотрицательным бактериям. Она имеет двойную внутреннюю и двойную наружную мембраны, за счет чего обеспечивается ее прочность. Многочисленные белки наружной мембраны «врезаны» во внутреннюю мембрану. 60% общего количества белка хламидий представлены основным белком наружной мембраны. Белки хламидий содержат видо- и сероспецифические участки. Однако в белках всех трех видов хламидий (Chl. trachomatis, Chl. pneumoniae, Chl. psittaci) имеются сходные для них всех участки. Вследствие этого возможно возникновение перекрестных реакций внутри рода. В жизненном цикле хламидий имеются две формы: элементарные и ретикулярные тельца. Элементарные тельца не проявляют метаболической активности, они внедряются в клетку организма хозяина. В клетке одновременно могут находиться несколько элементарных телец. Спустя 6–8 ч после внедрения они превращаются в ретикулярные тельца, которые делятся бинарно, проделывая 6–8 циклов. Дочерние ретикулярные тельца через промежуточные стадии превращаются в элементарные тельца нового поколения, которые переполняют содержащую их клетку организма хозяина и разрушают ее. Вследствие этого элементарные тельца выходят в межклеточное пространство, заражая новые эпителиальные клетки. Каждый цикл размножения хламидий длится 48–72 ч. Однако при наличии сниженного иммунитета в организме хозяина или при неадекватной терапии цикл размножения хламидий может задерживаться в репродуктивной фазе на недели и месяцы. Следует иметь в виду, что хламидии обладают способностью превращаться в L-формы, которые, обладая слабой иммуногенностью, могут в течение длительного времени находиться внутри клеток. При иммунодефицитах любого генеза L-формы реверсируют в исходные формы и происходит их дальнейшее размножение. Chl. pn. обладает тропностью к ворсинчатому эпителию бронхов и способна полностью обездвижить ворсинки в течение 48 ч после заражения. Клиническим проявлением персистирующего легочного хламидиоза могут быть бронхиальная астма и хронический обструктивный бронхит. Среди клинических проявлений хламидийного бронхита ведущим может быть сухой непродуктивный кашель. Поражение респираторного тракта при хламидиозе наиболее характерно для детей первого года жизни. Заболевание развивается постепенно. Общее состояние детей, как правило, не нарушено, температура тела у большинства пациентов остается в пределах нормальных значений. У новорожденных детей и детей первых месяцев жизни может развиться пневмония хламидийной этиологии. Заболевание также начинается с сухого непродуктивного кашля, который постепенно усиливается и приобретает приступообразный характер. Кашель сопровождается появлением цианоза, тахипноэ, рвоты. Затем появляются одышка, «кряхтящее» дыхание и к концу первой недели — выраженные признаки пневмонии. На рентгенограммах грудной клетки выявляются множественные мелкоочаговые тени на фоне незначительного вздутия легких. Появление клинически выраженных симптомов пневмонии сопровождается изменением характера кашля — он становится влажным. С нашей точки зрения, указание на существование в начале заболевания хламидийной пневмонией сухого непродуктивного кашля связано с предшествующим хламидийным бронхитом и нисходящим распространением инфекции, приводящим, в конце концов, к хламидийной пневмонии. Диагностика респираторного хламидиоза основывается на выявлении в содержимом бронхиального дерева фрагмента генома возбудителя методом полимеразной цепной реакции, выделении хламидий в культуре клеток и обнаружении диагностически значимых титров специфических антител к Chl. pneumoniae или Chl. trachomatis, преимущественно классов IgА и IgM. Респираторный микоплазмоз. Микоплазмы — свободно живущие прокариоты, лишенные истинной клеточной стенки и не способные синтезировать ее компоненты. Функции клеточной стенки выполняет трехслойная цитоплазматическая мембрана. Микоплазмы нуждаются в холестерине и других липидных ингредиентах для синтеза компонентов мембраны. Mycoplasma pneumoniae (M. pn.), в соответствии с постулатами Коха, патогенна для человека. Она проявляет выраженный тропизм к базальной мембране мерцательного эпителия дыхательных путей. Малый размер, активная скользящая подвижность, мощный адгезивный аппарат обеспечивают прочное прикрепление микоплазмы к мембране эпителиальной клетки. Прикрепившись к клеткам респираторного эпителия, она повреждает реснички и обусловливает цитопатические изменения в клетках эпителия, выделяя супероксиданты. Последние вызывают блокаду мукоцилиарного клиренса, а затем гибель клеток и слущивание их в просвет бронха. M. pn. имеет способные к сокращению микрофибриллы, содержащие белки, иммунологически и химически сходные с мышечным белком актином. Особенностью микоплазм, в том числе и M. Pn., является то, что за счет близкого антигенного сходства их компонентов с рядом антигенов организма хозяина они плохо распознаются макроорганизмом. Это создает условия для персистенции микоплазм в организме хозяина. Респираторный микоплазмоз может протекать в виде ограниченных острых инфекций верхних дыхательных путей, в виде микоплазменного бронхита и острой микоплазменной пневмонии. При возникновении респираторного микоплазмоза слизистая оболочка ротоглотки и дыхательных путей слабо (реже умеренно) гиперемирована; дети предъявляют жалобы на боль в горле, сухость и ощущение неловкости при глотании, затрудненное носовое дыхание. При развитии микоплазменного бронхита у больных появляется сухой непродуктивный кашель и развиваются явления обструкции бронхов. Лабораторная диагностика заболевания основывается на выявлении фрагмента генома возбудителя в содержимом бронхиального дерева методом полимеразной цепной реакции и выявлении диагностически значимого титра специфических антимикоплазменных антител в сыворотке крови. Коклюш. Возбудитель коклюша Bordetella pertussis — мелкая неподвижная грамотрицательная овоидная палочка длиной 0,5–2 мкм, относящаяся к строгим аэробам. Возбудитель очень нестоек и быстро погибает под воздействием повышенной температуры, прямого солнечного света, высушивания и различных дезинфицирующих средств. Вирулентная В. pertussis обладает гистаминсенсибилизирующей активностью, содержит лимфоцитозстимулирующий фактор, термолабильный токсин цитоплазмы, фактор, активирующий островки Лангерганса. Микроорганизм имеет ворсинки (пили, фимбрии), покрывающие поверхность клетки, обеспечивающие адгезию к мерцательному эпителию дыхательных путей. Он содержит также специфический трахеальный цитотоксин, вызывающий местные повреждения, приводящие к гибели и десквамации мерцательного эпителия. Внутрибрюшинная инъекция токсина, проведенная лабораторным животным, вызывает их гибель и развитие гиперчувствительности к гистамину и серотонину. Основным клиническим проявлением заболевания является кашель. Он появляется после окончания инкубационного периода, продолжающегося в среднем около 10–12 дней после контакта с больным, и сохраняется вплоть до полного выздоровления. Однако кашель в динамике болезни претерпевает сильные изменения. В самом начале продромального периода этот кашель мало чем отличается от кашля при вышеперечисленных заболеваниях. Это сухой непродуктивный кашель, у половины детей он носит навязчивый характер. Кашель чаще беспокоит заболевшего ребенка перед сном или ночью. Температура тела, как правило, остается нормальной, реже — в течение первых нескольких дней — субфебрильной. Самочувствие ребенка не страдает. Однако кашель постепенно начинает усиливаться, приобретая все более упорный и навязчивый характер, а затем становится приступообразным. В спазматический период он приобретает «типичные черты». В этот период во время кашля быстро, друг за другом следует несколько выдыхательных толчков, сменяющихся судорожным свистящим вдохом (репризы). Приступы этого кашля заканчиваются выделением вязкой прозрачной мокроты или рвотой. Частота возникновения приступов в течение суток на высоте заболевания у разных детей варьирует от 5 до 50. Приступы спазматического кашля нарастают, достигая максимума на 2-й неделе спазматического кашля. У детей первого года жизни на фоне приступов спазматического кашля могут возникать апноэ. Диагностика заболевания наиболее затруднена в продромальном периоде. В это время следует ориентироваться на эпидемиологическую обстановку в окружении больного и динамику процесса (постепенное прогрессирование кашля при отсутствии лихорадочной реакции). Основным методом лабораторной диагностики является бактериологический. Исследуемым материалом служит слизь из верхних дыхательных путей, осаждающаяся при кашле на задней поверхности глотки. Забор материала производится двумя заднеглоточными тампонами — сухим и увлажненным забуференным физиологическим раствором. Серодиагностика при коклюше не нашла достаточно широкого применения, поскольку может использоваться только для подтверждения диагноза у непривитых детей. Паракоклюш. Возбудителем паракоклюша является Bordetella parapertussis. Возбудитель близок к Bordetella pertussis. Симптомы заболевания, включая наличие в начале клинических проявлений сухого непродуктивного кашля, такие же, как при коклюше, но заболевание протекает быстрее и значительно легче. Резюмируя вышесказанное, следует подчеркнуть, что при всех указанных выше заболеваниях наблюдается однотипный сухой непродуктивный кашель. Перечисляя характерные особенности этого кашля, следует отметить, что он усиливается и учащается при воздействии на дыхательные пути раздражающих факторов: сухого и холодного воздуха, пыли, дыма, раздражающих запахов и т. п. Возбудители всех указанных заболеваний имеют тропность к эпителию респираторного тракта, в том числе к эпителиальным клеткам мерцательного эпителия бронхов. Период существования сухого непродуктивного кашля, обусловленного указанными патогенами, относительно короток — в среднем около 1 нед. По истечении этого срока кашель становится влажным, больные начинают откашливать мокроту, что способствует естественной санации трахеобронхиального дерева. Механизм возникновения сухого непродуктивного кашля у детей при вышеуказанных заболеваниях может быть представлен следующим образом. Все возбудители перечисленных выше заболеваний относятся к группе внутриклеточных (вирусы, хламидии) и мембранных (микоплазмы, Bordetella pertussis, Bordetella раrapertussis) патогенов. Следует отметить, что, по мнению ряда исследователей, мембранные патогены (в силу плотного прикрепления к мембране клетки хозяина) также можно причислить к внутриклеточным (А. А. Ярилин, 1999). Таким образом, возбудителей всех рассмотренных выше заболеваний можно отнести к внутриклеточным патогенам. В ответ на воздействие внутриклеточных патогенов в организме формируется не гуморальный, а клеточный иммунный ответ. Проявления клеточного иммунного ответа весьма разнообразны. Наиболее распространенным и «естественным» среди них является цитотоксический ответ, т. е. иммунная реакция, приводящая к формированию антигенспецифических Т-киллеров. Антигенспецифические Т-киллеры «узнают» инфицированную клетку по экспрессии на поверхности клетки опознаваемого антигена (т. е. по соответствующему опознавательному маркеру, находящемуся на поверхности клетки). Обнаружив такую клетку и воздействуя на нее, Т-киллеры уничтожают патоген вместе с клеткой. На определенной стадии воздействия на клетку (до момента полного ее разрушения) она претерпевает определенные изменения. Изменившиеся эпителиальные клетки могут вызывать раздражение рецепторов бронхиального дерева, что и приводит к возникновению сухого непродуктивного кашля. Схема формирования кашля при инфицировании организма хозяина тропными к клеткам эпителия бронхиального дерева внутриклеточными и мембранными патогенами представлена на рисунке 3.
Очевидно, что сухой непродуктивный кашель существует до момента разрушения пораженных клеток мерцательного эпителия. Как только пораженные клетки начинают распадаться, в процесс включаются другие защитные механизмы: начинаются фагоцитоз измененных структур, выделение слизи железами слизистой оболочки, и с этого момента кашель выполняет защитную функцию по элиминации из дыхательных путей чужеродных компонентов и отмерших собственных клеток слизистой оболочки респираторного тракта. Другие заболевания и состояния, сопровождающиеся сухим непродуктивным кашлем
Сухой непродуктивный кашель встречается также при синдроме крупа, при плевритах, при поражении средостения, при патологических процессах в окружности бронхов (туморозный бронхаденит) и проводников чувствительных нервов (сдавление опухолью или увеличенными лимфатическими узлами, аневризмой аорты) (рис. 4), при диссеминированных и фиброзирующих процессах в бронхах, при попадании инородных тел в бронхи. Для детской практики наибольшее значение имеют такие состояния, как синдром крупа и попадание инородных тел в дыхательные пути. Период непродуктивного кашля при этих состояниях относительно непродолжительный. При стенозирующем ларингите (или синдроме крупа) процесс вызывается также внутриклеточными патогенами. Наиболее часто синдром крупа развивается у детей, больных гриппом, парагриппом, аденовирусной инфекцией, реже при кори и других вирусных инфекциях. Механизм развития данного состояния аналогичен вышеуказанному, но процесс локализован в области голосовых связок. Как известно, синдром крупа проявляется триадой симпомов: сухим, непродуктивным, грубым «лающим» кашлем, шумным стенотическим дыханием и сиплым голосом. Клинические проявления обусловлены воспалительными изменениями в области голосовых связок и подсвязочном пространстве, приводящими к сужению просвета гортани, в котором ускоряется ток воздуха, что, в свою очередь, приводит к высыханию слизистой оболочки и образованию корок. Уменьшение притока воздуха к легким вызывает компенсаторное усиление внешнего дыхания. В процесс включаются вспомогательные мышцы грудной клетки; таким образом, усиливается втягивание воздуха через суженный просвет гортани. Вдох при этом удлиняется, и выпадает пауза между вдохом и выдохом. Дыхание становится шумным, стенотическим. Такое дыхание является ведущим симптомом крупа. Указанный механизм частично компенсирует недостаток кислорода в организме, поддерживая газообмен в легких на должном уровне. Однако при усилении стеноза гортани минутный объем воздуха в легких уменьшается, вследствие чего возникают гипоксемия, а затем и гипоксия, сопровождающаяся нарушением клеточного метаболизма. Синдром крупа при ОРВИ развивается внезапно, часто имеет волнообразное течение, кроме того, при этом состоянии никогда не бывает полной афонии: звонкие ноты при синдроме крупа на фоне ОРВИ у детей слышны постоянно. Указанные проявления позволяют отличить данный синдром от дифтерийного крупа. Инородные тела бронхов. Клиническая картина обусловлена величиной инородного тела и уровнем обтурации. После аспирации инородного тела обычно возникает приступообразный кашель, который может быть в начале непродуктивным. Однако у детей в случае пребывания в бронхах инородного тела более суток, как правило, начинается воспалительный процесс, кашель становится влажным. Очень важно своевременно диагностировать аспирацию инородного тела в дыхательные пути. Обычно после аспирации в дыхательные пути инородного тела, помимо приступообразного кашля, появляются затрудненное дыхание, боль в груди, может развиться цианоз. При длительном нахождении инородного тела в дыхательных путях явления обструкции нарастают. В результате отека слизистой оболочки бронха частичная закупорка может перейти в вентильную, а затем и в полную — с последующим развитием ателектаза легочной ткани. Длительное пребывание в бронхах инородного тела приводит к развитию нагноительного процесса дистальнее места обтурации. При аспирации инородного тела на рентгенограммах видны рентгеноконтрастные инородные тела; о наличии нерентгеноконтрастных инородных тел могут свидетельствовать косвенные признаки: вздутие или гиповентиляция доли легкого, смещение органов средостения при вдохе в сторону расположения инородного тела (симптом Гольцкнехта–Якобсона). Расположение инородного тела можно уточнить с помощью бронхографии. Среди основных проявлений плеврита, помимо сухого непродуктивного кашля, можно упомянуть боль в груди и появление других объективных признаков данного заболевания. Диагностика заболевания облегчается, если провести рентгенологическое исследование. Сухой непродуктивный кашель, обусловленный увеличением лимфатических узлов в средостении, в области бифуркации бронхов, сдавлением чувствительных нервов аневризмой аорты, а также при наличии диссеминированных и фиброзирующих процессов в бронхах, обычно наблюдается в течение длительного отрезка времени. Поэтому существование длительного непродуктивного кашля требует тщательного обследования, проводимого с целью исключения указанных заболеваний. ЛечениеПрежде чем говорить о терапии сухого непродуктивного кашля, важно установить причину его возникновения и провести лечение соответствующего заболевания. Что же касается терапии непосредственно непродуктивного сухого кашля, то она носит сугубо симптоматический характер. Механизм возникновения сухого непродуктивного кашля при бронхите объясняет крайне малую эффективность отхаркивающих средств при его лечении. При появлении кашля, который носит такой характер, рекомендуются следующие мероприятия: Биокалиптол успокаивает раздражающий болезненный кашель, не меняя физиологию кашля. В состав биокалиптола на 100 г сиропа входит эвкалиптол (0,14 г), фолкодин (0,1 г), настойка белладонны (0,6 г) и гваякол (0,015 г). Назначается детям от 2,5 до 8 лет по 1–2 чайные ложки в день, от 8 до 15 лет — по 4–8 чайных ложек в день. Противопоказанием является возраст до 2,5 лет. Гексапневмин (в свечах) обладает антимикробным, жаропонижающим, противокашлевым действием. Имеются свечи для грудных детей и свечи для детей более старшего возраста. В состав свечи для детей грудного возраста входит биклотимола 40 мг, эвкалиптола 35 мг, парацетамола 100 мг; свечи для детей содержат беклотимола 80 мг, эвкалиптола 70 мг, парацетамола 200 мг, фолкодина 5 мг. К числу противопоказаний к применению препарата в детском возрасте относятся астматический кашель, печеночно-клеточная недостаточность. Препарат назначается детям до 30 мес — по 1 свече (для грудных детей) 2 раза в день (утром и вечером), старше 5 лет — по 1 свече (для детей) 2–3 раза в день. Пакселадин обладает противокашлевым действием. Показанием к его назначению является кашель любой этиологии. У детей препарат применяется в сиропе (в 1 флаконе сиропа вместимостью 125 мл — 10 мг/5 мл окселадина цитрата). Детям назначается сироп по 1 мерной ложке на 10 кг массы тела в сутки (детям в возрасте до 4 лет по 1–2, от 4 до 15 лет — по 2–3 мерные ложки в сутки). Следует иметь в виду, что при передозировке препарата необходимы госпитализация, контроль за деятельностью дыхательной и сердечно-сосудистой систем и симптоматическое лечение; антидот не известен. Стоптуссин обладает противокашлевым, муколитическим, отхаркивающим действием. 1 мл стоптуссина (капли для приема внутрь) содержит бутамирата цитрата 4 мг и гвайфенезина 100 мг. Цитрат бутамирата обладает бронхолитическим и противокашлевым эффектом, связанным с периферическим местноанестезирующим действием на рецепторы бронхов. Гвайфенезин снижает вязкость мокроты, улучшает ее отхождение, уменьшает частоту кашля. Препарат может быть использован у больных сахарным диабетом. К числу противопоказаний относятся гиперчувствительность и миастения. Препарат назначается внутрь после еды. Соответствующее количество капель растворяют в 100 мл жидкости (вода, чай, фруктовый сок). Дозировка препарата: детям с массой тела до 7 кг — по 8 капель 3 — 4 раза в сутки; детям с массой тела 7 — 12 кг — по 9 капель 3 — 4 раза в сутки; при массе тела 12 — 20 кг — по 14 капель 3 раза в сутки; при массе 20 — 30 кг — по 14 капель 3 — 4 раза в сутки; при массе тела 30 — 40 кг — по 16 капель 3 — 4 раза в сутки; при массе тела 40- 50 кг — по 25 капель 3 раза в сутки; при массе тела 50 — 70 кг — по 30 капель 3 раза в сутки; при массе тела 70 — 90 кг — по 40 капель 3 раза в сутки. При приеме данного препарата следует иметь в виду, что 1 мл стоптуссина содержит 280 мг этанола. Коделак содержит: кодеина 0,008 г; травы термопсиса 0,2 г; натрия гидрокарбоната 0,2 г; корня солодки 0,2 г; оказывает противокашлевое, отхаркивающее действие. Его назначают по 1 таблетке 2–3 раза в сутки. Противопоказаниями являются возраст до 2 лет, бронхиальная астма, дыхательная недостаточность любой этиологии, черепно-мозговая травма, гипотония, коллапс, нарушение ритма сердечной деятельности, нарушение функции печени и почек, интоксикационная диарея, гипокоагуляция. В дальнейшем могут быть рекомендованы различные противокашлевые препараты в зависимости от того, сохраняется у пациента сухой кашель или переходит в продуктивный. Пастилки алекс плюс, содержащие гидробромид декстрометорфана, терпингидрат и левоментол, обладают противокашлевым, отхаркивающим, спазмолитическим действием. Детям от 4 до 6 лет назначают по 1–2 пастилке 3–4 раза в день. Гликодин сироп содержит гидробромид декстрометорфана, терпингидрат, левоментол; препарат оказывает противокашлевое и муколитическое действие. Детям от 4 до 6 лет назначают по 1/4 чайной ложки, от 7 до 12 лет — по 1/2 чайной ложки 3–4 раза в день. Флуифорт выпускается в виде сиропа, содержащего лизиновую соль карбоцистеина, и в виде дозированного гранулята. Оказывает мукорегулирующее и отхаркивающее действие. Сироп назначают детям в возрасте: от 1 до 5 лет — по 2,5 мл; старше 5 лет — по 5 мл 2–3 раза в день. Детям от 12 лет флуифорт можно назначать в гранулах (содержимое пакетика растворяют в питьевой воде, перемешивают, дозировка: 1 пакетик в день). Амбробене выпускается в виде сиропа, таблеток, раствора для инъекций и раствора для приема внутрь и ингаляций. Обладает отхаркивающим и муколитическим действием. Сироп назначают детям в возрасте: до 2 лет по 2,5 мл 2 раза в сутки; от 2 до 5 — по 2,5 мл 3 раза в сутки; от 5 до 12 лет по 5 мл 2–3 раза в сутки внутрь, после еды, с достаточным количеством жидкости. Таблетки назначают детям от 5 до 12 лет по 1/2 таблетки 2–3 раза в сутки. Мукодин для детей выпускают в виде 2,5% и 5% сиропа, содержащего карбоцистеин. Препарат обладает муколитическим и отхаркивающим действием. Детям в возрасте 2–5 лет назначают по 1/2 — 1 чайной ложке 2,5% сиропа, детям в возрасте 5–12 лет — по 2 чайной ложки 2,5% сиропа или по 1 чайной ложке 5% сиропа 4 раза в сутки. Суприма-бронхо — растительный сироп от кашля. Обладает муколитическим, отхаркивающим, противовоспалительным и бронхолитическим действием. Хорошо подобранная комбинация лекарственных растений: солодка, куркума, адатода васика, базилик священный, кардамон и др. — помогает лучше справиться с кашлем. Его назначают детям 3–5 лет по 1/2 чайной ложки, детям 6–14 лет по 1/2–1 чайной ложке; с 14 лет по 1–2 чайной ложке 3 раза в сутки. Бронхолитин — сироп, содержащий гидробромид глауцина и гидрохлорид эфедрина, обладает противокашлевым и бронхорасширяющим действием. Детям старше 3 лет назначают по 1 чайной ложке 3 раза в день; старше 10 лет — по 2 чайной ложки 3 раза в день. Доктор МОМ — сироп, содержащий экстракты базилика, солодки, куркумы, имбиря, адатоды васика, паслена, девясила, перца, терминалии белерика, алоэ барбаденсис, ментола, обладает противовоспалительным и отхаркивающим действием. Его назначают детям по 1/2–1 чайной ложке 3 раза в день. Линкас — сироп, cнижает интенсивность и увеличивает продуктивность кашля, оказывает муколитическое, отхаркивающее, бронхолитическое и противовоспалительное действие за счет входящих в его состав экстрактов растений: адхатоды, солодки, длинного перца, фиалки, иссопа, альпинии, кордии, алтея, зизифуса и аносмы. Детям в возрасте от 6 мес до 3 лет сироп назначают по 1/2 чайной ложки 3 раза в день; детям в возрасте от 3 до 8 лет — по 1 чайной ложке 3 раза в день; от 8 до 18 лет — по 1 чайной ложке 4 раза в день. Л. Г. Кузьменко, доктор медицинских наук, профессор
|