Врожденная мальформация что это
Врожденная гигантская артерио-венозная мальформация у пациента старше 20 лет. Клинический разбор.
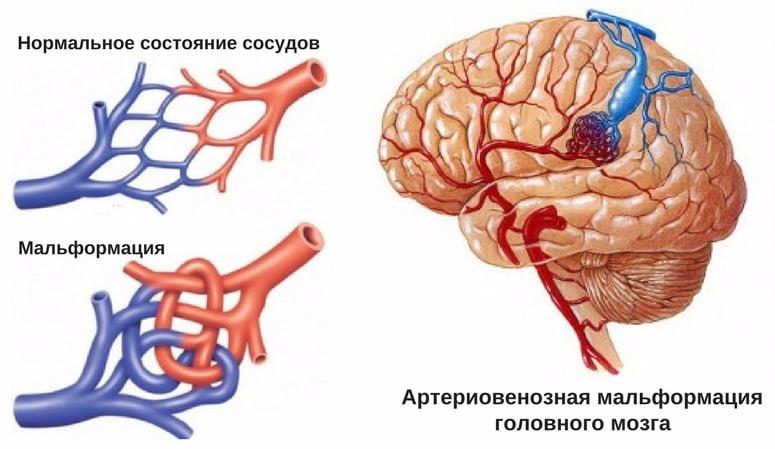
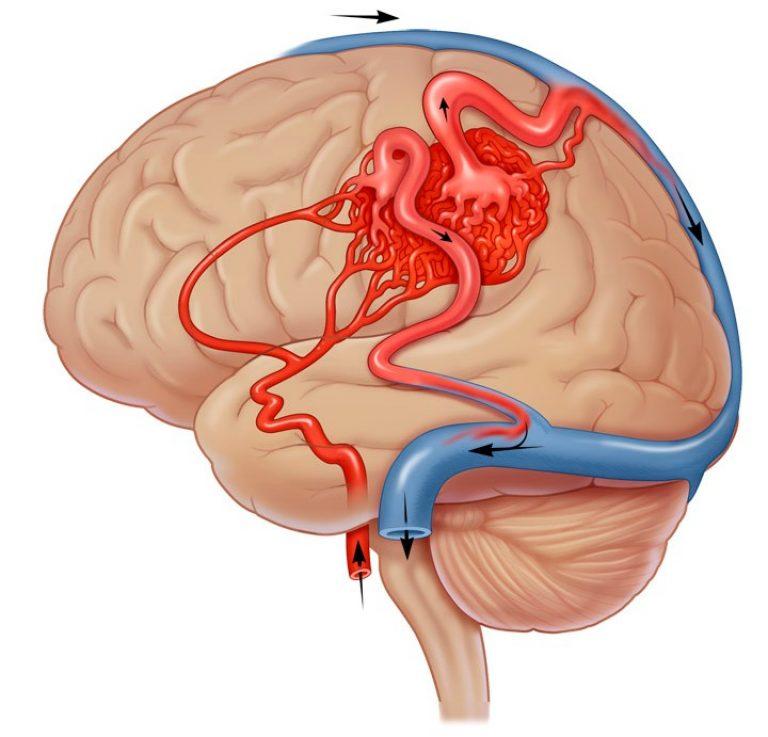
Артерио-венозная мальформация (АВМ) представляет собой врожденную аномалию сосудов, при которой в веществе мозга образуются сплетения патологических артерий и вен.
Артерио-венозная мальформация (АВМ) представляет собой врожденную аномалию сосудов, при которой в веществе мозга образуются сплетения патологических артерий и вен. При этом артериальная кровь из артерий попадает прямо в вены, минуя капиллярную сеть. Стенки этих артерий лишены полноценного мышечного слоя, в результате чего часто происходит разрыв сосуда. Вены обычно расширяются, так как принимают дополнительный объём крови. Мальформации могут располагаться на поверхности мозга или в глубоких отделах (таламусе, базальных узлах). По размерам они варьируют от небольших (диаметром несколько миллиметров) до гигантских размеров, занимающих целые доли мозга. По мировым данным частота встречаемости АВМ составляет от 0.89 до 1.24 на 100 000 населения в год.
Основные механизмы патологического влияния артерио-венозной мальформации на головной мозг:
1. Разрыв патологически измененных сосудов клубка или аневризм артерий, питающих АВМ.
2. Хроническая недостаточность кровообращения, вызванная артериовенозным шунтированием.
3. Синдром прорыва нормального перфузионного давления.
В редких случаях артериовенозная мальформация бывает настолько большой, что вызывает ишемию соседних участков головного мозга по механизму обкрадывания. Чаще всего такие мальформации встречаются в бассейне средней мозговой артерии и распространяются от коры мозга до желудочков, часто сопровождаются гидроцефалией.
По типу течения можно выделить:
1. Геморрагический тип течения заболевания – в 50 – 70 % случаев. Для этого типа течения характерно наличие у больного артериальной гипертензии, небольшой размер узла мальформации, дренаж ее в глубокие вены, а так же мальформации задней черепной ямки. Первое проявление заболевания – разрыв аневризмы.
2. Торпидный тип течения, характерен для больных с АВМ больших размеров, локализацией ее в коре, кровоснабжение ветвями средней мозговой артерии. Часто проявляется судорожным синдромом (у 26 – 67% больных), кластерными головными болями, прогрессирующим неврологическим дефицитом, как и при опухолях головного мозга. (См. таблицу №1)
Смертность от кровоизлияния составляет около 15%. Лечение АВМ должно быть комплексным. Применяется открытое хирургическое вмешательство, радиохиругия, эндоваскулярная эмболизация.
Открытым хирургическим вмешательством является радикальная экстирпация АВМ с приемлемым риском неврологических осложнений поверхностных АВМ вне функционально значимых зон головного мозга. Удаление АВМ градации 4 – 5 по шкале Spetzler-Martin сопряжено с большими техническими сложностями, очень высоким риском глубокой инвалидизации и летального исхода. АВМ расположенные в глубинных отделах, стволе мозга – недоступны.
При радиохирургическом методе возможна полная облитерация АВМ диаметром менее 3 см у 85% больных (на протяжении 2 лет). На протяжении этого периода сохраняется риск кровоизлияния.
Эндоваскулярный (эндартериальный) метод в последние годы стал методом выбора при лечении АВМ. Эндоваскулярная процедура малоинвазивна, величина, локализация АВМ не влияют на риск процедуры. Риск осложнений менее 3% (что меньше, чем годовой риск кровоизлияния). Часто применяются комбинированные методы лечения АВМ, что позволяет значительно снизить риск осложнений и радикальность вмешательства.
В настоящей статье мы приводим интересный клинический случай консервативного ведения гигантской АВМ.
Описание клинического случая
В неврологическом отделении для больных с острыми нарушениями мозгового кровообращения с палатами реанимации и интенсивной терапии наблюдался мужчина 27 лет с диагнозом: «Разрыв врожденной гигантской артерио-венозной мальформации левого полушария головного мозга. Повторные субарахноидально-паренхиматозные кровоизлияния. Симптоматическая эпилепсия. Каротидно-кавернозное соустье слева. Рецидивирующие носовые кровотечения. Хроническая постгеморрагическая железо-фолиеводефицитная анемия».
Анамнез заболевания. В 5-летнем возрасте отмечался эпизод утраты сознания с судорогами. Обследован в НИИ нейрохирургии им. Бурденко, где при ангиографии выявлена артерио-венозная мальформация в левом полушарии головного мозга. В связи с выраженным объемом мальформации и высоким операционным риском от открытого хирургического лечения воздержались, назначена симптоматическая терапия. Непродолжительное время получал тегретол. В последующие годы судорог не отмечалось. Обучался до 11 лет в обычной школе, развивался без существенных отклонений, у психологов и неврологов не наблюдался. В дальнейшем отмечалось нарастание мышечных атрофий в правых конечностях, появление контрактуры правой кисти, усиление сосудистого рисунка на лице слева. В течение многих лет имели место носовые кровотечения. За 3 недели до госпитализации кровотечения участились. Снизился аппетит, стал вялым, часто жаловался на боли в шейном отделе позвоночника. 14.08 утром упал, потеряв сознание, был обнаружен родителем лежащим на полу, отмечались судорожные подергивания в левых конечностях, была однократная рвота. С этого же времени стал жаловаться на непостоянные боли в поясничном и шейном отделе позвоночника. Амбулаторно были сданы анализы крови, отмечено резкое снижение уровня сывороточного железа, гемоглобина. Для обследования и лечения госпитализирован в КБ №1.
При поступлении в стационар 20.08: состояние тяжелое; в неврологическом статусе обращали на себя внимание: астеническое телосложение, выраженная бледность кожных покровов, череп гидроцефальной формы, значительная выраженность сосудистого рисунка на лице слева, экзофтальм (больше слева), спастический правосторонний гемипарез с развитием мышечной гемигипотрофии и сгибательных контрактур.
При дообследовании выявлено:
В ОАК при поступлении: Hв- 69г/л, эритроциты-4,06х1012, тромбоциты-360, лейкоциты-5,4х109, п/я-6%, с/я-69%, эо-1%, баз-0%, лимф-19%, мон-5%, СОЭ-3мм/ч. В биохимическом анализе крови и коагулограмме, общем анализе мочи при поступлении изменений не выявлено.
При ЭЭГ: Диффузные изменения ЭЭГ. Основной ритм покоя слева дезорганизован, замедление биопотенциалов над левым полушарием. На фоне гипервентиляции регистрируется генерализованная островолновая активность пароксизмального характера над левым полушарием.
На МРТ головного мозга (20.08): Гигантская артериовенозная мальформация левого полушария головного мозга с тотальной атрофией всего полушария, гидроцефалия. (Рис. 1)
Дуплексное исследование МАГ: расширение обеих ОСА, ПА и левой ВСА, Небольшая извитость обеих ВСА. Признаки снижения периферического сопротивления в сосудах основания мозга, наиболее выраженные в бассейне левой ВСА.
Течение заболевания:
Длительное время находился в БИН, где в первую неделю практически ежедневно на фоне терапии антиконвульсантами повторялись судорожные приступы. Далее при повторных люмбальных пункциях и КТ диагностировано повторное субарахноидальное кровоизлияние. На КТ от 01.09: отмечается отрицательная динамика в виде увеличения размеров мальформации за счет полости с геморрагическим содержимым, которая пролабирует в полость правого бокового желудочка. Нельзя исключить наличие свободной крови в левом боковом желудочке.
КТ головного мозга от 01.09.09. (Рис. 3)
Было принято решение о проведении процедур ликворофильтрации. Всего было проведено 2 процедуры экстракорпоральной фильтрации ликвора однопрокольным «маятниковым» методом. После проведения первой процедуры и санации геморрагического ликвора частота судорожных припадков уменьшилась, уменьшились общемозговые симптомы (головная боль, тошнота, сомнолентность). При этом отмечалось значительное снижение клеточного состава ликвора. Осложнений после процедуры не было.
С 04.09 отмечалось наличие у больного стойкой лихорадки, п/я сдвиг лейкоцитарной формулы влево без лейкоцитоза, признаки острого бронхита, в дальнейшем плевропневмонии и антибиотик-ассоциированной диареи. Получал следующую схему: цефтриаксон (как стартовая а/б терапия), абактал (смена с учетом чувствительности бактериального агента), ванкомицин (в составе комплексной терапии диареи).
За время госпитализации пациент также перенес госпитальную пневмонию, длительное время проводился подбор противосудорожной терапии, был консультирован эпилептологом.
На фоне проводимого лечения постепенно уменьшилась лихорадка, нормализовались водно-электролитные показатели, нормализовался стул, вырос уровень гемоглобина (112 г/л при выписке), не рецидивировали носовые кровотечения. Судорожные приступы не повторялись с 22.09. Начаты постепенные реабилитационные мероприятия. У пациента сохранялись головные боли, менингеальный синдром. 3.11 выписан домой.
Пациент наблюдается специалистами клиники по настоящее время.
Заключение
Описан клинический случай течения гигантской артерио-венозной мальформации с повторными субарахноидальными кровоизлияниями без проведения оперативного вмешательства с благоприятным исходом.
Список литературы
Коллектив авторов: Кудакова А. М., Литвинов Н. И., Каленова И. Е., Казанцева И.В., Зубанов А.Г.
Артерио-венозные мальформации
Происхождение сосудистых мальформаций
Артериовенозные соустья часто бывают множественными, имеют разнообразный калибр и форму. В зависимости от диаметра различают макрофистулы, заметные невооруженным глазом, и микрофистулы, которые выявляются только при микроскопическом исследовании тканей конечности.
Окончательно причины развития синдрома Паркса-Вебера-Рубашова не установлены. Ряд авторов рассматривают его как результат мутаций в гене RASA1, который кодирует белок p120-RasGAP, участвующий в передаче химических сигналов из внеклеточного пространства к ядру клетки. Вместе с тем, каким именно образом эти изменения приводят к специфическим сосудистым аномалиям у лиц с синдромом Паркса Вебера-Рубашова, не установлено.
Патологические соустья чаще располагаются в зоне бедренной, ветвей подколенной артерии, а также по ходу большеберцовых артерий. Интенсивный сброс артериальной крови через артерио-венозные свищи ведет к повышению давления крови в венах.
Из-за повышенной функциональной нагрузки изменяется гистологическая структура венозной стенки. Происходит утолщение ее мышечной оболочки и формирование внутренней эластической мембраны («артериализация» вены).
Значительная часть артериальной крови при наличии свищей поступает в венозное русло, минуя капиллярную сеть, поэтому возникает тяжелое кислородное голодание в тканях и нарушаются обменные процессы. Из-за венозной гипертензии усиливается нагрузка на сердце, что постепенно приводит к расширению его границ и сердечной декомпенсации.
Основные симптомы
Преимущества лечения в клинике
Диагностика

Клиническая симптоматика обусловлена нарушениями регионарного кровообращения и центральной гемодинамики. Конечность удлинена на 3-8 см, мягкие ткани ее гипертрофированы. Удлинение конечности обусловлено продуктивной перестройкой костной ткани из-за усиленной васкуляризации эпифизарных линий.
Характерно наличие варикозно расширенных поверхностных вен на нижней или верхней конечности. Их появление связано с высокой венозной гипертензией вследствие заброса крови из артерии. Стенки вен плотноэластической консистенции, с трудом сжимаемые. Расширенные вены не исчезают после придания конечности возвышенного положения. Иногда при осмотре над ними определяется пульсация.
Рука, приложенная к месту проекции артериовенозного соустья, ощущает вибрацию (симптом «кошачьего мурлыкания»). При аускультации в этой области выслушивают непрерывный систоло-диастолический шум, усиливающийся в момент систолы.
Нарушения микроциркуляции, связанные с регионарными гемодинамическими расстройствами, в ряде случаев приводят к образованию язв и некрозов дистальных отделов конечностей. Из язв часто возникают повторные обильные кровотечения, приводящие к тяжелой анемии. Нередко бывает гипертрихоз и гипергидроз.
Ряд клинических симптомов связан с изменениями центральной гемодинамики. При значительной венозной гипертензии увеличивается нагрузка на правые отделы сердца, следствием ее являются гипертрофия сердечной мышцы, увеличение ударного и минутного объема сердца Однако по мере прогрессирования заболевания сократительная функция сердца начинает ослабевать, происходит миогенная дилатация сердца с расширением его полостей Развивается сердечная недостаточность, проявляющаяся одышкой, сердцебиениями, отеками, застойной печенью, асцитом, анасаркой. Для врожденных артериовенозных свищей характерно урежение пульса, наступающее после пережатия приводящей артерии.
Реографическая кривая, записанная с сегмента конечности, где расположены артериовенозные соустья, характеризуется высокой амплитудой, отсутствием дополнительных зубцов на катакроте, увеличением реографического индекса. В дистальных сегментах конечности амплитуда кривой, напротив, снижена. Артериализация венозной крови ведет к увеличению насыщения ее кислородом, содержание которого в расширенных венах увеличивается на 20-30%.
Наиболее важным методом диагностики врожденных артериовенозных свищей является ангиография. Различают прямые и косвенные ангиографические признаки артериовенозных свищей Наличие на ангиограммах контрастированного соустья или сосудистой полости, сообщающейся с артерией и веной, относят к прямым признакам. Косвенно о наличии свища свидетельствуют одновременное контрастирование артерий и вен, расширение просвета приводящей артерии, обеднение сосудистого рисунка дистальнее расположения артериовенозного свища.
Понятие мальформации, разновидности и пути лечения. Справка
Сосудистая мальформация обозначает неправильное соединение артерий, вены или обеих. Он включает мальформацию нормальных вен (венозная ангиома) или артерий напрямую переходящих в вены (артериовенозная мальформация или АВМ). Эти мальформации являются врожденными, и точная причина их образования неизвестна.
Масштабы сосудистых мальформаций бывают самыми разными. Мальформации в особо крупных размерах могут вызывать головную боль, сдавливание головного мозга, приводить к кровоизлияниям и эпилептическим припадкам.
Чаще всего, встречается такая разновидность сосудистых мальформаций как артериовенозная. Ей характерно переплетение извитых тонкостенных сосудов, объединяющих между собой артерии и вены. Исходя из многочисленных исследований, эти сосуды образуются из артериовенозных свищей, которые с течением времени увеличиваются. В результате этого заболевания приносящие артерии расширяются, а их стенки гипертрофируются по выносящим венам течёт артериальная кровь.
В медицинской практике встречаются как небольшие, так и огромные мальформации. При сильно развитых мальформациях, кровоток становится достаточно сильным для того, чтобы существенно увеличить сердечный выброс. Вены, идущие от мальформаций, имеют вид гигантских пульсирующих сосудов.
Артериовенозные мальформации могут образовываться во всех отделах полушарий головного мозга, в стволе мозга и в спинном мозге, однако наиболее крупные из них образуются в задних отделах полушарий мозга. У мужчин артериовенозные мальформации встречаются чаще и могут появляться у разных членов семьи на протяжении одного или нескольких поколений.
Крайне редки повторные кровоизлияния в первые недели заболевания, поэтому антифибринолитические препараты (понижающие фибринолитическую активность крови) медики не назначают.
В медицинской практике известны случаи как массивного кровоизлияния, быстро приводящего к смерти, так и небольшие (диаметром около 1 см). В последнем из вариантов оно сопровождается лишь минимальными очаговыми неврологическими патологиями или протекает бессимптомно.
Диагноз АВМ устанавливается по Магнитно-резонансной томографии (МРТ), Компьютерной томографической ангиографии (КТ-ангиографии) и церебральной ангиографией. АВМ могут раздражать окружающий мозг и вызывать судороги, головные боли. Нелеченные АВМ могут увеличиваться и разрываться, приводя к внутримозговому кровоизлиянию и невосполнимому разрушению мозга.
Существуют три вида лечения мальформации: прямое микрохирургическое удаление, стереотаксическая радиохирургия и эмболизация (закупоривание кровеносных сосудов) с помощью нейроэндоваскулярного метода. Хотя микрохирургическое лечение часто позволяет удалить всю мальформацию, в некоторых случаях применяют комбинацию различных методов. К сожалению, использование стереотаксической радиохирургии возможно лишь при размерах мальформации не более 3,5 см. Воспаление в стенке сосуда, которое вызывает облучение, ведет к постепенному (до 2 лет) закрытию мальформации. При эмболизации в просвет питающего сосуда проводится тонкий катетер и вводится клей или мелкие частицы. Иногда нейроэндоваскулярный метод облегчает прямое удаление мальформации или уменьшает ее размеры для проведения стереотаксической радиохирургии.
Данное заболевание названо в честь австрийского патолога Ханса Киари (Hans Chiari), который в 1891 году описал несколько типов аномалий развития ствола мозга и мозжечка. Наиболее распространены аномалии Киари I и II типа, и поэтому в дальнейшем речь пойдет только о них.
При аномалии Киари низко расположенные миндалины мозжечка затрудняют свободную циркуляцию спино мозговой жидкости между головным и спинным мозгом. Миндалины блокируют большое затылочное отверстие, как пробка затыкает бутылочное горлышко. В результате нарушается отток ликвора (спинномозговой жидкости) и развивается гидроцефалия (водянка головного мозга).
Мальформация Киари I типа характеризуется смещением миндалин мозжечка вниз через большое затылочное отверстие к верхним отделам спинного мозга. Этот тип мальформации сопровождается гидромиелией (расширение центрального канала спинного мозга) и обычно проявляется в подростковом или взрослом возрастах.
Самым частым симптомом является головная боль. Особенно характерна боль в затылочной области, усиливающаяся при покашливании и натуживании; боли в шее; слабость и нарушения чувствительности рук; неустойчивая походка; двоение в глазах, смазанная речь, затрудненное глотание, рвота, шум в ушах.
Лечение: нейрохирургическая операция по декомпрессии задней черепной ямки.
При наличие гидроцефалии проводится шунтирование.
Мальформация Киари II типа, называемая также мальформацией Арнольд Киари.
Данное заболевание названо в честь немецкого патологоанатома Юлиуса Арнольда, который описал в 1984 году данное заболевание.
Частота этого заболевания составляет от 3,3 до 8,2 наблюдений на 100 тыс. населения.
При аномалии Арнольда Киари наблюдается врожденное увеличение диаметра большого затылочного отверстия. В увеличенное отверстие может выпасть и вклиниться нижний отдел мозжечка (миндалины мозжечка), что приводит к взаимному сдавлению мозжечка и спинного мозга. В сочетании возможны также гидроцефалия (повышенное давление жидкости в полости черепа), сердечно сосудистые аномалии, закрытый задний проход и другие нарушение пищеварительного тракта, нарушение развития мочеполовой системы.
Хотя причина мальформации Киари точно не известна, существует несколько обоснованных теорий, указывающих на смещение мозжечка вследствие повышения давления в вышележащих отделах.
Диагноз устанавливается по результатам магнитно резонансной томографии. При необходимости выполняется компьютерная томография с трехмерной реконструкцией затылочной кости и шейных позвонков. Проведение магнитно резонансной томографии позволяет нейрохирургам точно определить величину смещения мозжечка, определить форму мальформации и степень прогрессирования заболевания.
В тяжелых случаях возможно развитие состояний, угрожающих инфарктом головного и спинного мозга.
Лечение мальформации Киари и сопутствующей сирингомиелии (хроническое прогрессирующее заболевание нервной системы, при котором в спинном мозге образуются полости) возможно, к сожалению, лишь хирургическим путем. Операция состоит в местной декомпрессии или установке ликворного шунта. Местная декомпрессия выполняется под наркозом и состоит в удалении части затылочной кости, а также задних половин I и/или II шейных позвонков до того места, куда спускаются миндалины мозжечка. Эта эффективная операция расширяет большое затылочное отверстие и устраняет сдавление ствола мозга, спинного мозга и миндалин мозжечка. Во время операции открывается также твердая мозговая оболочка толстая мембрана, окружающая головной и спинной мозг. В раскрытую твердую мозговую оболочку вшивается заплатка из другой ткани (искусственной или взятой у самого больного) для более свободного прохождения ликвора.
Реже выполняются операции по дренированию спинномозговой жидкости из расширенного спинного мозга в грудную или брюшную полость специальной полой трубкой с клапаном (шунтом) или в подоболочечное пространство. Иногда эти операции выполняются поэтапно.
Артериовенозные мальформации сосудов головного мозга: лечение, операции и последствия
Артериовенозная мальформация (АВМ) головного мозга – это локальный дефект архитектоники внутричерепных сосудов, при котором формируется беспорядочное соединение между артериями и венами с образованием извитого сосудистого клубка. Патология возникает вследствие ошибки морфогенеза, а потому в основном является врожденной. Может быть одиночной или распространенной.
При мозговой АВМ кровоток осуществляется аномально: кровь из артериального бассейна прямиком, обходя капиллярную сеть, перебрасывается в венозную магистраль. В зоне мальформации отсутствует нормальная промежуточная капиллярная сеть, а связующий узел представлен фистулами или шунтами в количестве 1 и более единиц. Стенки артерий дегенерированы и не имеют надлежащего мышечного слоя. Вены, как правило, расширены и истончены по причине нарушенной ауторегуляции мозгового кровотока.
АВМ головного мозга, как и аневризмы, опасны внезапным внутримозговым кровоизлиянием, которое возникает вследствие разрыва стенки патологического сосуда. Разорвавшаяся мальформация чревата ишемией мозга, отеком, гематомой, прогрессией неврологического дефицита, что не всегда для больного заканчивается благополучно.
Статистика заболеваемости и последствий патологии
Артериовенозная мальформация в структуре всех патологий с объемными образованиями в тканях головного мозга в среднем составляет 2,7%. В общей статистике острых нетравматических геморрагий в субарахноидальное пространство, 8,5%-9% случаев кровоизлияний происходят по причине мальформаций. Инсультов головного мозга – 1%.
Встречаемость заболевания происходит со следующей средней частотой в год: 4 случая на 100 тыс. населения. Некоторые зарубежные авторы указывают другую цифру – 15-18 случаев. Несмотря на врожденную природу развития, клинически проявляется только у 20%-30% детей. Причем возрастной пик обнаружения АВМ ГМ у детей приходится на младенчество (≈13,5%) и возраст 8-9 лет (столько же %). Считается, что у ребенка с таким диагностированным сосудистым нарушением риски разрыва гораздо выше.
По статистике, мальформации проявляют себя по большей мере в возрасте 30-40 лет, поэтому диагностируются чаще у людей именно этой возрастной группы. Заболевание обычно протекает скрыто в течение десятков лет, чем и объясняется такая тенденция его определения далеко не в детские годы. Половой закономерности в развитии церебральных АВМ у мужского и женского пола пациентов не обнаружено.
При наличии мальформации ГМ вероятность разрыва составляет от 2% до 5% в год, с каждым последующим годом риски увеличиваются. Если кровоизлияние уже состоялось, риск его повторного рецидива существенно возрастает, вплоть до 18%.
Летальные исходы из-за внутричерепного кровоизлияния, которое часто является первым проявлением болезни (в 55%-75% случаев), случаются у 10%-25% пациентов. Смертность вследствие разрыва, согласно исследованиям, больший процент имеет у детей (23%-25%), чем у взрослых людей (10%-15%). Инвалидизация от последствий заболевания отмечается у 30%-50% больных. Примерно к 10%-20% пациентов возвращается полноценное или приближенное к норме качество жизни. Причина такой грозной тенденции заключается в поздней диагностике, несвоевременном получении квалифицированной медицинской помощи.
В какой части головы локализируются АВМ головного мозга?
Распространенная локализация артериовенозной аномалии – это супратенториальное пространство (верхние отделы мозга), проходящее над палаткой мозжечка. Чтобы было понятнее, изъяснимся проще: сосудистый дефект примерно в 85% случаев обнаруживается в больших полушариях. Преобладают поражения сосудистых звеньев теменной, лобной, затылочной, височной долей больших полушарий.
В целом, АВМ могут располагаться в любом полюсе головного мозга, причем как в поверхностных частях, так и глубинных слоях (таламусе и др.). Достоверно определить точную локализацию очага возможно только после прохождения аппаратного исследования с возможностями визуализации мягких тканей. К базовым принципам диагностики относят МРТ и метод ангиографии. Эти методы позволяют качественно оценить порядок ветвления артерий и построение вен, их соединение между собой, калибр ядра АВМ, афференты артерий, дренирующие вены.
Причины развития артериовенозного порока и симптомы
Заболевание является врожденным, поэтому анормальная закладка сосудов в определенных зонах мозга происходит в ходе внутриутробного периода. Достоверные причины развития патологии до текущего момента так и не установлены. Но, по словам специалистов, на аномальное строение сосудистой системы ГМ у плода предположительно могут способствовать негативные факторы в течение беременности:
Специалисты также полагают, что в формировании порока может играть роль и генетический фактор. Наследственность до недавнего времени не воспринималась как причина патологии серьезно. Сегодня же все больше поступает сообщений о причастности и данного фактора. Так, в ряде случаев у кровных родственников больного определяются аналогичного типа сосудистые пороки. Предположительно их вызывает передающаяся по наследству генная мутация, затрагивающая хромосому 5q, локус СМС1 и RASA1.
Как было сказано ранее, для заболевания характерно продолжительное «немое» течение, которое может продолжаться десятилетиями. О диагнозе либо узнают случайно в момент диагностического обследования структур головного мозга, либо уже после случившегося разрыва мальформации. В немногочисленных вариантах болезнь может давать о себе знать до того как лопнет сосуд. Тогда клиника патологии чаще проявляется такими симптомами, как:
Клиническая картина при разрыве АВМ подобна всем типам внутричерепных кровоизлияний:
У детей заболевание зачастую проявляется отставанием в психическом развитии, задержкой речевых функций, эпиприступами, симптомами сердечной недостаточности, когнитивными нарушениями.
Виды церебральных мальформаций венозно-артериального русла
Патологические образования принято различать по топографо-анатомическому признаку, гемодинамической активности, размерам. Первый параметр характеризует место расположения мальформации в головном мозге, отсюда происходят их названия:
По гемодинамической активности выделяют мальформации:
Поражение также оценивается по размерам, учитывается диаметр только клубка мальформации. При диагностике размеров используют следующие наименования АВМ:
Для предупреждения тяжелой геморрагии и связанных с ней необратимых осложнений крайне важно выявить и устранить очаг в ближайшее время, до разрыва. Почему? Объяснение куда более убедительное – при разрывах слишком большой процент людей погибает (до 75% пациентов) от обширного кровоизлияния, несопоставимого с жизнью.
Необходимо понимать, что сосуды АВМ слишком подвержены прорывам, так как они серьезно истощены на почве ненормального строения и нарушенного тока крови. Одновременно с этим, крупные порочные образования сдавливают и повреждают окружающие мозговые ткани, что несет дополнительную угрозу состоятельности функций ЦНС. Поэтому, если диагноз подтвержден клинически, оттягивать с лечением ни в коем случае нельзя.
Методы лечения мальформаций сосудов головного мозга
Терапия заключается в полной резекции или полноценной облитерации сосудистого дефекта хирургическим путем. Существует 3 вида высокотехнологичных операций, которые применяются в этих целях: эндоваскулярное лечение, стереотаксическая радиохирургия, микрохирургическое вмешательство.
Видео открытой операции можно посмотреть по ссылке: https://www.youtube.com/watch?v=WA2FTX1NK1Y
В определенных ситуациях невозможно сразу приступить к прямой микрохирургии ввиду высоких интраоперационных рисков, особенно при АВМ больших размеров. Или же другой вариант: ангиома после стереотаксии или катетерной эмболизации лишь частично компенсирована, что крайне плохо. Поэтому иногда целесообразно обращаться к поэтапному лечению, используя последовательную комбинацию нескольких ангионейрохирургических методов.
Где лучше оперироваться и цены операции
Грамотно спланированный алгоритм лечебных действий поможет полностью удалить сосудистый конгломерат не в ущерб жизненно важным тканям. Адекватность терапии с учетом принципа индивидуальности убережет от прогрессии неврологических отклонений, возможного раннего рецидива со всеми вытекающими последствиями.
Оперировать высший орган ЦНС, который отвечает за множество функций в организме (двигательные способности, память, мышление, речь, обоняние, зрение, слух и пр.), следует доверять мирового уровня нейрохирургам. Кроме того, медучреждение должно быть снаряжено широкой базой высокотехнологичного интраоперационного оборудования передового образца.
В зарубежных странах с высокоразвитой нейрохирургией услуги стоят дорого, зато там, что называется, возвращают пациентов к жизни. Среди популярных направлений, одинаково продвинутых в хирургии головного мозга, выделяют Чехию, Израиль и Германию. В чешских клиниках цены на медицинскую помощь по поводу артериовенозных мальформаций самые низкие. Невысокая стоимость, совершенная квалификация чешских врачей-нейрохирургов сделали Чехию самым востребованным направлением. В это государство стремятся попасть не только пациенты из России и Украины, но и Германии, Израиля, других стран. И коротко о ценах.