циталомегавирус что это у новорожденных
Цитомегаловирус у детей
Содержание
Цитомегаловирус – одна из разновидностей герпеса. Практически каждый человек на земле является носителем вируса герпеса, и большая часть людей заражается им в детстве.
Большую часть времени вирус находится в «дремлющем» состоянии. Однако некоторые его проявления могут быть опасны для здоровья.
Цитомегаловирус попадает в организм, как и все остальные виды герпеса. Если иммунитет человека в норме, данный вирус может никак себя не проявлять неограниченное количество времени.
Причины и пути заражения
Основная причина – это вирус HCMV-5, передающийся от человека к человеку. У детей старше нескольких месяцев и взрослых заражение происходит почти бессимптомно и в большинстве своей не представляет особой опасности для здоровья.
Но ребенок может заразиться этим вирусом еще до появления на свет, т.е. в данном случае речь идет о врожденном вирусе. И тогда цитомегаловирус может нанести серьезный урон организму. С высокой долей вероятности могут возникнуть пороки развития, серьезные нарушения в нервной системе и системе пищеварения, в сердечно-сосудистой и опорно-двигательной системах, а также возможны необратимые поражения органов слуха и зрения. Источник:
А.И. Смирнова, Е.В. Россихина, Н.С. Дюпина
Роль цитомегаловирусов в акушерской патологии и неонатологии // Вятский медицинский вестник, 2010.
Вирус проникает через плаценту, поэтому поражает детей еще на этапе внутриутробного развития, может передаваться во время родов и кормления грудью.
Основные пути заражения, которые с вероятностью 98% приводят к заболеванию:
Симптомы
Если инфекция развивается у детей в период новорожденности, ей могут сопутствовать симптомы:
Цитомегаловирус может развиваться и бессимптомно, что наиболее опасно. Вследствие бессимптомного протекания инфекции у детей могут развиваться изменения скелета черепа, недостаток массы тела, нарушения умственного развития.
Приобретенная инфекция (когда ребенок заразился в старшем возрасте) может протекать со следующими симптомами:
Чаще всего инфекция проходит без какого-либо специфического лечения при заражении в более взрослом, чем грудничковый, возрасте. Но если симптомы инфекции не проходят спустя 2 месяца, срочно обратитесь к врачу!
Методы диагностики заболевания
Комплексное обследование при подозрении на цитомегаловирус состоит из ряда лабораторных анализов. Антигены и антитела могут обнаруживаться в слюне, крови, выделениях. Как вспомогательная методика проводится цитология. Точный диагноз ставится, когда выявлена ДНК вируса HCMV-5 в слюне, крови и моче. Может быть назначен анализ ПЦР, ИФА. Грудным детям делают только анализ крови, потому что другая диагностика затруднена.
Лечение
Лекарственная терапия применяется при заражении ребенка в новорожденном возрасте или при тяжелом течении заболевания. Лечение направлено не на полное избавление от вируса, что физически невозможно, а на снижение его активности. Для лечения чаще всего применяются антигерпетические препараты. Для составления схемы лечения обратитесь к педиатру.
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
История
Исходя из теории ко-эволюции вирусов с их хозяевами, считается, что герпетические вирусы появились в кембрийский период. В человеческой популяции герпетические вирусы распространены на протяжении тысячелетий. 24 ноября 1974 г. американским антропологом Д. Джохансоном в Великой рифтовой долине был обнаружен скелет афарского австралопитека Люси — предполагается, что это ветвь прародителей Homo sapiens [1]. Возраст Люси определен как 3,2–3,5 млн лет. В «слюне» Люси найдены три герпетических вируса — ЦМВ, вирус Эпштейна–Барр (ВЭБ), вирус простого герпеса 1-го типа (ВПГ 1-го типа). «Современные» люди, мигрировавшие из Африки от 60 до 100 тысяч лет назад, были уже носителями ЦМВ, ВЭБ, ВПГ 1-го типа и ВПГ 2-го типа. Человек со времен афарского австралопитека инфицировался вирусами в раннем детстве в семьях с большим количеством детей; вирусы передавались контактным путем со слюной, в грудном молоке и пр. Под воздействием, в том числе, и герпетических вирусов как компонентов комменсальной микробиоты, передаваемой от матери, эволюционировала иммунная система человека [2].
Характеристика возбудителя
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Патогенез
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
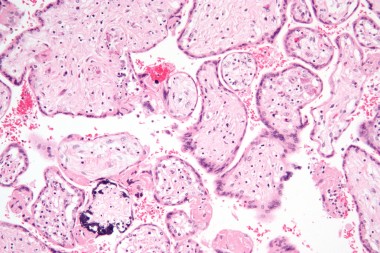
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Клиника ЦМВИ
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
У новорожденного антенатальная ЦМВИ проявляется симптомами «тяжелой инфекции» с полисистемным поражением: задержкой внутриутробного развития, часто — недоношенностью, гепатоспленомегалией, затяжной неконъюгационной и конъюгационной желтухой, тромбоцитопенической пурпурой, анемией, ДВС-синдромом с кровоизлиянием во внутренние органы, прежде всего в мозг, пневмонией, микроцефалией, хориоретинитом, увеитом, кардитом, различными вариантами поражения центральной нервной системы, в том числе продуктивным вентрикулоэнцефалитом с прогрессирующей гидроцефалией, а также — кортикальными или мозжечковыми пороками развития [13]. В дальнейшем этим детям присущи недостаточная прибавка веса, задержки психического и моторного развития, мышечная слабость, часто — длительная субфебрильная температура, стойкая анемия и тромбоцитопения, длительный гепатит с холестатическим синдромом и высоким риском фиброза и цирроза печени, мальабсорбция.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
Цитомегаловирусная инфекция у детей
Цитомегаловирусная инфекция у детей (ЦМВИ) – типичный представитель оппортунистических инфекционных заболеваний, клинически проявляющихся только на фоне иммунодефицитных состояний.
Цитомегалия — это вирусное заболевание, которое проявляется множеством симптомов, которые возникаюь из-за образования гигантских клеток с типичными внутриядерными и цитоплазматическими включениями в слюнных железах, висцеральных органах и центральной нервной системе.
Цитомегаловирусная инфекция, согласно международной классификации, бывает таких видов:
Также существует врожденная цитомегаловирусная инфекция и цитомегаловирусный мононуклеоз.
Цитомегалия бывает врожденной или приобретенной. При врожденной могут быть поражены многие органы и системы ребенка, такую форму болезни называют генерализированной.
Приобретенная цитомегалия у детей раннего возраст протекает по типу мононуклеозоподобного синдрома. В некоторых случаях вирус преимущественно поражает желудочно-кишечный тракт, легкие, печень. Или же болезнь может принять генерализированную форму. Обе формы (врожденная и приобретенная) могут проходить бессимптомно. Согласно классификации по признаку течения, цитомегалия бывает острой и хронической.
Что провоцирует / Причины Цитомегаловирусной инфекции у детей:
Возбудитель – ДНК-содержащий вирус семейства Herpes-viriae – Cytomegalovirus hominis. Источником цитомегаловирусной инфекции у детей является мать. Механизмы передачи: вертикальный и интранатальный.
Пути передачи – гематогенный (трансплацентарный), восходящий, контактный, аспирационный (при заглатывании инфицированных околоплодных вод). У детей первого года жизни возможно инфицирование через грудное молоко. Дети раннего возраста могут инфицироваться контактно-бытовым, воздушно-капельным, трансфузионным путем.
Эпидемиологические особенности ЦМВИ (широкое распространение цитомегаловируса в человеческой популяции, различные механизмы и пути передачи, преобладание субклинических форм инфекции), а также особенности иммунитета у беременных и плода способствуют повышенному риску внутриутробного инфицирования вирусом цитомегалии.
У больных цитомегаловирусной инфекцией клетки, зараженные вирусом, обнаруживают в осадке мочи, слюне, спинномозговой жидкости и пораженных органах. Вирус сохраняет жизнедеятельность в среде, имеющей комнатную температуру. Он имеет чувствительность к дезинфицирующим средствам и эфиру. Вирус устойчив к антибиотикам.
Патогенез (что происходит?) во время Цитомегаловирусной инфекции у детей:
У новорожденных детей встречается в 0,2-2,5% случаев. Клинические формы врожденной цитомегаловирусной инфекции у детей: бессимптомная, генерализованная. У 80% детей, перенесших генерализованную ЦМВИ, в дальнейшем отмечается неврологическая симптоматика, у 17% детей при бессимптомном течении заболевания отмечается минимальная мозговая дисфункция, задержка развития, неврозоподобные расстройства.
Вирус цитомегалии, поступивший в ранее неинфицированный организм, проникает внутрь клеток и начинает активно реплицироваться. Внутриклеточное проникновение цитомегаловируса (ЦМВ) обусловлено взаимодействием гликопротеинов вирусной оболочки с рецепторами клетки-мишени. В результате этого взаимодействия вирусный капсид проникает и клетку, ДНК вируса достигает ядра инфицированной клетки, изменяет синтез нуклеиновых кислот. Начинается процесс репликации, результатом которого является образование дочерних вирусов. Пораженные ЦМВ клетки гипертрофируются, в них увеличиваются ядра. На конечной стадии трансформации инфицированные клетки приобретают типичные признаки в виде «совиного глаза» (увеличенная клетка, в которой протоплазма из-за большого размера ядра визуализируется лишь в виде тонкой полоски). В результате поражения клеток, к которым тропен 11МВ, возникают интерстициальное воспаление, васкулит, дистрофические изменения в окружающих тканях. Одновременно отмечается лимфоидногистиоцитарная инфильтрация.
Скорость репликации и инфицирования дочерними вирусами незараженных клеток зависит от функционального состояния иммунной системы. Неспецифические факторы иммунитета – система интерферона, комплемента, естественные киллеры – на первых этапах инфекционного процесса замедляют скорость распространения возбудителя, а в дальнейшем потенцируют активность специфического иммунитета и препятствуют инфицированию непораженных клеток. Однако наиболее действенной защитой от ЦМВИ является создание специфического иммунитета (образование специфических антител и специфических Т-лимфоцитов). Специфическая иммунная защита может формироваться только в том случае, если вирусы расположены и неклеточно. Внутриклеточное расположение вируса защищает его от иммунного воздействия.
Клинические проявления: риск инфицирования плода, тяжесть заболевания новорожденного ребенка и дальнейший прогноз при внутриутробной ЦМВИ зависят от характера течения инфекционного процесса у матери в период беременности. Если женщина, не имеющая иммунитета к вирусу цитомегалии, впервые инфицируется им в период беременности, то это приводит к развитию у нее первичной ЦМВИ. Частота передачи цитомегаловируса при первичной инфекции от серонегативной беременной плоду составляет от 30 до 50%. Следует отметить, что в большинстве случаев отмечается бессимптомное течение инфекции у женщин. При вторичной цитомегаловирусной инфекции риск внутриутробного инфицирования плода значительно ниже (2%).
Симптомы Цитомегаловирусной инфекции у детей:
Клинические проявления внутриутробной ЦМВИ:
Клиническая картина приобретенной цитомегалии. Инкубационный период может длиться минимум 15 дней, максимум 3 месяца. Всё это время ребенок является носителем инфекции.
При приобретенной цитомегалии ребенок заражается от матери или медперсоналав роддоме в том случае, если данные взрослые – носители вируса. Если малышу делают переливание плазмы/крови от доноров, и кровь недостаточно проверена, возможно заражение.
Болезнь может проявиться в изолированном поражении слюнных желез, либо инфекция поражает, помимо слюнных желез, еще и висцеральные органы. Приобретенная цитомегалия редко бывает генерализированной. У ребенка постепенно повышается температура. Среди симптомов отмечают такие: боли в горле, увеличение шейных лимфатических узлов, печени и селезенки. Могут быть головные боли, боли в животе, анорексия, ощущение слабости в теле.
Слизиста оболочка ротоглотки чуть красновата, можно наблюдать увеличение небных миндалин.
В других случаях могут проявляться симптомы интерстициальной пневмонии, такие как цианоз, одышка и пр. Не исключены желудочно-кишечные расстройства, проявляющиеся в учащении стула и рвоте. Может наблюдаться также нарушение печеночных функций, например, потемнение мочи, желтуха и т. д., а также изменения в мочи.
Болезнь длится долго. Температура может ежедневно повышаться до уровня 39—40 ˚ С. Ребенок во время подъемов температуры ощущает озноб, что может длиться от 2 до 4 недель, редко – более длительный срок.
Если заражение возникло вследствие переливания крови, через 5-6 недель после процедуры возникает цитомегаловирусный мононуклеозоподобный синдром.
Генерализированная форма приобретенной цитомегаловирусной инфекции отличается тем, что вирус постепенно поражает многие органы и системы в организме ребенка. Лихорадка длительная, проявляется общеинфекционный токсикоз. Вирус поражает легкие, что приводит к интерстициальной пневмонии. Поражение желудочно-кишечного тракта проявляется в повторяющихся приступах рвоты и жидком многократном стуле. Вирус при генерализированной форме поражает сердечно-сосудистую систему. Фиксируются явления паренхиматозного гепатита, энцефалита. Течение генерализированной формы длительное.
Диагностика Цитомегаловирусной инфекции у детей:
Чтобы диагностировать наличие цитомегаловирусной инфекции у детей проводиться лабороторное исследование крови на специфические антитела к цитомегаловирусу – иммуноглобулинов М и G.
Обнаружение иммуноглобулинов М может указывать на первичное заражение цитомегаловирусами либо на реактивацию хронической цитомегаловирусной инфекции. Высокие титры IgМ у беременных могут способствовать инфицированию плода. Повышение IgМ определяется в крови через 4-7 недель после заражения вирусом и наблюдается в течение16-20 недель.
Повышенные иммуноглобулины G развиваются в период снижения активности цитомегаловирусной инфекции. Их наличие в крови указывает на цитомегаловирус в организме, но не показывает активности инфекционного процесса.
С помощью ПЦР-диагностики определяется ДНК цитомегаловируса в клетках крови и слизистых – соскобы из уретры и цервикального канала, мокроты, слюна и т.д. Эффективным способом диагностики является проведение количественной ПЦР, которая показывает активность цитомегаловируса и вызываемого им инфекционного процесса. Диагноз ставится, когда выделение цитомегаловируса в забранном материале пошается.
Зависимо от того, какой орган пострадал от инфекции, пациент проходит осмотр гинеколога, гастроэнтеролога, андролога или других докторов. Дополнительно может назначаться проведение УЗИ органов брюшной полости, гастроскопия, кольпоскопия, МРТ головного мозга и другое.
Лечение Цитомегаловирусной инфекции у детей:
В настоящее время существует два основных направления терапии и профилактики вирусных инфекций. Это виростатические препараты и специфические иммуноглобулины. Эти два вида терапии имеют принципиальные отличия в механизме противовирусного действия.
Ганцикловир назначают внутрь во время еды, а также вводят внутривенно. Биоусвоение из желудочно-кишечного тракта равно 15-20%, тем не менее этого достаточно для оказания эффекта. У препарата высокая активность и он обладает способностью избирательно накапливаться в клетках, инфицированных вирусом, но не в интактных клетках. Его концентрация в инфицированных клетках может в 30-120 раз быть больше, чем в плазме крови. Это важное обстоятельство объясняет большую широту терапевтического действия данного препарата по сравнению с другими и меньшую опасность осложнений. Связывание с белками плазмы крови всего 9-30%, поэтому препарат хорошо проникает в различные ткани и жидкости (включая ликвор). Большая часть препарата (80-90%) в неизмененном виде и в виде метаболита 9-карбоксиметоксиметилгуанина выводится почками. Период полувыведения примерно 3,3 ч, однако при почечной недостаточности он может увеличиваться до 20 ч, поэтому необходимо корректировать дозирование. Так, при скорости клубочковой фильтрации (СКФ) менее 70 мл/мин — дозу препарата снижают в 2 раза; при СКФ менее 50 мл/мин – дозу уменьшают еще на треть; при СКФ менее 25 мл/мин еще на ‘/2 и при СКФ менее 10 мл/мин – в 3 раза.
Нежелательные эффекты ганцикловира: гематотоксичность (нейтро-, лейко-, тромбоцитопения); энцефалопатические реакции; иммунодепрессия; повреждение репродуктивной функции у мужчин и женщин; мутагенное, тератогенное и канцерогенное действие.
Фоскарнет (фосфоноформат) вводят внутривенно. Период его полувыведения от 2 до 4 ч. Экскретируется в неизмененном виде почками. Фоскарнет может вызывать костномозговую депрессию, иммунодепрессию, нарушения функции печени и почек; он обладает тератогенным, мутагенным и канцерогенным свойством.
При использовании ганцикловира и фоскарнета необходимо каждые 2 дня анализ крови. При выраженной нейтропении (меньше 500/мкл) и тромбоцитопении (менее 25 000/мкл) препараты срочно отменяют.
Ганцикловир и фоскарнет являются цитостатиками, поэтому при лечении ЦМВИ их иногда комбинируют с иммуностимуляторами или с интерфероногенами (например, с циклофероном и др.), а также со стимуляторами кроветворения (например, с филграстимом и др.) и с иммуноглобулинами (цитотект).
Цитотект – иммуноглобулин с повышенным содержанием специфических антител к цитомегаловирусу. Его применяют как средство заместительной терапии.
Индивидуальная непереносимость препарата проявляется головной болью, тошнотой, головокружением, рвотой, диареей, тахикардией, цианозом, одышкой, гипертермией, ознобом, повышенным потоотделением, болью в спине, миалгией. Перечисленные симптомы могут появиться уже через 30 мин после начала инфузии и наблюдаться в течение первых суток. Тяжелая анафилактическая реакция может наблюдаться у больных с отсутствием или выраженным дефицитом IgA, что примерно в 30% случаев связано с наличием у них антител против названного иммуноглобулина. Когда такие больные получают иммуноглобулиновый препарат, у них образуются макромолекулярный комплекс IgA – анти-IgA, приводящий к анафилаксии. Целесообразно у всех больных определять IgA в сыворотке крови перед введением цитотекта.
Профилактика Цитомегаловирусной инфекции у детей:
К методам профилактики принадлежат неспецифические: соблюдение личной гигиены, к специфическим относятся медикаментозный метод препаратами – ганцикловир, ацикловир, фоскарнет.
Чтобы исключить возможность инфицирования цитомегаловирусом пациентов при пересадке органов и тканей необходимо проводить тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Особую опасность цитомегаловирусная инфекция представляет для беременных женщин, так как может спровоцировать выкидыш, мертворождение или вызвать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с токсоплазмозом, герпесом и краснухой принадлежит к числу инфекций, обследоваться на которые женщины должны еще на этапе планирования беременности.
