цилиндроклеточная метаплазия пищевода это что
Абляция очагов при пищеводе Барретта
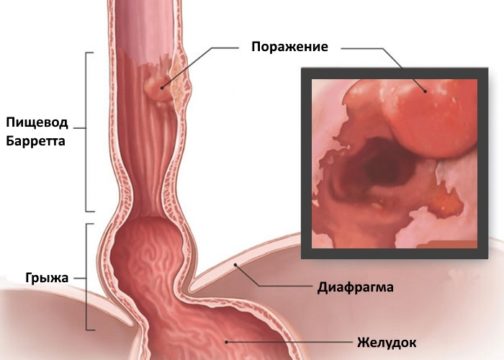
Пищевод Барретта – это патологическое состояние, при котором плоский эпителий нижней трети пищевода замещен метапластическим цилиндрическим эпителием. Пищевод Барретта является серьезным осложнением гастроэзофагеальной рефлюксной болезни (ГЭРБ), официально доказанным предраковым состоянием, которое может приводить к развитию злокачественной опухоли пищевода.
Диагностировать данное заболевание можно при эндоскопическом исследовании с проведением биопсии.
Специалисты отделения эндоскопии НИИ онкологии им. Н.Н.Петрова придерживаются позиции, согласно которой для постановки диагноза «пищевод Барретта» необходимо обнаружение кишечной метаплазии в биоптатах, т.к. только неполная кишечная метаплазия в дистальном отделе пищевода предрасполагает к развитию дисплазии и повышает риск возникновения рака пищевода в 30-125 раз.
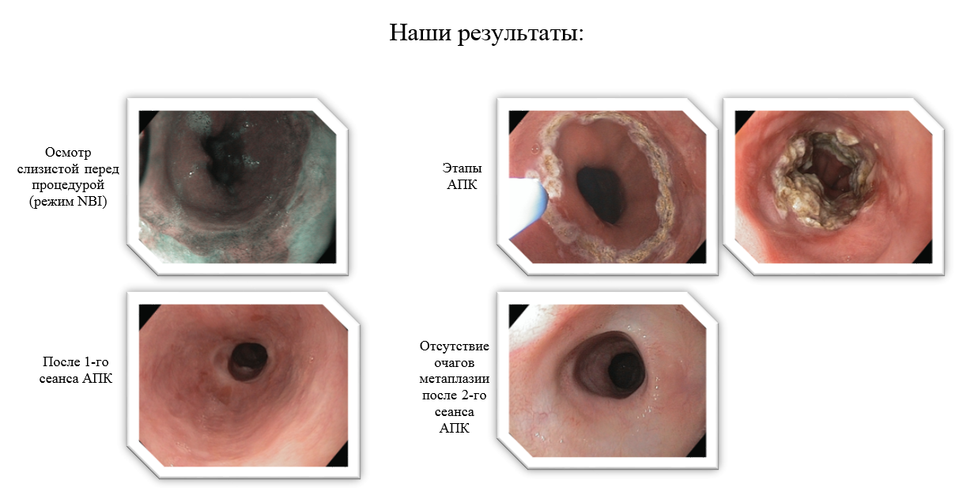
При обнаружении очагов метаплазии перед врачами-эндоскопистами ставится важная диагностическая задача – выполнить тщательный прицельный осмотр слизистой для выявления участков с нерегулярным рельефом и сосудистым рисунком, которые свидетельствуют о возникновении дисплазии различной степени тяжести или аденокарциномы. Такой подход позволяет произвести забор биоптатов прицельно, а не случайным образом, что повышает диагностическую ценность и снижает вероятность ошибки в обнаружении рака.
Для решения этих задач требуется оснащение эндоскопического отделения современным оборудованием и применение современных уточняющих методик осмотра слизистой оболочки.
Лечение пациентов с пищеводом Барретта
Принятая в НИИ онкологии им. Н.Н.Петрова тактика лечения и последующего динамического наблюдения пациентов с цилиндроклеточной метаплазией основана на рекомендациях Британского общества гастроэнтерологов по диагностике и лечению пищевода Барретта (2014 г) и Американской Гастроэнтерологической Ассоциации.
Все пациенты с метаплазией в нижней трети пищевода получают курс комплексной антирефлюксной терапии длительностью 4-8 недель, включающий в себя:
Тактика лечения зависит прежде всего от результатов гистологического исследования материала, взятого из участков метаплазии, а также от протяженности сегмента метаплазии:
Аргоноплазменная абляция очагов метаплазии
Аргоноплазменная абляция может осуществляться 2-мя способами:

Эндоскопическое лечение сопровождается антисекреторной терапией с помощью ингибиторов протоновой помпы для эффективного и быстрого заживления дефектов слизистой оболочки и создания условий для появления в этих зонах многослойного плоского эпителия пищевода.
Подготовка к процедуре
Процедура аргоноплазменной абляции очагов метаплазии проводится строго натощак, полностью исключается прием пищи за 12 часов и жидкости за 6 часов до начала процедуры
Необходима отмена пероральных антикоагулянтов (препаратов для разжижения крови) накануне исследования, пауза п/к введения гепарина за 4-6 часов до процедуры
Процедура абляции может быть выполнена под внутривенной анестезией. Если исследование будет проводиться под наркозом, прием любого количества жидкости до процедуры строго воспрещен. Управление транспортным средством после окончания исследования является нежелательным и может представлять угрозу для жизни и здоровья.
Пищевод Барретта: симптомы, прогноз, лечение
Пищевод Барретта (ПБ, синдром Барретта) — это изменение слизистой нижнего отдела пищевода по цилиндрическому типу любой длины, так называемая метаплазия. Эти изменения могут быть распознаны при эндоскопическом исследовании, после взятия биопсии из измененных участков и гистологического подтверждения.
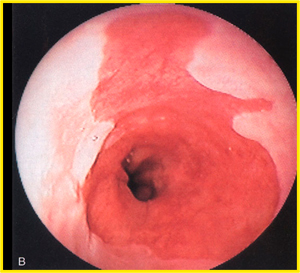 | 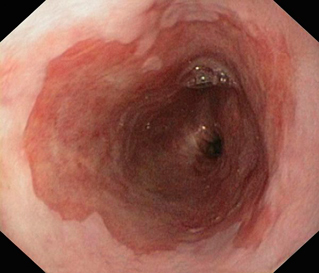 |
Причины и симптомы заболевания
Пищевод Барретта — это заболевание которое возникает в течении жизни, зачастую по причине следующих факторов:
Наиболее частые формы патологических изменений слизистой оболочки пищевода, которые могут привести к ПБ:
Основные жалобы пациентов и признаки пищевода Барретта
Не следует игнорировать перечисленные симптомы и откладывать поход к врачу, лучше профилактировать заболевание и начать лечение на ранних этапах, ведь процессы, происходящие на клеточном уровне не обратимы.
Диагностика пищевода Барретта
Основной и наиболее эффективный метод диагностики синдрома Барретта — эндоскопический. Его цель — получение биопсийного материала. При этом морфологическое исследование направлено на:
Для определения более точных границ измененной слизистой во время эндоскопического исследования используют хромоскопию, это окраска слизистой. Обычно используют раствор Люголя, при аллергии на йод — метиленовый синий, уксусную кислоту.
Лечение пищевода Барретта
Применяют следующие методы лечения пищевода Барретта:
Еще один применяемый и весьма радикальный метод — удаление нижней части пищевода.
Профилактика
Не существует специфической профилактики синдрома Барретта.
Предупредить его развитие помогает своевременная диагностика и лечение гастроэзофагеальной рефлюксной болезни, регулярные и своевременные посещения гастроэнтеролога, обследования и стойкое динамическое наблюдение.
После эффективного консервативного и хирургического лечения пищевода Барретта всем пациентам необходимо проходить ежегодное эндоскопическое обследование с биопсией эпителия.
Авторская публикация:
ВИНЦКОВСКАЯ АЛЕКСАНДРА ИГОРЕВНА
онколог, эндоскопист
НМИЦ онкологии им Н.Н. Петрова
Можно ли вылечить Пищевод Барретта? (Выпуск 4)
Пищевод Барретта определяется как замещение слизистой пищевода слизистой желудочного типа (цилиндроклеточной метаплазии) с наличием среди нее очагов кишечных клеток (кишечной метаплазии).
Вопрос века
Если развитие цилиндроклеточной метаплазии уже состоялось, можно ли на фоне лечения добиться, чтобы на этом месте образовался нормальный эпителий пищевода? Решению вопроса о том, можно ли вылечить пищевод Барретта было посвящено множество исследований и, к сожалению, на сегодня ни медикаментозное, ни хирургическое лечение обеспечить этого с доказательной достоверностью не могут. В ряде исследований отмечено о появлении даже островков нового эпителия пищевода, но неполное его восстановление. Некоторые авторы сообщали о полной регрессии цилиндроклеточной метаплазии, но только у 2 пациентов из 190 наблюдавшихся.
Можно ли вылечить пищевод Барретта разрушением очагов болезни?
Перспективным и современным методом лечения пищевода Барретта рассматривается в настоящее время различные формы абляции (разрушение очагов пищевода Барретта различными методами). К этим методам прибегают только при прогрессировании пищевода Барретта, т.е. обнаружении на фоне цилиндроклеточной метаплазии, кишечной метаплазии в сочетании с дисплазией.
Также следует отметить, что данные процедуры делаются под контролем зрения человека, не на микроскопическом уровне. Возникает пресловутый «человеческий фактор», когда невозможно точно и повсеместно определить все очаги поражения. Описаны не единичные случаи остаточных микроскопических очагов пищевода Барретта, которые не были разрушены. Поверх этих очагов образовывался новый эпителий пищевода, а под ним из неразрушенных остатков пищевода Барретта продолжал развиваться процесс, который при последующей эндоскопии никак не определялся.
Можно ли вылечить пищевод Барретта изменением мировозрения?
Нужно помнить, что развитие пищевода Барретта – это своеобразный защитный механизм организма от агрессии кислотой и желчью. К этому агрессивному воздействию клетки слизистой пищевода не адаптированы, вот и образуются в этом месте такие клетки (клетки желудка и кишки), которые привычны к кислоте и/или желчи. Поэтому, чтобы вылечить данное состояние, необходимо не только прием лекарственных препаратов для ликвидации уже приобретенных изменений, но и глубоко изменение образа жизни и, если хотите, мировозрения.
Поэтому, отвечая на этот вопрос, сегодня с уверенностью можно сказать: медицине пока это не подвластно. При подозрении и обнаружении пищевода Барретта необходимо проводить пожизненную медикаментозную терапию с оптимальным сочетанием хирургических вмешательств, и при возникновении диспластических процессов в слизистой пищевода Барретт прибегать к из разрушению, т.е абляции.
Цилиндроклеточная метоплазия пищевода
Добрый день. Делал гастроскопию с биописей. Пришел такой результат.
«цилиндроклеточная метоплазия слизистой пещевода». Все документы с иследованием прикрепил к вопросу.
Гастранэнтеролог назначил лечение. Пантопразол 20 мг по 1 таблетки в день в течении 4 недель.
Но я как то поднапрегся от диагноза, меня ничего не беспокоит. Я не пью, не курю. Это часто встречается? Какой прогноз? можно ли полностью избавится? мне 29 лет всего
Хронические болезни: удален жп, невроз (ОКР)
На сервисе СпросиВрача доступна консультация гастроэнтеролога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!
Можете прочитать о клпассификациии метаплазии пищевода вводя в поисковик следующий заголовок :
Пражская классификация метаплазии в пищеводе (2004)
Параскевова А.В., Трухманов А.С., Сторонова О.А., Пономарев А.Б., Ивашкин В.Т. Клинико-морфологические и функциональные показатели ГЭРБ при наличии цилиндроклеточной метаплазии слизистой оболочки пищевода. Вопросы детской диетологии. 2020; 18(2):61–68.
Клинико-морфологические и функциональные показатели гастроэзофагеальной рефлюксной болезни при наличии цилиндроклеточной метаплазии слизистой оболочки пищевода
А.В.Параскевова, А.С.Трухманов, О.А.Сторонова, А.Б.Пономарев, В.Т.Ивашкин
Первый Московский государственный медицинский университет им. И.М.Сеченова (Сеченовский Университет), Москва, Российская Федерация
Цель. Оптимизировать тактику ведения пациентов с гастроэзофагеальной рефлюксной болезнью (ГЭРБ) на основании оценки клинических данных и морфофункциональных методов диагностики для предотвращения развития цилиндроклеточной метаплазии эпителия пищевода.
Пациенты и методы. В исследование было включено 63 пациента с ГЭРБ. После проведения эзофагогастродуоденоскопии с биопсией и морфологическим исследованием слизистой пищевода было выделено 2 группы: пациенты с ГЭРБ, осложненной цилиндроклеточной метаплазией (ЦКМ) (n = 32), и пациенты с ГЭРБ без ЦКМ (n = 31). Пациентам проводилась манометрия пищевода высокого разрешения и 24-часовая рН-импедансометрия.
Результаты. Жалоба на затруднение прохождения пищи по пищеводу у пациентов с ГЭРБ, осложненной ЦКМ, встречалась чаще, чем у пациентов с ГЭРБ без ЦКМ. По данным манометрии, давление покоя нижнего пищеводного сфинктера у пациентов с ГЭРБ, осложненной ЦКМ (17,3 [13,3; 21,4] мм рт. ст.), было ниже, чем у пациентов с ГЭРБ без ЦКМ (22,3 [18,5; 26,1] мм рт. ст.), р = 0,063. Неэффективная моторика пищевода встречалась чаще у пациентов с ГЭРБ, осложненной ЦКМ (41,6%), чем у пациентов с ГЭРБ без ЦКМ (11,1%). Затруднение прохождения пищи по пищеводу сопровождалось неэффективной моторикой пищевода. Количество кислых гастроэзофагеальных рефлюксов (ГЭР) по данным 24-часовой рН-импедансометрии, у пациентов с ГЭРБ, осложненной ЦКМ (39,5 [2,0; 103,0]) было больше, чем у пациентов без ЦКМ (37,0 [0; 79,0]), р = 0,332. При этом количество слабокислых ГЭР у пациентов с ГЭРБ, осложненной ЦКМ (32,0 [4,0; 100,0]) было достоверно меньше, чем у пациентов без ЦКМ (47,0 [12,0; 100,0]), р = 0,010.
Заключение. ГЭРБ – мультифакторное заболевание с первичным нарушением двигательной функции верхних отделов желудочно-кишечного тракта. Характер рефлюката может влиять на тип метаплазии эпителия.
Ключевые слова: ГЭРБ, метаплазия, манометрия пищевода, 24-часовая рН-импедансометрия
Для цитирования: Параскевова А.В., Трухманов А.С., Сторонова О.А., Пономарев А.Б., Ивашкин В.Т. Клинико-морфологические и функциональные показатели гастроэзофагеальной рефлюксной болезни при наличии цилиндроклеточной метаплазии слизистой оболочки пищевода. Вопросы детской диетологии. 2020; 18(2): 61–68. DOI: 10.20953/1727-5784-2020-2-61-68
Clinical, morphological and functional characteristics of gastroesophageal reflux disease with esophageal columnar metaplasia
A.V.Paraskevova, A.S.Trukhmanov, O.A.Storonova, A.B.Ponomarev, V.T.Ivashkin
Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russian Federation
Objective. To optimise the tactics of treatment of patients with gastroesophageal reflux disease (GERD) based on assessment of clinical data and morphofunctional diagnostic methods in order to prevent the development of esophageal columnar metaplasia.
Patients and methods. The study included 63 patients with GERD. After esophagogastroduodenoscopy with biopsy and morphological examination of the esophageal mucosa 2 groups were singled out: patients with GERD complicated by columnar metaplasia (ECM) (n = 32), and patients with GERD without ECM (n = 31). Patients underwent high-resolution esophageal manometry and 24-hour рН-impedance monitoring.
Results. Complaints of difficult passage of food through the esophagus in patients with GERD complicated by ECM were more common than in patients with GERD without ECM. According to the findings of manometry, lower esophageal sphincter resting pressure in patients with GERD complicated by ECM (17.3 [13.3; 21.4] mmHg) was lower than in patients with GERD without ECM (22.3 [18.5; 26.1] mmHg), р = 0.063. Ineffective esophageal motility was more common in patients with GERD complicated by ECM (41.6%) than in patients with GERD without ECM (11.1%). Difficult passage of food through the esophagus was accompanied by ineffective esophageal motility. The number of acid gastroesophageal refluxes (GER) according to 24-hour рН-impedance monitoring in patients with GERD complicated by ECM (39.5 [2.0; 103.0]) was greater than in patients without ECM (37.0 [0; 79.0]), р = 0.332. The number of weak acid GER in patients with GERD complicated by ECM (32.0 [4.0; 100.0]) was significantly less than in patients without ECM (47.0 [12.0; 100.0]), р = 0.010.
Conclusion. GERD is a multifactor disease with primary impairment of the motor function of the upper gastrointestinal tract. The character of the refluxate might influence the type of epithelial metaplasia.
Key words: GERD, metaplasia, esophageal manometry, 24-hour pH-impedance monitoring
For citation: Paraskevova A.V., Trukhmanov A.S., Storonova O.A., Ponomarev A.B., Ivashkin V.T. Clinical, morphological and functional characteristics of gastroesophageal reflux disease with esophageal columnar metaplasia. Vopr. det. dietol. (Pediatric Nutrition). 2020; 18(2): 61–68. (In Russian). DOI: 10.20953/1727-5784-2020-2-61-68
Цилиндроклеточная метаплазия (ЦКМ) слизистой оболочки пищевода является приобретенным состоянием вследствие длительного воздействия патологического гастроэзофагеального рефлюктата на плоский эпителий.
Гистологически нормальный пищевод представлен многослойным плоским неороговевающим эпителием. В норме после завершения эмбрионального развития цилиндроклеточный эпителий в пищеводе не встречается [1].
Специализированный цилиндрический эпителий в пищеводе развивается из стволовых клеток. Эпителиальные стволовые клетки-предшественники располагаются в выводных протоках кардиальных желез пищевода. Их дифференцировка меняется вследствие хронического воспаления. На начальном этапе развитие ЦКМ в пищеводе является адаптивной реакцией слизистой пищевода, направленной на защиту от непрерывного повреждающего действия патологического гастроэзофагеального рефлюктата 2. Патологический рефлюктат действует на базальный слой эпителия пищевода и ведет к пролиферации стволовых клеток-предшественников, смене генетического сигнала и развитию цилиндроклеточной трансформации эпителия пищевода. На первом этапе развивается кардиальная метаплазия слизистой пищевода. Кардиальная метаплазия пищевода является промежуточным состоянием между плоским эпителием пищевода и фундальным типом метаплазии [5]. Переход кардиального эпителия в желудочный тип метаплазии характеризуется появлением париетальных клеток.
Дальнейшее развитие из желудочной метаплазии специализированного кишечного эпителия может быть обусловлено характером патологического рефлюктата. Патологический рефлюктат, кроме соляной кислоты и пепсина, может содержать желчные кислоты. Таким образом, метаплазированные участки эпителия пищевода подвергаются комплексному воздействию желудочного и дуоденального содержимого [6, 7].
В связи с возможным влиянием характера рефлюктата на тип ЦКМ пациентам с гастроэзофагеальной рефлюксной болезнью (ГЭРБ), осложненной ЦКМ, необходимо проведение 24-часовой рН-импедансометрии. Ранее проведенные исследования показали, что, по данным 24-часовой рН-импедансометрии, у пациентов с кишечным типом метаплазии эпителия пищевода отмечалось преобладание количества гастроэзофагеальных рефлюксов (ГЭР) и удлинение времени экспозиции болюса. В этих же исследованиях обращало на себя внимание более частое нарушение моторики пищевода и наличие грыжи пищеводного отверстия диафрагмы у пациентов с ГЭРБ, осложненной ЦКМ, по сравнению с пациентами с ГЭРБ без ЦКМ [8, 9].
Вне зависимости от гистологического типа ЦКМ пищевода является риском развития аденокарциномы пищевода (АКП) у мужчин в 0,28% случаев, у женщин – в 0,13% [10]. Рак пищевода занимает 7-е место в мире среди онкологических заболеваний у мужчин и 13-е – у женщин [11]. Вероятность возникновения АКП у пациентов с кишечной метаплазией составляет 0,5–2,1% в год [12]. В связи с риском развития АКП на фоне ЦКМ изучение ГЭРБ, осложненной цилиндроклеточной метаплазией, остается актуальным и в настоящее время.
Цель исследования – оптимизировать тактику ведения пациентов с ГЭРБ на основании оценки клинических данных и морфофункциональных методов диагностики для предотвращения развития цилиндроклеточной метаплазии эпителия пищевода.
Пациенты и методы
В исследование, проведенное на базе клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х.Василенко Первого МГМУ им. И.М.Сеченова Минздрава России (Сеченовский Университет), было включено 63 пациента, страдающих ГЭРБ. Исследование было одобрено локальным комитетом по этике Сеченовского Университета, выписка из протокола № 05-15 от 20.05.2015.
Критериями включения в исследование были: возраст от 18 до 65 лет, информированное согласие, отсутствие приема ингибиторов протонной помпы или блокаторов Н2-гистаминовых рецепторов в анамнезе как минимум за 1 неделю до включения в исследование. У всех пациентов, включенных в исследование, либо по клинической симптоматике, либо по данным эзофагогастродуоденоскопии (ЭГДС) были выявлены признаки рефлюкс-эзофагита.
Основными жалобами пациентов, включенных в исследование, были изжога, «горечь» во рту. Анализ жалоб пациентов, включенных в исследование, проводился с помощью опросника FSSG (Frequency Scale for the Symptoms of GERD) – Шкалы для оценки частоты cимптомов ГЭРБ. Для подтверждения диагноза всем пациентам проводилась ЭГДС с биопсией пищевода для оценки состояния слизистой оболочки пищевода, выявления ЦКМ и верификации формы ГЭРБ (неэрозивный рефлюкс-эзофагит, эрозивный эзофагит, пищевод Барретта).
Учитывая то, что не все взятые биоптаты содержали метаплазированный эпителий, анализ морфологических изменений плоского эпителия пищевода осуществлялся по классификации Esohisto project. Оценивались маркеры повреждения эпителия пищевода: степень выраженности гиперплазии базального слоя, толщина сосочкового слоя эпителия слизистой, степень расширения межклеточных пространств, появление в эпителиальном пласте сегментоядерных лейкоцитов (наиболее часто это эозинофилы, нейтрофилы), мононуклеарных клеток.
При микроскопическом исследовании биоптатов пищевода, содержащих очаги ЦКМ, проводился анализ характера выстилающих эпителиоцитов, типов желез, признаков пролиферации и дисплазии эпителия слизистой пищевода. По результатам проведенного анализа нами было выделено 3 типа ЦКМ: фундальный, кардиальный, кишечный.
For correspondence: Anna V. Paraskevova, doctor, department of functional diagnostics, V.Kh.Vasilenko Clinic of Internal Diseases Propaedeutics, Gastroenterology and Hepatology, I.V.Sechenov First Moscow State Medical University (Sechenov University). Address: 1/1 Pogodinskaya str., Moscow, 119991, Russian Federation. Phone: (499) 248-6991. E-mail: paraskevova.anna@ mail.ru. ORCID ID: h ttps://orcid.org/0000-0002-1662-2352
© Издательство «Династия», 2020. Тел./факс: +7 (495) 660-6004, e-mail: red@ phdynasty.ru, ww w.phdynasty.ru
Информация о соавторах:
Трухманов Александр Сергеевич, доктор медицинских наук, профессор кафедры пропедевтики внутренних болезней, гаcтроэнтерологии и гепатологии Первого Московского государственного медицинского университета им. И.М.Сеченова (Сеченовский университет). Адрес: 119991, Москва, ул. Погодинская, 1, стр. 1. Телефон: (499) 248-3600. E-mail: troukh@ mail.ru. ORCID: ht tps://orcid.org/0000-0003-3362-2968.
Сторонова Ольга Андреевна, кандидат медицинских наук, врач отделения функциональной диагностики Клиники пропедевтики внутренних болезней, гаcтроэнтерологии и гепатологии им. В.Х.Василенко Первого Московского государственного медицинского университета им. И.М.Сеченова (Сеченовский университет) Адрес: 119991, Москва, ул. Погодинская, 1, стр. 1. Телефон: (499) 248-6991. E-mail: storonova@ yandex.ru. ORCID: ht tps://orcid.org/0000-0002-0960-1166.
Пономарев Андрей Борисович, доцент, врач-патологоанатом кафедры патологической анатомии им. академика А.И.Струкова Первого Московского государственного медицинского университета им. И.М.Сеченова (Сеченовский университет). Адрес: 119991, Москва, ул. Трубецкая, 8, стр. 2. Телефон: (499) 248-3555. E-mail: enpab19@ gmail.com
Ивашкин Владимир Трофимович, академик РАН, доктор медицинских наук, профессор, заведующий кафедрой пропедевтики внутренних болезней гаcтроэнтерологии и гепатологии Первого Московского государственного медицинского университета им. И.М.Сеченова (Сеченовский университет) Адрес: 119991, Москва, ул. Погодинская, 1, стр. 1. Телефон: (499) 248-3591. E-mail: v.t.ivashkin@ mail.ru. ORCID: ht tps://orcid.org/0000-0002-6815-6015
Information about co-authors:
Alexander S. Trukhmanov, MD, PhD, DSc, professor at the department of department of introduction to internal medicine, gastroenterology and hepatology, Sechenov First Moscow State Medical University (Sechenov University). Address: 1/1 Pogodinskaya str., Moscow, 199991, Russian Federation. Phone: (499) 248-3600. E-mail: troukh@ mail.ru. ORCID: ht tps://orcid.org/0000-0003-3362-2968
Olga A. Storonova, MD, PhD, doctor, department of functional diagnostics, V.Kh.Vasilenko Clinic of Propaedeutics of Internal Diseases, Gastroenterology and Hepatology, I.M.Sechenov First Moscow State Medical University (Sechenov University). Address: 1/1 Pogodinskaya str., Moscow, 199991, Russian Federation. Phone: (499) 248-6991. E-mail: storonova@ yandex.ru. ORCID ID: ht tps://orcid.org/0000-0002-0960-1166
Andrey B. Ponomarev, MD, associate professor, anatomical pathologist at the A.I.Strukov department of anatomical pathology, I.M.Sechenov First Moscow State Medical University (Sechenov University). Address: 8/2 Trubetskaya str., Moscow, 119991, Russian Federation. Phone: (499) 248-3555. E-mail: enpab19@ gmail.com
Vladimir T. Ivashkin, MD, PhD, DSc, RAS Academician, professor, head of department, department of propaedeutics of internal diseases, gastroenterology and hepatology, I.M.Sechenov First Moscow State Medical University (Sechenov University). Address: 1/1 Pogodinskaya str., Moscow, 119991, Russian Federation. Phone: (499) 248-3591. E-mail: v.t.ivashkin@ mail.ru. ORCID ID: h ttps://orcid.org/0000-0002-6815-6015
Информация о финансировании. Финансирование данной работы не проводилось.
Financial support. No financial support has been provided for this work.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. The authors declare that there is no conflict of interest.