цефепим или цефтриаксон что лучше при пневмонии ковид
При коронавирусе развивается не пневмония, а пневмонит: Пульмонолог из Коммунарки рассказал, чем лечить, а что бесполезно
Практикующий пульмонолог Олег Абакумов, работающий в Многопрофильном медицинском центре в посёлке Коммунарка Московской области, провёл в «красной зоне», то есть с больными коронавирусом, 8 месяцев. Молодой доктор переехал в столицу не так давно из Воронежа, но опыт по лечению «ковида» уже приобрёл приличный. Так что на своей странице в Интаграме (dr.abakumoff) он активно ведёт целый блог, отвечая на все вопросы.
Не коронавирус страшен, а иммунитет
О вреде противомалярийных лекарств
В схеме лечения коронавируса от Минздрава РФ на первом месте стоит, в том числе, и препарат «Гидроксихлорохин» (ранее был «Плаквенил», что по сути одно и то же). Препарат обладает противомалярийными свойствами, и также оказывает противовоспалительное и иммунодепрессивное действие при некоторых заболеваниях. Однако Абакумов уверяет, что лекарство это не только бесполезно, но и вредно.
О.А.: «Арбидол — вообще не используйте, просто потому что. Мы его не используем, он не работает. Вообще, всё лечение коронавирусной инфекции в том, что, с одной стороны, мы профилактируем тромбоз, с другой — мы должны подавлять ваш же иммунитет. Ваш иммунитет — это очень серьёзная, разрушительная штука. Пить что-то для иммунитета я бы не советовал лишний раз. Ни один противовирусный препарат сейчас не доказан. Более того, что не доказан, я вам скажу, что все старые препараты не работают. Не может ни один препарат попасть в ковид. Не было раньше такого штамма ковида SARS-CoV-2. Единственно, что может сработать в первые часы или в первые пару дней, то это Интерферон. Да, это не доказано, но интерфероны, но в большой дозировке от 5 мл, могут сработать. Чем раньше примете, тем лучше. Когда всё уже плохо, смысла нет. Но может он сыграть и злую шутку: на фоне цитокинового шторма может его увеличить».
Модный и дорогой Фавипиравир не работает
На первом месте в схеме лечения от Минздрва РФ стоит дорогостоящий препарат (порядка 12 тысяч рублей) «Фавипиравир». Его рекомендовано назначать и для лёгкой, и для среднетяжёлой, и для тяжёлой формы коронавируса. В общем, при любом случае. Но в необходимости такого лечения Абакумов сомневается.
О.А.: «Все вдруг начали переживать, что вышел новые препарат, хотя он не новый, а с 2006 года, «Фавипиравир» называется. Он японский препарат, с 2006 года его начали разрабатывать в Японии против гриппа. Смысл такой, что он не особо против гриппа-то работает, ну а против коронавируса… ну, как-то шатко-валко мы его используем, но я не могу сказать, что он крутой и стоит этих 12 тысяч. Еще там куча побочек. Еще тератогенным эффектом обладает и на печень влияет, поэтому я бы не советовал. А продают его за такие бабосы, знаете почему? Потому что купили лицензию на производство и надо же бабки отбить».
Лёгочникам болезнь не так страшна, как диабетикам
Люди, у которых есть бронхолёгочная патология, по словам Абакумова, находятся лишь на третьем месте в группе риска.
О.А.: «Людям с бронхолёгочной патологией особо бояться не стоит, потому что ковид — это не поражение лёгких. Это отек альвиол, повреждение свертывающей системы крови, но это не поражение легких. А бояться стоит диабетикам, первое место у диабетиков. Они болеют более тяжело, а второе место — это люди с сердечной недостаточностью — это ишемическая болезнь сердца, это гипертоническая болезнь. Это те люди, у которых есть поражение сосудов. Ковид — это про сосуды. Это когда капилляры забиваются тромбами. Это цитокиново-брадикининовый шторм».
Про лечение
О.А.: «Это фраксипарины, антикоагулянт «Клексан». Потому что гепарин, с одной стороны, профилактирует тромбозы, а с другой — обволакивает вирус. И вирус уже не такой агрессивный. А ещё я рекомендую сдавать D-димер: он показывает риск возникновения тромбозов».
Как узнать, разбушевался иммунитет или нет?
О.А.: «Лихорадка очень высокая. Если у вас повышение температуры тела уже в течение нескольких дней, то, скорее всего, вы идёте к цитокиновому шторму. А если к этому присоединяется десатурация — снижение сатурации, плюс отдышка, вы начинаете задыхаться. Плюс у вас нарастает негативная симптоматика по КТ, плюс у вас нарастает С-реактивный белок — это фактор воспаления. Просто к бабке не ходи, на КТ не ходи, сдай С-реактивный белок и ты увидишь, есть ли у тебя поражение лёгких от коронавируса. Короче, если всё это есть, — это цитокиновый шторм. Он не сбивается ни парацетамолом, ничем, кроме двух вещей — гормоны — дексаметазон, преднизолон в больших дозировках и пульсотерапия. И второе — это блокаторы интерлейкина 6, это имунносупрессоры, которые используют в ревматологии. Это препараты типа «Барицитиниб» («Олумиант»), если всё плохо — «Тоцилизумаб»».
Пульмонолог уточняет: сначала идут гормоны, их можно использовать и амбулаторно дома. Принимать их следует осторожно людям с сахарным диабетом, также гормоны увеличивают рост лейкоцитов. Поэтому если много лейкоцитов в крови на фоне приёма гормонов — это не повод для приёма антибиотиков. А после перенесенного заболевания лечащий врач может порекомендовать продолжить гормональное лечение и дома.
Про пользу АЦЦ и витамин Д
О.А.: «Это муколитик, он разжижает мокроту, но еще снижает оксидативный стресс в организме. Поэтому тоже следует принимать. Тоже дополнительно назначаем АЦЦ, но в больших дозировках. Витамин Д не обладает противовирусной активностью, но он общеукрепляющий. Масляный в дозировке 4000 МЕ минимум, следует принимать во время еды».
Как восстановить обоняние и вкус
Как известно, при коронавирусе у многих пропадает обоняние и вкус: люди не чувствуют ни запахов, ни вкуса пищи. Некоторые уверяют, что после перенесенного «ковида» этот симптом не исчезает. Что в этом случае делать?
О.А.: «Это нарушение нейронов, то есть это не поражение головного мозга. Поражение нейронов: разрыв цепочки между носом и башкой. Те, кто принимал гормоны у меня, у них быстрее восстанавливался запах, чем у тех, кто не принимал. За полгода я это заметил, поэтому я рекомендую тем, у кого нарушено обоняние, есть местные гормональные спреи мометазонсодержащие. Можно их использовать. Второе: очень классно себя показывают витамины группы В, поэтому Мильгамма, пожалуйста, тоже можно пропить».
По наблюдением доктора, обоняние у переболевших очень долго не восстанавливается, и неизвестно, восстановится ли со временем.
Вакцина ничего глобально не изменит
О.А.: «Вакцина она ничего такого не решит глобального. Ну, во-первых, сразу всех не привьют. Чтобы она что-то решила, это должно быть 70% привитых людей. Тогда это что-то решит. Но сразу мы всех так глобально не привьем. Второе: открою вам маленькую тайну — вот если даже вы заболели, даже если у вас появились антитела, даже если вы завакцинировались и у вас появились антитела — не факт, что вы не заболеете второй раз, хотя вы заболеете более легко. И смысл такой, что вы, даже имея антитела, даже завакцинировавшись, вы всё равно можете оставаться переносчиком. Поэтому пока не будет 70% заболевших или привитых, никакого популяционного иммунитета не будет».
Тесты ПЦР врут
О.А.: «Тест ПЦР может показать положительный результат и уже переболевшего человека через месяц, например. Потому что у переболевшего в рото- и носоглотке могут быть обломки вируса. И эти обломки, остатки, так скажем. И тест ПЦР может на это дело среагировать. И это не круто: повторная изоляция, вы считаетесь заболевшим. Но на самом деле не факт, что вы болеете повторно. Тесты ПЦР могут быть как ложноотрицательными, так и ложноположительными».
Антисептики на «ковид» уже не действуют
О.А.: «Самая злая шутка была с антисептиками. Все начали заливать друг друга антисептиками. Каждые 3 секундочки нужно обработать руки обязательно. Все начали использовать антисептики, и вирус начал к ним привыкать. Понимаете? Уже достаточно большое количество антисептиков, которые вообще не действуют на коронавирус. Это как водичкой вы его побрызгали. Мойте лучше руки с мылом, лишний раз пользоваться антисептиком я не рекомендую».
Лечение пневмонии при коронавирусной инфекции
Коронавирусная инфекция стала самой обсуждаемой темой последнего времени. Это респираторное заболевание, а особенно его угрожающие последствия, стали основной страшилкой современности, хотя в 80% случаев оно протекает легко и относительно без последствий. Только у 20% заболевших «корона» протекает в тяжелой форме. Как известно, вызывающий ее вирус может провоцировать возникновение пневмонии, т. е. воспаления легких, в 2—5% случаев приводящей к тяжелым осложнениям, уносящим жизни.
Особенности пневмонии при коронавирусе
Для коронавирусной инфекции типично развитие вирусной атипичной пневмонии, которая может развиваться как практически сразу же после заражения, так и уже после возникновения основных симптомов заболевания. При ней в легких и бронхах, а точнее в их мельчайших составляющих, альвеолах и бронхиолах, возникает острый воспалительный процесс, но часто это сопровождается смазанной клинической картиной, что и отличает атипичную пневмонию.
Развитие пневмонии опасно не только при коронавирусе, но и в целом. Ведь, несмотря на весь прогресс медицины, она остается опасным заболеванием, входящим в первую десятку болезней, приводящих к смерти больных даже в самых развитых странах.
Пневмония после коронавируса может быть первичной и вторичной. В первом случае она вызывается самим вирусом SARS-CoV-2 и, как правило, протекает атипично. Во втором случае она носит вирусно-бактериальную природу и может сочетаться с первичным воспалением легких или же выступать его поздним осложнением, то есть такая пневмония развивается уже после перенесения коронавирусной инфекции. Замечено, что бактериальная флора чаще всего присоединяется к вирусу на 4—7 день и может выступить главной причиной воспаления легких.
Вызывать пневмонию после коронавируса могут и другие виды вирусов, в том числе гриппа, парагриппа, кори, аденовирус и пр., если после выздоровления от «короны» человек столкнулся с этими инфекциями.
При попадании вируса из носовой или ротовой полости в бронхи возникает отек слизистых оболочек, изменяется рН, что нарушает движение ресничек, ответственных за естественное очищение нижних дыхательных путей. Постепенно бронхи отекают все больше, а их просветы перекрываются слизью, что серьезно затрудняет прохождение воздуха. В результате сильно страдает газообмен легких, в кровь поступает меньше кислорода, что приводит к возникновению гипоксии. Это отрицательно сказывается на работе всего организма, в том числе головного мозга, а не только легких. Кроме того, при поражении легких SARS-CoV-2 наблюдается нарушение синтеза сурфактанта – особого вещества, призванного обеспечивать правильную работу альвеол и защищает их от образования рубцовой ткани, т. е. развития фиброза. В результате развивается вирусная пневмония.
Вирусные частицы проникают в клетки альвеол, там размножаются и впоследствии высвобождаются в легкие, а клетка погибает. Таким образом, одновременно поражается большое количество альвеол, нарушается их целостность и повышается проницаемость стенок. Это приводит к тому, что в них нарушаются обменные процессы, жидкость проникает в межклеточное пространство, что приводит к нарушению водно-солевого обмена. Поскольку в пораженных альвеолах скапливаются разрушенные элементы клеток, лейкоциты, эритроциты, это приводит к отеку легких. При разрушении поврежденных клеток стенки альвеол спадаются, что провоцирует развитие нарушений дыхания, тяжесть которых зависит от объема поражения легких.
Как правило, начало развития коронавирусной инфекции плавное. Изначально поднимается температура до субфебрильных значений, т. е. до 37,5°С, и возникает слабость. Это может сопровождаться незначительным першением в горле, покраснением, слезоточивостью глаз. Обусловленная вирусом SARS-CoV-2 пневмония обычно развивается на 8—9 день от начала заболевания. Во многих случаях это протекает бессимптомно, в чем и заключается основное коварство воспаления легких такого типа. Иногда пневмония возникает уже на 5—6 день от начала заболевания. У ряда больных это сопровождается нарушениями работы ЖКТ, в том числе тошнотой, диареей, реже рвотой, а иногда и появлением сыпи на коже. По собранным данным, подобное протекание заболевания характерно для перенесения «короны» в менее тяжелой форме.
На более поздних этапах развития пневмонии возникает надсадный сухой кашель, боль в груди и одышка. Появление подобных признаков является поводом для немедленного обращения за медицинской помощью, поскольку характерное для коронавируса воспаление легких может приводить к тяжелым последствиям, в том числе необратимому фиброзу, что существенно снизит качество жизни, станет причиной инвалидности или даже смерти больного.
При прогрессировании воспалительного процесса в легких наблюдается возникновение острого дистресс-синдрома, что сопровождается:
При тяжелой одышке больные стараются принять вынужденное положение тела: сидя, уперев руки перед собой в стул, кровать или колени.
Если в это время сделать КТ легких, на полученных снимках будут видны обусловленные вирусным поражением двусторонние изменения в легких в виде затемнений округлой формы, склонных сливаться между собой и формировать так называемый рентгенологический признак «эффект матового стекла». После разрешения воспалительного процесса, отмершие участки легких заменяются фиброзными рубцами. Рентген не дает такой исчерпывающей информации, как КТ, и в легких ситуациях при незначительном объеме поражений легких может вовсе оказаться бесполезным, так как изменения не будут видны.
Также обусловленная коронавирусом пневмония сопровождается поражением стенок сосудов легких с нарушением свертываемости крови. Это приводит к образованию тромбов и резкому увеличению риска развития тромбоэмболии.
Но если заболевание осложняется присоединением бактериальной флоры, т. е. развитием вторичной вирусно-бактериальной пневмонии, клиническая картина становится значительно ярче уже с первых дней. В таких ситуациях больным будет досаждать сначала приступообразный сухой кашель, постепенно сменяющийся влажным с отхождением густой, слизисто-гнойной мокроты.
Выраженная лихорадка – типичный признак бактериальных инфекций. При этом она может сохраняться достаточно долго и плохо поддаваться купированию жаропонижающими средствами. Нередко наблюдаются боли в груди разной интенсивности, усиливающиеся при кашле, чихании, движениях.
В целом вирусная пневмония при адекватном лечении длится от 2-х недель до 4—6 недель.
Пневмония особенно опасна для пожилых людей старше 65—70 лет, а также лиц, имеющих сопутствующие заболевания, в частности:
Диагностика
Диагностика пневмонии после коронавируса в целом осуществляется так же, как и в других случаях, т. е. включает сбор анамнеза, в рамках чего врач выясняет, когда появились первые признаки заболевания, как оно протекало, когда наступило ухудшение и т. д. Обязательно проводится аускультация легких, во время которой можно услышать характерные хрипы, заметить учащение сердцебиения и дыхания. Также обязательно измеряют сатурацию, т. е. определяют уровень насыщения крови кислородом. Эта неинвазивная процедура занимает меньше минуты и осуществляется с помощью пульсоксиметра, надеваемого на палец больного.
Непременно проводится ПЦР тест на SARS-CoV-2, а также рентгенография органов грудной клетки или компьютерная томография. В рамках диагностики пневмонии также обязательно выполняется:
Все эти анализы крайне важны, поскольку позволяют установить причину развития воспаления легких, его возбудителя и чувствительность к различным лекарственным средствам. Это позволяет разработать наиболее эффективную тактику лечения пневмонии.
Лечение пневмонии после COVID-19
Воспаление легких легкой степени тяжести может лечиться дома под строгим контролем терапевта или педиатра. При этом важно обеспечить максимальную изоляцию больного от остальных членов семьи. Если это возможно, и больной способен сам себя обслуживать, стоит на время переехать в другое жилье для полной самоизоляции. При отсутствии такой возможности больному следует постараться выделить отдельное помещение, посуду, полотенце и т. д. Также обязательно нужно регулярно проветривать комнату и проводить влажную уборку во избежание заражения других членов семьи.
Больному, проходящему лечение пневмонии при коронавирусе в домашних условиях, необходимо обеспечить обильное питье, причем желательно отдавать предпочтение теплым напиткам, например, компоту, воде, морсу. Но от кофеинсодержащих напитков, в частности кофе, чая, энергетиков, лучше отказаться, так как они оказывают стимулирующее действие на нервную систему, повышая активность и «отвлекая» организм от борьбы с инфекцией.
Обязательной госпитализации подлежат:
При диагностировании изолированной вирусной пневмонии, т. е. при получении отрицательных результатов анализов на бактериальную микрофлору, пациентам назначаются препараты 4-х групп:
Таким образом, специфического лечения вирусной пневмонии не существует, а все мероприятия направлены на поддержание организма, пока иммунная система ведет борьбу с вирусом и вызванными им изменениями в легких.
При присоединении вторичной бактериальной инфекции обязательно назначаются антибиотики. Но при пневмонии после коронавируса их нередко назначают даже при отсутствии подтверждений наличия бактериальной микрофлоры с целью снижения риска осложнения течения и без того опасного воспаления легких. Поэтому антибиотики часто назначаются всем больным с подтвержденным диагнозом COVID-19 и при пневмонии после него.
В особенно тяжелых случаях в состав медикаментозной терапии включают кортикостероиды, обладающие выраженными противовоспалительными свойствами и помогающие защитить стенки сосудов альвеол от повреждения. Их вводят внутривенно короткими курсами.
При развитии дыхательной недостаточности и низком уровне сатурации пациентов лечат в отделении интенсивной терапии с применением экстракорпоральной мембранной оксигенации, т. е. искусственного введения в легкие кислорода за счет использования зондов и других средств. В особенно сложных случаях больных вводят в искусственную кому и подключают к аппарату искусственной вентиляции легких до стабилизации состояния больного и устранения риска летального исхода.
Противовирусные препараты
Пневмония, обусловленная SARS-CoV-2 – новое явление для современной медицины, которое стало вызовом для нее и поставило задачу подобрать и синтезировать новые эффективные по отношению именно к этому штамму вируса препараты. Так, сегодня для лечения воспаления легких в таких ситуациях применяются лекарственные средства на основе ингибиторов протеаз, в которых действующим веществом выступает лопинавир, ритонавир, авифавир.
Также достаточно хорошо себя зарекомендовали в борьбе с SARS-CoV-2 противомалярийные препараты, в частности хлорохин и дезоксихлорохин. Но они отрицательно сказываются на работе сердечно-сосудистой системы, поэтому решение об их применении, особенно у пациентов с заболеваниями сердца и сосудов, принимается строго индивидуально после тщательного взвешивания рисков и ожидаемой пользы.
В последние годы на фармацевтическом рынке появилась масса противовирусных средств общего назначения: Арбидол, Амиксин, Оциллококцинум и пр. Еще до появления COVID-19 они часто назначались педиатрами и терапевтами при ОРВИ, гриппе и других вирусных инфекциях. Их эффективность была подтверждена в ходе проведения клинических исследований и доказано, что препараты такого рода способствуют повышению естественных защитных сил организма, а также останавливают или как минимум замедляют размножение вируса. Поэтому их также нередко рекомендуют принимать при пневмонии при коронавирусной инфекции или возникшей уже после ее перенесения.
Интерфероны
Интерфероны – естественные биологически активные вещества, вырабатывающиеся в организме человека в ответ на вирусную инвазию. Сегодня их чаще всего получают генно-инженерными методами. Препараты на основе интерферонов нередко назначают с самых первых дней перенесения вирусных инфекций, в том числе спровоцировавших развитие воспаления легких, так как они обладают противовоспалительными и иммуномодулирующими свойствами. Но пока что нет убедительной доказательной базы их эффективности.
Дезинтоксикационная терапия
Поскольку при пневмонии организм испытывает интоксикацию, особенно при тяжелом ее течении, пациентам нередко назначают средства, очищающие его от вредных веществ. В подавляющем большинстве случаев дезинтоксикационная терапия проводится в стационаре, так как предполагает внутривенные инфузии глюкозы, физиологического раствора, полиглюкина, а также введение гепарина для снижения риска развития сосудистых нарушений.
Средства симптоматической терапии
Обязательно при пневмонии после коронавируса назначаются препараты, улучшающие самочувствие больного. Это:
Витамины
При вирусной, как и вирусно-бактериальной пневмонии после коронавируса лечение включает использование витаминов. В первую очередь показан прием витамина D, С, А, а также группы В. Они способствуют ускорению восстановления поврежденных слизистых оболочек легких, синтезу гемоглобина, улучшения кровообращения, укреплению стенок сосудов, нормализации течения обменных процессов.
Антибиотики
При диагностировании вторичной вирусно-бактериальной пневмонии антибиотик подбирается в соответствии с результатами бакпосева. В остальных случаях назначается антибактериальный препарат широко спектра действия.
Таким образом, препаратами выбора могут стать:
На фоне приема антибиотиков, а также после окончания курса назначается прием пре- и пробиотиков. Эти препараты способствуют восстановлению нормальной микрофлоры кишечника, которая также является частью иммунной системы организма.
Прогноз
При пневмонии, обусловленной коронавирусной инфекцией, для большинства категорий населения прогноз благоприятный. В 50—60% случаев она протекает в легкой форме. Осложнения возникают только у 3—10 % больных, а летальный исход наблюдается у 1—4% людей, но в старшей возрастной группе 65+ смертность в разных странах достигает 20%.
При этом оценка динамики состояния пациента при перенесении пневмонии после коронавируса осуществляется на основании имеющейся клинической картины. Рентгенологическим показателям уделяется значительно меньшее внимание, поскольку даже через месяц КТ может показывать те же изменения в легких, что и в разгар болезни. Поэтому контрольную томографию следует проводить не ранее чем через 3—6 месяцев после начала болезни.
Стратегические подходы к выбору цефалоспориновых антибиотиков при инфекциях дыхательных путей
Проблема рациональной антибиотикотерапии остается одной из самых сложных в клинической практике. Если ранее врач в вопросе выбора лекарственного препарата ориентировался на его эффективность, переносимость и безопасность, то сегодня этого оказыва
 |
Проблема рациональной антибиотикотерапии остается одной из самых сложных в клинической практике. Если ранее врач в вопросе выбора лекарственного препарата ориентировался на его эффективность, переносимость и безопасность, то сегодня этого оказывается недостаточно. Фактор удобства приема препарата и, что особенно непривычно для нашего понимания, вопросы цены и стоимости лечения в условиях серьезного ограничения финансирования здравоохранения часто могут оказаться определяющими. На приобретение лекарственных средств лечебные учреждения тратят 15–20% своего бюджета, причем 50–60% этих расходов приходится на долю антибактериальных препаратов, что заставляет пересмотреть существующие и искать новые подходы к их применению.
Путаница, возникающая при использовании различных антибактериальных препаратов, в том числе и цефалоспориновых антибиотиков (ЦА), связана с недопониманием или просто незнанием основных принципов клинической химиотерапии. В связи с этим мы хотели бы остановиться на некоторых ошибках и «заблуждениях» практикующих врачей, возникающих при назначении антибактериальных препаратов, на примере ЦА, а также определить их место в лечении инфекции дыхательных путей.
Часто от практикующих врачей приходится слышать о безусловных преимуществах IV поколения препаратов перед III, III поколения перед II и т. д. Это абсолютно неверно. Такая точка зрения приводит к использованию «резервных» и мощных препаратов при лечении банальной инфекции, способствует развитию резистентности, а значит, лишает возможности применять препараты первых поколений и, наконец, вызывает значительное и неоправданное увеличение стоимости курса лечения.
ЦА занимают одно из важных мест в лечении инфекций верхних и нижних дыхательных путей. Наиболее ответственным этапом в антибактериальной терапии данной категории пациентов является выбор первоначального препарата. От адекватности выбора зависит эффективность и безопасность лечения, а также его комфортность, переносимость, стоимость, эпидемиологическая ситуация.
Анализ имеющихся данных об использовании ЦА в России за 1997–1998 гг. позволяет выявить предпочтения врачами того или иного препарата (группы препаратов) и определенных методов его введения. Как видно из рис. 1, при назначении цефалоспориновых антибиотиков подавляющее большинство врачей выбирают парентеральные препараты.
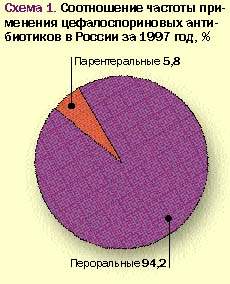 |
Данный факт лишь подтверждает, что в нашей стране пероральные лекарственные средства, и особенно пероральные цефалоспорины, очень мало популярны и практически не используются. Такое отношение к таблетированным формам отражает некоторый консерватизм практических врачей, связанный с тем, что еще 15-20 лет назад существовавшие тогда пероральные средства не выдерживали сравнения с парентеральными препаратами ни по эффективности терапии, ни по ее переносимости. Лишь последние десятилетия с момента создания первого перорального цефалоспорина — цефалексина и появления новых пероральных бактерицидных препаратов эта лекарственная форма несколько укрепила свои позиции не только в амбулаторной, но и в стационарной практике. Однако радикально на положении дел это не сказалось.
Очевидно, что такая форма назначения препаратов имеет безусловные преимущества. Это проявляется и в возможности амбулаторного ведения больного, и в удобстве приема препарата, и в снижении риска постинъекционных осложнений и длительности пребывания в стационаре, и даже в избавлении от психологического дискомфорта, связанного с инъекциями.
Наличие антибактериальных препаратов в двух формах — для парентерального и перорального применения — делает возможным их использование для проведения так называемой ступенчатой терапии. Суть такого лечения состоит в назначении внутривенного или внутримышечного препарата и в последующем, через двое-трое суток после достижения клинического эффекта, переводе на пероральный прием. Возможность проведения ступенчатой терапии одним и тем же препаратом является существенным преимуществом данного лекарственного средства перед его аналогами. Ступенчатая терапия предоставляет клинические и экономические преимущества как пациенту, так и лечебному учреждению.
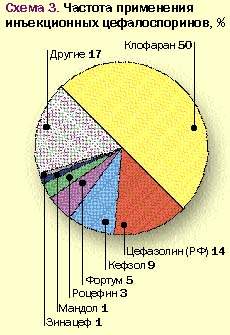
На основании приведенных данных трудно понять логику выбора цефалоспоринового антибиотика того или иного поколения и принципы, которыми руководствуется врач при назначении препарата. Анализ использования цефалоспориновых антибиотиков по поколениям (см. рис. 2 и 3) свидетельствует о предпочтительном назначении препаратов I и III поколений, причем из препаратов III поколения (61%) половина приходится на цефотаксим, а из препаратов I поколения большая часть приходится на цефазолин.
 |
В клинической практике врач начинает проводить антибактериальную терапию, в большинстве случаев не имея результатов микробиологической верификации инфекционного агента, а зачастую и без перспектив получения такого рода данных. Поэтому при выборе антибактериального препарата по-прежнему приходится ориентироваться на сведения, полученные из литературы, данные микробиологического мониторинга, а также на особенности клинической ситуации. Все это позволяет с большей или меньшей долей вероятности определить этиологический инфекционный агент с учетом клинической формы инфекции дыхательных путей (пневмония, хронический бронхит, синусит и т. д.), возраста (дети, старики), сопутствующих заболеваний (сахарный диабет, хроническая алкогольная интоксикация, лечение глюкокортикоидами и цитостатиками). Необходимо также иметь в виду особенности развития инфекции в амбулаторных условиях или в стационаре (лечение по поводу другого заболевания, пребывание в реанимации) при соответствующей эпидемиологической ситуации. Следует отметить, что при выборе препарата важно отличать «госпитальную», или нозокомиальную инфекцию, возникшую спустя двое суток после поступления в стационар, от «амбулаторной» инфекции, долечиваемой в стационаре. В последнем случае тактика антибактериальной терапии должна существенно отличаться.
Таким образом, ориентировочная этиология бронхолегочной инфекции служит основанием для выбора среди ЦА конкретного препарата (или поколения препаратов) с соответствующей антимикробной активностью.
У больных с амбулаторной инфекцией верхних и нижних дыхательных путей, основными возбудителями которых являются стрептококки, Н. influenzae, Moraxella catarrhalis, — препаратами выбора могут быть ЦА I или II поколения. В амбулаторных условиях предпочтение следует отдавать оральным цефалоспоринам (цефаклор, цефуроксим аксетил, цефтибутен). В то же время необходимо иметь в виду недостаточную активность ЦА в целом в отношении атипических бактерий (8–35% в этиологии «домашней» пневмонии) и некоторых анаэробных микроорганизмов, вероятность влияния которых увеличивается у больных с хроническими синуситами и отитами.
При обострениях хронического бронхита особое значение приобретают препараты, высокоустойчивые к действию b-лактамаз, продуцируемых как грамотрицательными, так и грамположительными микроорганизмами (цефуроксим аксетил), и обладающие высокой активностью против Н.influenzae (цефтибутен).
 |
При выявлении показаний для госпитализации больных с «домашней» инфекцией, подразумевающих более тяжелое течение, чаще обнаруживаются Streptococcus pneumonia, Staphylococcus aureus, Н.influenzae и Еntеrobacteriacea. В этом случае более обосновано назначение парентеральных цефалоспоринов II поколения (цефуроксим, цефамандол). Однако именно в таких ситуациях чаще всего и допускаются ошибки: при госпитализации больного в стационар с «домашней» пневмонией нередко назначают бензилпенициллин, аминопенициллины и ЦА I поколения (малоэффективные ввиду высокой резистентности патогенной флоры), либо, для «перестраховки» и при наличии в стационаре, ЦА III поколения (цефотаксим, реже цефтриаксон). Однако более обосновано — и это определяется спектром активности препарата — назначение ЦА II. Среди больных, получающих терапию в стационаре по поводу инфекций нижних дыхательных путей, преобладают нетяжелые случаи. Поэтому идеология назначения ЦА II поколения в качестве «стартовых» препаратов должна доминировать как с позиции адекватной клинической эффективности, экономической целесообразности, так и с позиции сохранения резерва в более тяжелых ситуациях.
Выбор ЦА в качестве первоначального антибиотика при внебольничной пневмонии у больных моложе 60 лет без сопутствующей патологии следует считать, по-видимому, не всегда оправданным. Это обусловлено этиологически широким спектром пневмоний в данной ситуации, который может включать не только пневмококки и Н.influenzae, но и так называемые атипичные возбудители — Мусорlаzma pneumоniaе, Legionella, Chlamidia pneumоniaе, которые не чувствительны к цефалоспоринам всех генераций. Между тем рациональная эмпирическая антибактериальная терапия бронхолегочных инфекций, в том числе пневмоний, должна предусматривать выбор препарата, по возможности активного против всех вероятных в данной ситуации возбудителей. К сожалению, сегодня трудно назвать препарат, полностью удовлетворяющий этим требованиям, за исключением нового поколения фторхинолонов или «респираторных» фторхинолонов. Некоторые из них — например, грепафлоксацин — проходят сейчас в нашей стране регистрацию. В случаях назначения ЦА при данном варианте пневмоний предпочтение следует отдавать ЦА I и II поколения. Применение в подобных ситуациях ЦА III поколения нерационально ввиду высокого риска развития резистентности. Выбор конкретного препарата среди ЦА I–II поколения должен осуществляться исходя из преимущества лекарственных форм, фармакокинетических свойств, стоимости и др. При нетяжелых пневмониях возможно назначение оральных цефалоспоринов. При этом необходимо иметь в виду их различную противомикробную активность по отношению к различным микроорганизмам. Так, например, цефтибутен обладает наибольшей активностью в отношении Н.influenzae, а цефуроксим аксетил — в отношении S.аureus.
Общие принципы выбора первоначального ЦА сохраняются и у больных пневмонией на фоне тяжелых сопутствующих заболеваний (ХОЗЛ, сердечная недостаточность, сахарный диабет, алкогольная интоксикация и др.) и в возрасте старше 60 лет. Этиологическое значение в данной клинической ситуации приобретают Н.influenzae, S.аureus, некоторые грамотрицательные микроорганизмы (Е.соli, Сlebsiella), возрастает частота бета-лактамазопродуцирующих бактерий. В связи с этим возрастает значение препаратов, активных в отношении названных возбудителей. Известно, что противомикробное действие ЦА при переходе активности от первого поколения к последующим характеризуется снижением противостафилококковой активности и преобладанием активности против некоторых грамотрицательных микроорганизмов. Ценным свойством является устойчивость ЦА II поколения к b-лактамазам. В связи с этим врач должен ориентиро-ваться в данной ситуации на цефалоспорины II или по крайней мере III поколения.
Иной подход, определяющий выбор ЦА для лечения бронхолегочной инфекции, наблюдается у больных с «госпитальной» инфекцией. Госпитальные пневмонии занимают особое место среди всех внутрибольничных инфекций из-за тяжести течения и трудностей терапии. Основными возбудителями госпитальных пневмоний являются грамотрицательные микроорганизмы семейства Еntеrobacteriacea — Сlebsiella, Protei, Enterobacter, Providencia, Serracia, а также Staphylococcus аureus, как чувствительный, так и устойчивый к метициллину. Вероятность этиологической роли того или иного инфекционного агента при госпитальных пневмониях определяется особенностями клинической ситуации (послеоперационный период, пребывание в реанимации, искусственная вентиляция легких и т. д.). У больных реанимационных и ожоговых отделений, с иммунодефицитами и муковисцидозом основным микроорганизмом бактериальных осложнений является синегнойная палочка, выявляемая в 70–95% случаев. Наряду с ней у таких больных высевается золотистый стафилококк или гемофильная палочка, устойчивая к ЦА II–III поколения. Основное место в лечении госпитальных пневмоний среди ЦА занимают препараты III (цефтазидим, цефоперазон) и IV поколений (цефпиром, цефепим). С учетом вероятности этиологической роли Pseudomonas aeruginoza в соответствующих ситуациях (ИВЛ, наличие трахеостомы, предшествующая глюкокортикоидная терапия) назначаемые ЦА должны обладать антисинегнойной активностью. Среди имеющихся в распоряжении врача ЦА наибольшей активностью в отношении Pseudomonas aeruginoza обладают цефалоспорины III поколения (цефтазидим, цефоперазон) и IV поколения (цефпиром), которые, однако, не имеют серьезных преимуществ в отношении синегнойной палочки перед цефтазидимом. Появление в терапевтическом арсенале ЦА IV поколения расширяет возможности антибактериальной терапии госпитальных пневмоний с высокой вероятностью грамотрицательной флоры, в том числе золотистого стафилококка, и могут рассматриваться как препараты ургентных ситуаций.
| Цефалоспорины, открытые более 50 лет тому назад, продолжают занимать прочные позиции в лечении различных бактериальных заболеваний, несмотря на появление новых антимикробных средств. Цефалоспориновые антибиотики подразделяются на четыре поколения, отличающиеся по спектру действия, антибактериальной активности, стабильности в присутствии b-лактамаз, фармакокинетическому профилю. Все это наряду с многообразием лекарственных форм и стоимостью определяет их различные показания. Очевидно, что по мере появления новых поколений цефалоспориновых антибиотиков в клинической практике возникает немаловажная проблема дифференцированного назначения препарата с учетом свойств как самого антибиотика, так и особенностей инфекционно- воспалительного процесса у конкретного больного |
Таким образом, рациональный выбор первоначального ЦА для лечения инфекций верхних и нижних дыхательных путей определяется в первую очередь вероятностью этиологической роли того или иного микроорганизма в конкретной клинической ситуации. Такой подход требует от практического врача (а именно от него зависит адекватный выбор препарата) умения выявлять особенности каждого случая пневмонии (эпидемиологическую обстановку, фоновую патологию, факторы риска и др.) и ориентировки в антимикробном спектре назначаемого антибиотика. Однако в клинической практике при выборе ЦА, как, впрочем, и других антибиотиков, приходится наряду с ориентировочной этиологией бронхолегочной инфекции учитывать и другие факторы. Среди последних имеет значение фармакокинетика препарата, наличие разнообразных лекарственных форм, риск развития побочных эффектов, стоимость и др.
В настоящее время не окончательно определено место пероральных препаратов III поколения в клинической практике, так как их сравнительная клиническая и бактериологическая эффективность мало отличается от препаратов II поколения. Более того, как было сказано выше, преимущество цефалоспоринов III поколения состоит в их высокой активности в отношении b-лактамазопродуцирующих бактерий, наиболее часто вызывающих серьезные стационарные инфекции. Но поскольку в этом случае больные находятся в стационаре, то уже более обоснованно получают парентеральную терапию. В то же время ввиду сниженной активности в отношении грамположительных бактерий, часто являющихся причиной именно амбулаторной инфекции, назначение препаратов III поколения имеет меньше преимуществ перед препаратами II поколения.
Цель антибактериальной терапии состоит не только в достижении клинического эффекта, но и в полной эрадикации возбудителя, т. е. бактериологической эффективности. Это в основном определяется адекватным дозированием препарата для достижения необходимой концентрации в очаге инфекции. Высокая степень накопления препарата в тканях является необходимым требованием к лекарственному веществу.
ЦА первого поколения хуже проникают в ткани, что уменьшает степень бактериальной эрадикации.
Данные о биодоступности оральных ЦА следует иметь в виду при дифференцированном назначении их больным с сопутствующей патологией кишечника, связанной с нарушением всасывания, а также при одновременном приеме антисекреторных препаратов, антацидов, с учетом влияния пищи на всасывание ЦА.
Знание путей элиминации ЦА наряду с оценкой функционального состояния печени и почек (возраст, сопутствующая патология) также может определять выбор более адекватного для данной ситуации препарата. Выбирая ЦА для лечения тяжелых госпитальных пневмоний, например, у новорожденных и стариков или у больных с патологией почек, при наличии почечной недостаточности предпочтение следует отдать цефоперазону с учетом его преимущественно билиарной экскреции.
При дифференцированном выборе ЦА необходимо учитывать риск развития побочных эффектов. Наиболее типичны реакции гиперчувствительности (лихорадка, кожная сыпь), гематологические синдромы (цитопения, эозинофилия), нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея), печени (повышение активности трансаминаз), почек (повышение уровня креатинина), ЦНС (головная боль), флебиты при внутривенном введении. Поэтому анамнестические и клинико-лабораторные данные о наличии у больных какой-либо патологии должны влиять на выбор соответствующего препарата.
Флебиты часто возникают при введении цефалотина, цефотаксима, цефепима. Цефуроксим, цефоперазон, цефтибутен могут вызывать анемию (чаще гемолитическую), а при назначении цефалотина, цефамандола, цефотаксима, цефтазидима иногда выявляются фиксированные на эритроцитах антитела. Повышение активности печеночных ферментов возможно на фоне лечения цефоперазоном, цефтриаксоном, цефтазидимом, цефуроксимом. Уровень креатинина может повышаться при лечении цефалексином и цефподоксимом. Оральные цефалоспорины чаще всего вызывают нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея). При лечении парентеральными ЦА отмечено увеличение протромбинового времени, за исключением цефтазидима, не влияющего на синтез факторов протромбинового комплекса и показатели свертываемости крови. Возможны реакции гиперчувствительности (кожная сыпь, лихорадка, эозинофилия) на фоне применения почти всех ЦА III поколения.
Таким образом, дифференцированный выбор ЦА для лечения инфекций верхних и нижних дыхательных путей должен базироваться на учете и адекватной оценке многих факторов, включающих как особенности клинической ситуации, так и антимикробную активность и фармакокинетические характеристики назначаемого препарата.









