коралловые камни в почках это какие камни
Многоточечный анализ минерального состава коралловидных камней в изучении особенностей их формирования
Голованов С.А., Андрюхин М.И., Поликарпова А.М., Сивков А.В., Меринов Д.С., Просянников М.Ю.
Проблема лечения коралловидных камней почек продолжает быть актуальной в урологии, поскольку они в отличие от других типов мочевых камней, обладают особым характером роста, при котором отростки конкремента постепенно заполняют внутренние полости чашечно-лоханочной системы почки, приводя, в конечном счете, к снижению функции этого органа. При коралловидном нефролитиазе хроническая болезнь почек распространена намного больше и имеет более серьезные последствия, чем считалось ранее [1]. Кроме того, оперативное лечение коралловидных камней более травматично и связано с более высокими рисками развития осложнений и повторного камнеобразования [2,3]. Минеральная основа камня составляет основную массу камня, тогда как на долю органического матрикса приходится всего 2-3% [4]. На разломах мочевых камней часто видна неоднородность их структуры. Это может указывать на существование особенностей минерального состава в различных слоях камня, что обусловлено характерным эпитаксиальным ростом мочевого камня, когда происходит формирование одного слоя кристалла поверх слоя другого. Такой же характер роста можно предполагать и у коралловидных камней.
Однако данные по химическому составу различных слоев коралловидного камня в доступной литературе отсутствуют.
Учитывая это, целью нашей работы явилось сравнение минерального состава различных слоев и зон коралловидных камней для выяснения особенностей их формирования и роста.
МАТЕРИАЛЫ И МЕТОДЫ
При этом анализировался состав фрагментов, взятых из разных зон одного и того же конкремента. Образцы материала отбирали из внутреннего и коркового слоев отдельно лоханочной части камня и его рогового отростка чашечной области. Анализировали минеральный состав 4-х зон каждого коралловидного камня: наружного коркового слоя отростка области чашечек (зона 1), внутреннего слоя этого отростка (зона 2); наружного коркового слоя отростка области лоханки (зона 3) и внутренней сердцевины этого отростка (зона 4). Минеральный состав мочевых конкрементов определяли методом инфракрасной спектроскопии на ИК-Фурье спектрометре Nicolet iS10 (Thermo Scientific, США). Соотношение минеральных компонентов в камне определяли с использованием библиотеки спектров мочевых камней известного состава. Для обработки данных использовали статистический пакет Statistica v 10.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
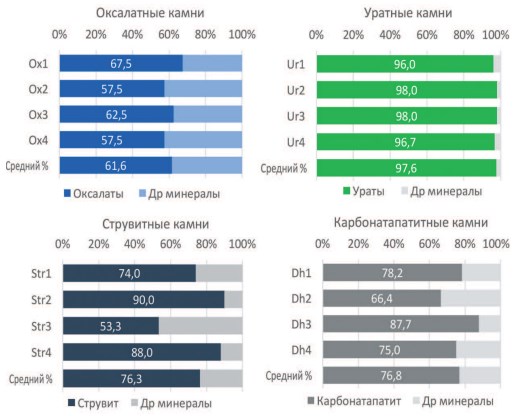
Результаты анализа минерального состава наружных (корковых) и внутренних слоев отростков коралловидных камней, как в области лоханки, так и области чашечек, представлены на рисунке 1.
Рис. 1. Среднее содержание главного минерального компонента в 4-х зонах мочевых камней: в оксалатных камнях (Ox1-Ox4); в уратных камнях (Ur1-Ur4); в камнях из карбонатапатита (даллита) (Dh1-Dh4); в струвитных камнях (Str1-Str4)
Можно заметить, что соотношение минеральных компонентов в различных зонах коралловидных камней достаточно стабильно и в целом характеризует принадлежность конкремента к определенному метаболическому типу. Во всех случаях отнести принадлежность камня к конкретному метаболическому типу можно либо, измельчив весь камень и взяв часть образца для анализа, либо провести анализ образца любой из 4-х зон камня, выбранных для исследования. Таким образом, для диагностики метаболического типа камня, по-видимому, нецелесообразно проводить анализ минерального состава различных его зон. Общепринятым подходом является исследование химического состава либо целого камня, либо его фрагментов, после тщательного измельчения образцов, как это рекомендовано в соответствующих методиках по инфракрасному анализу состава мочевых камней 11.
В отличие от других типов мочевых камней коралловидные камни обладают уникальной формой и особым характером роста, что может проявляться различиями химического состава различных слоев и участков камня.
Как известно, мочевой камень состоит из ядра, представленного сгустком органического вещества (матрикса) либо скоплением кристаллов и их зерен, поверх которого формируется несколько слоев, состоящих из минеральных и органических веществ. Таким образом, уролиты, имеющие ритмически-зональное строение, характеризуются чередованием слоев разного состава [12].
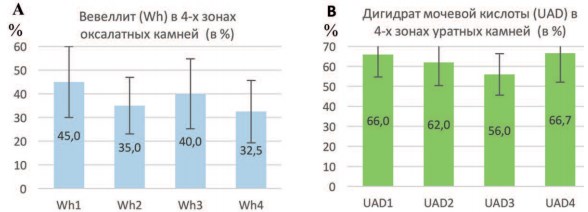
Было отмечено, что во внешних слоях оксалатных коралловидных камней в зонах, относящихся к области чашечек (зона 1), происходит более активное накопление вевеллитного минерального компонента, по сравнению с внутренними зонами этих камней, то есть области чашечек (зона 2) и области лоханки (зона 4) (рис. 2).
Рис. 2. Среднее содержание (M ± m) в 4-х зонах оксалатных (A) и уратных (B) мочевых камней: вевеллита (Wh) (Wh1-Wh4) и дигидрата мочевой кислоты (UAD) (UAD1-UAD4) Показатели достоверности различия: Wh1-Wh2 p=0,092; Wh1-Wh4 p=0,015; Wh3-Wh4 p=0,058
Отчетливая тенденция к накоплению относительного содержания вевеллита наблюдается в корковой зоне лоханочной области камня [Wh3], (40,0 ± 14,7%) по сравнению с внутренними слоями этой области [Wh4], (32,5 ± 13,1%, p=0,058).
Однако наибольшее накопление этого минерала происходит в корковой зоне, предлежащей к области чашечек [Wh1], (45,0 ± 15,0%), по сравнению с внутренними слоями этой области [Wh2], (35,0 ± 11,9%, p=0,092, тенденция) и особенно — по сравнению с внутренними слоями лоханочной области [Wh4], (32,5±13,1%, p=0,015) (рис.2).
По-видимому, накопление вевеллита в корковых слоях может являться результатом воздействия тех механизмов литогенеза, которые отвечают за особый характер роста коралловидных оксалатных камней, в частности за формирование отростков, растущих преимущественно в сторону чашечек.
В коралловидных камнях, представленных уратами, не наблюдалось достоверных отличий в распределении таких минеральных компонентов, как безводная мочевая кислота (UA), и ее дигидратная форма (UAD) по наружным или внутренним слоям в областях чашечек или лоханки (рис. 2). Однако отмечено, что во внутренних слоях отростка области чашечек, в зоне 2 [Ur2] содержание уратного компонента положительно коррелирует с уровнем экскреции мочевой кислоты (ранговый коэффициент корреляции Спирмена r=0,9487, p=0,0513), а содержание мочевой кислоты в этой зоне имеет отрицательную корреляцию с величиной экскреции кальция (r=-0,9487, p=0,0513).
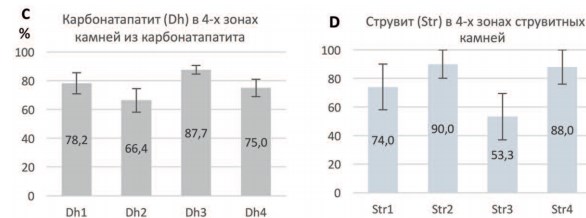
В камнях из карбонатаппатита, то есть состоящих главным образом из минерала даллита [карбонатапатит фосфат, Dahllite (Dh)] подобно оксалатным камням, отчетливо прослеживается тенденция накопления карбонатапатита в поверхностных корковых слоях коралловидного камня (рис.3). Так, в области чашечек содержание карбонатапатита в наружных корковых слоях [Dh1] достигало в среднем 78,2 ± 7,4% по сравнению с содержанием этого минерала во внутренних слоях камня той же области чашечек [Dh2], (66,4± 8,2%, p=0,0182, критерий серий Вальда-Вольфовица). Однако наиболее высокое накопление карбонатапатита отмечалось в поверхностных слоях камня области лоханки [Dh3], (87,7±3,0%) в отличие от внутренних слоев камня, находящихся в лоханочной области [Dh4], (75,0±6,0%, р=0,0421) (рис. 3).
Рис. 3. Среднее содержание (M ± m) в 4-х зонах карбонатапатитных (C) и струвитных (D) мочевых камней: карбонатапатита, (даллита,Dh) Dh1-Dh4 и струвита (Str) (Str1-Str4) Показатели достоверности различия: Dh1-Dh2 p=0,018; Dh2-Dh3 p=0,030; Dh3-Dh4 p=0,042 Str2-Str3 p=0,043; Str3-Str4 p=0,043
Сравнение этих результатов с показателями экскреции некоторых метаболических факторов риска развития уролитиаза показывает, что накопление карбонатапатита в корковых слоях камня области лоханки [Dh3] имеет обратную корреляцию с показателями суточной экскреции мочевой кислоты (r= — 0,905, p=0,005) и фосфатов (r= — 0,764, p=0,046). Полученные данные находятся в соответствии с результатами проведенных ранее исследований, в которых изучалась связь метаболических факторов и частоты формирования камней определенного метаболического типа. Было отмечено, что между степенью выраженности урикурии и частотой выявления камней из карбонатапатита существует обратная зависимость [13]. Та же обратная зависимость между частотой образования камней из карбонатапатита и фосфатурией была отмечена и в другой работе [14].
Обнаруженная зависимость роста наружных слоев коралловидных камней от экскреции с мочой некоторых продуктов обмена, способных оказывать влияние на литогенез, указывает на возможность поиска методов, препятствующих или предупреждающих рост почечных камней в виде кораллов.
В отличие от кальциевых (оксалатных и карбонатапатитных) камней, струвитные коралловидные конкременты, наоборот, склонны накапливать струвит во внутренних слоях камня, нежели в поверхностных (рис. 3). Самая низкая концентрация струвита обнаружена в корковых слоях лоханочной части камня [Str3] (53,3 ± 16,3%), а самая высокая — во внутренних слоях лоханочной части [Str4] (88,0 ± 12,0%, p=0,0431) и области чашечек [Str2] (90,0 ± 10,0%, p=0,0431, по критерию Вилкоксона для парных сравнений). Таким образом, содержание струвита в коре лоханочной части камня на 65-69% меньше, чем во внутренних слоях областей этого камня [Str2] и [Str4].
Обнаружено, что накопление струвита во внутренних слоях камня лоханочной области [Str4] положительно коррелирует с величиной суточной экскреции кальция (r=0,826, р=0,0220) и мочевой кислоты (r=0,796, p=0,0321). Интересно отметить, что если повышенная экскреция кальция приводит к накоплению струвита во внутренних слоях лоханочной области камня, то при этом гиперкальциурия может усиливать отложение струвита на поверхности отростка, растущего в сторону чашечек [Str1], (r=0,9276, p=0,0077). Возможно, что этими биохимическими изменениями мочи в определенной степени объясняется особая форма и быстрый рост струвитных коралловидных камней, постепенно заполняющих своей массой чашечно-лоханочную систему почки.
Хорошо известно, что главной причиной возникновения коралловидных камней и, в особенности струвитных, являются бактерии, а именно уреазопродуцирующие бактерии, такие как Proteus mirabilis, Klebsiella species, Providencia rettgeri и Morganella morganii. Эти бактерии, как известно, расщепляя мочевину, приводят к повышению рН мочи выше 7,0 и образованию конкрементов из струвита. Имеются данные об участии в фосфатном литогенезе нанобактерий, которые, образуя фосфатную оболочку, могут служить центром кристаллизации и приводить к образованию депозитов кальция фосфата в почечных лимфатических протоках и собирательных трубочках [15,16]. В зоне собирательных трубочек и нижних отделах нефрона кристаллы фосфата кальция способны индуцировать гетерогенную нуклеацию кальция оксалата с образованием в почечных сосочках «бляшек Рэндела» [15,16], служащих основой для формирования кальциевых камней. Из этого следует, что коралловидные камни инфекционного происхождения могут образовываться при участии уреазопродуцирующих бактерий и нанобактерий.
Известно, что среди пациентов с коралловидный нефролитиазом у 64,7% больных наблюдается рост микрофлоры в посеве мочи [17]. Сходные данные были получены и в настоящей работе. У 19 из 31 обследованных больных (61,3%) в посеве мочи отмечался рост микрофлоры. Эти пациенты имели преимущественно инфекционные конкременты, которые состояли из струвита и/или карбонатапатита (даллита). В бактериальном посеве мочи были обнаружены: Klebsiella pneumoniae (5 больных), Escherichia coli (4 больных), Enterococcus faecalis (4 больных), Staphylococcus hemoliticus (2 больных), Proteus mirabilis (2 больных), Citrobacter breundi (1 больной), Corynebacterium glucuronolitycum (1 больной). Полученные данные подтверждают тот факт, что конкременты, состоящие из струвита или карбонатапатита (даллита) имеют инфекционное происхождение. Можно полагать, что инфекция в сочетании с метаболическими нарушениями может способствовать превращению обычного камня лоханки в коралловидный конкремент в результате индуцированной микрофлорой вторичной кристаллизации фосфатов.
ЗАКЛЮЧЕНИЕ
Формирование коралловидных камней различного минерального состава имеет свои особенности. Литогенез оксалатных камней характеризуется накоплением вевеллита в корковой зоне области чашечек. Образование камней из карбонатапатита протекает сходным образом, однако минерал карбонатапатит склонен преимущественно накапливаться в поверхностных слоях камня в области лоханки, нежели в области чашечек, что коррелирует со снижением суточной экскреции мочевой кислоты и фосфатов. В уратных коралловидных камнях не отмечено различий распределения уратных компонентов в различных зонах камня. Тем не менее, выявлена положительная корреляция между накоплением уратов во внутренних слоях области чашечек и суточной экскрецией мочевой кислоты. В струвитных коралловидных камнях минерал струвит накапливается преимущественно во внутренних слоях камня, коррелируя с повышенной экскрецией кальция и мочевой кислоты, что отличает литогенез этих камней от кальций-содержащих конкрементов (оксалатных и карбонатапатитных).
Особенности литогенеза коралловидных камней, относящихся к различным метаболическим типам, указывают на необходимость особых подходов к выбору лечебных мер предупреждения роста коралловидных камней в ходе метафилактики, включая рациональную антибиотикотерапию и коррекцию имеющихся литогенных метаболических нарушений.
ЛИТЕРАТУРА
1. Хасигов А.В., Белоусов И.И., Коган М.И. Оценка резервов почечных функций при чрескожной нефролитотомии коралловидного нефролитиаза. Урология 2012;(6):70-73
2. Акилов Ф.А., Мухтаров Ш.Т., Гиясов Ш.И., Насыров Ф.Р., Мирхамидов Д.Х.. Интраоперационные осложнения эндоскопического удаления камней из верхних мочевыводящих путей. Урология 2013;(2):79-82.
3. Ganpule AP, Vijayakumar M, Malpani A, Desai MR. Percutaneous nephrolithotomy (PCNL) a critical review. Int J Sur 2016;36(Pt D):660-664; DOI: 10.1016/j.ijsu.2016.11.028.
4. Маждракова Г., Попова Н. Болезни почек. Медицина и физкультура. София, 1980. 805 с.
5. Rendina D, De Filippo G, De Pascale F, Zampa G, Muscariello R, De Palma D, et al. The changing profile of patients with calcium nephrolithiasis and the ascendancy of overweight and obesity: a comparison of two patient series observed 25 years apart. Nephrol Dial Transplant. 2013;28(Suppl 4):iv146-51. doi: 10.1093/ndt/gft076.
7. Daudon M, Lacour B, Jungers P. Influence of body size on urinary stone composition in men and women. Urol Res 2006;34(3):193-9. Epub 2006 Feb 11. doi: 10.1007/s00240-006-0042-8
8. Hesse A, Schneider H.-J., Hienzsch E. Die infrarotspektroskopische Harnsteinanalyse. Dtsch Med Wochenschr 1972;97:1694-1701.
9. Hesse A, Molt K. The technique of analysis of urinary calculi by infrared spectroscopy (in German). J Clin Chem Clin Biochem 1982;20:861-73.
10. Hesse A, Kruse R, Geilenkeuser WJ, Schmidt M. Quality control in urinary stone analysis: results of 44 ring trials (1980-2001). Clin Chem Lab Med 2005;43(3):298-303.
11. Abdel-Halim RE, Abdel-Halim MR. A review of urinary stone analysis techniques. Saudi Med J 2006t;27(10):1462-7
12. Полиенко А.К. Минеральный состав, морфология и структура уролитов. Дисс. докт. геолого-минеральных наук, Томск; 2014. URL: http://www.lib.tpu.ru/fulltext/a/2014/01.pdf
13. Голованов С.А., Сивков А.В., Дрожжева В.В., Анохин Н.В. — Метаболические факторы риска и формирование мочевых камней. Исследование I: влияние кальцийурии и урикурии. Экспериментальная и клиническая урология 2017;(1):52-57.
14. Голованов С.А., Сивков А.В., Дрожжева В.В., Анохин Н.В. — Метаболические факторы риска и формирование мочевых камней. Исследование II: влияние фосфатурии и магнийурии. Экспериментальная и клиническая урология 2017;(2):40-46.
15. Letavernier E, Vandermeersch S, Traxer O, Tligui M, Baud L, Ronco P, et al. Demographics and Characterization of 10,282 Randall Plaque-Related Kidney Stones. Medicine (Baltimore) 2015; 94(10): 566. doi: 10.1097/MD.0000000000000566.
16. Singh VK, Rai PK. Kidney stone analysis techniques and the role of major and trace elements on their pathogenesis: a review. Biophys Rev 2014; 6(3-4): 291-310. doi: 10.1007/s12551-014-0144-4.
17. Ma K, Huang XB, Xu QQ, Li JX, Xiong LL. Infrared spectrophotometry for crystalline composition of staghorn calculi. Zhonghua Yi Xue Za Zhi 2010;90(44):3150-2
Большой камень в почке
Большой камень в почке (коралловидный камень почки) – может иметь разные размеры, что в большей степени обусловлено размером лоханки самой почки, т.к камень принимает ее размеры. Отсюда и название “коралловидный”. Однако, большой камень в вашей почке необязательно должен быть какой либо причудливой формы, иногда они бываю шаровидные или овальные.
Камень в почке мы называем “большим” тогда когда его размер превышает 2 см. По большому счету это обусловлено лишь хирургической тактикой, так как данные камни не подлежат дистанционному дроблению. Как мы лечим такие камни вы можете узнать в статье: Чрескожная нефролитотрипсия.
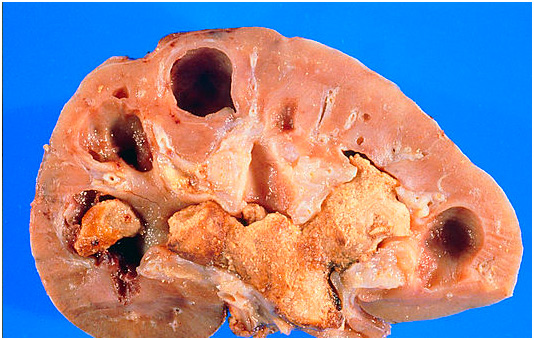
Рисунок. Большой конкремент почки.
В литературе вы можете встретить такие названия больших камней, как коралловидный конкремент или камень в виде оленьего рога. Почему они так называются? Потому что конкременты могут достигать таких размеров, что занимают значительное пространство чашечно-лоханочной системы почки, принимая ее причудливую форму, напоминая коралл или олений рог. В зависимости от размера коралловидного конкремента и его расположения в почечно-лоханочной системе, выделяют четыре степени, или стадии:
1 стадия – конкремент заполняет лоханку почки и одну из чашечек;
2 стадий – камень настолько большой, что занимает всю лоханку и две или более чашечки;
3 стадия большой камень почки расположен в лоханке с отростками во всех чашечках;
4 стадия – конкремент выполняет всю чашечно-лоханочную систему почки, вызывая изменение ее формы, т.е. деформацию.
Рисунок. Большой камень в почке.
Рисунок. Большой камень в почке.
Также можно встретить и такую классификацию больших камней в почках, как неполные и полные коралловидные конкременты. Термин «неполный коралловидный конкремент» означает, что он заполняет лоханку почки и отдает отростки в чашечках, но при этом не занимает всю чашечно-лоханочную систему. «Полный коралловидный конкремент» выполняет всю полостную систему почки.
Большие камни в почках чаще всего состоят из магниевых солей аммоний фосфата (т.е. это струвитные, или инфекционные камни) и/или кальций апатитов. Конкременты, состоящие из цистина или уратов, в чистой форме или в смеси с другими химическими элементами, также могут достигать больших размеров, принимая причудливую коралловидную форму. Кальций оксалатные и кальций фосфатные конкременты могут достигать больших размеров, но, как правило, не принимают форму коралла или оленьего рога.
Клинический случай. В 2007 году описывался случай большого почечного конкремента, размером 230*140 мм и весом 1,350 грамм, располагающийся в единственной работающей почке. При этом мужчина 47 лет жаловался на боль в поясничной области справа. При его обследовании в моче обнаружили кровь. А после выполнения ультразвукового исследования, внутривенной пиелографии и компьютерной томографии установили наличие большого камня в правой почке и полное отсутствие функции левой почки. Камень был удален путем нефролитотомии, по составу он представлял собой кальций фосфатный конкремент.
Со временем, не леченный большой камень в почке может вызывать угрожающие жизни состояния, такие как почечная недостаточность или инфекция крови (сепсис).
Если большой камень в почке своевременно не удалить у четверых пациентов из пяти произойдет нарушение функции органа. Полное удаление конкремента является главной целью лечения! Только полное его удаление дает возможность избавиться от инфекционных возбудителей, вызывающих образование конкремента, прекратить дальнейший его рост, предотвратить закупорку почки.
Возможные способы лечения коралловидных конкрементов:
Если сравнивать чрескожную нефролитотрипсию и дистанционное дробление конкрементов, то частота успешного лечения достигает 78% и 54% соответственно. В среднем необходимо 1,9 процедура для полного удаления большого камня путем чрескожной нефролитотрипсии, 3,3 комбинированные процедуры, 3,6 процедур дистанционного дробления.
В прошлом широко было распространено открытое удаление больших камней почки, однако в настоящее время наиболее широко применяется чрескожная нефролитотрипсия. Иногда может понадобиться несколько процедур для полного очищения органа от камней.
Рисунок. Большой коралловидный камень почки.
Фотография дня – 26 марта 2010 года в английской газете «Телеграф». Доктор демонстрирует килограммовый камень, удаленный у Шан Цьеу Джи. Фотография сделана у кровати пациента, провинция Дзилин, Китай.
Главное меню
Главное меню
Современные подходы к лечению крупных и коралловидных камней единственной или единственно-функционирующей почки
Оперативное лечение пациентов с крупными и коралловидными камнями анатомически или функционально единственной почки представляет собой сложную проблему и должно быть тщательно спланировано. Это обусловлено тем, что дальнейшее ухудшение функции единственной почки или потеря органа в результате оперативного лечения неминуемо приведут к существенному снижению качества жизни, связанному с необходимостью постоянного проведения диализа или выполнения трансплантации почки. Именно поэтому в таких случаях необходимо выбрать самый безопасный метод для удаления конкрементов, чтобы свести к минимуму риск различных осложнений, повторных операций и потери органа. Эндоскопические методы удаления конкрементов предполагают меньшую хирургическую травму почки и, следовательно, низкий риск прогрессирования нарушения функции почки. В силу малой частоты осложнений и высокой эффективности лечения эндоскопические процедуры такие, как перкутанная нефролитотрипсия (ПНЛ) и ретроградная интраренальная хирургия (РИРХ), в настоящее время занимают ведущее место в удалении камней единственной почки [1, 2]. Однако эффективность лечения зависит от навыков и опыта хирурга. Кроме того, при определенных клинических ситуациях применение эндоскопических методов лечения является нецелесообразным, что диктует необходимость использования открытых или лапароскопических способов удаления камней почек [3, 4]. С учетом вышеуказанных обстоятельств актуальным представляется анализ современных подходов к лечению крупных и коралловидных камней единственной почки для выработки оптимальной тактики ведения этой сложной категории пациентов.
ДИСТАНЦИОННАЯ ЛИТОТРИПСИЯ (ДЛТ)
К крупным камням почек относят камни размером более 20 мм, и ДЛТ рассматривается как один из возможных методов лечения у части пациентов с крупными камнями единственной почки. Однако следует отметить, что этот метод в качестве монотерапии, в основном, применяется при камнях почки до 20 мм [5]. В случае монотерапии ДЛТ при более крупных камнях в качестве максимального размера было указано значение 40 мм х 30 мм [6]. По мнению Н.К. Дзеранова [7], при крупных и коралловидных камнях (К-1 и К-2 по классификации НИИ урологии [8]) ДЛТ должна проводиться только на фоне дренированной единственной почки и с использованием низкоэнергетических ударноволновых импульсов.
Известно, что чем больше размер конкремента, тем выше количество сеансов ДЛТ. В соответствии с рекомендациями Европейской Ассоциации Урологов (EAU) количество сеансов на камень не должно превышать 3-5 сессий [9]. Зависимость результатов лечения от размеров конкремента продемонстрирована в работе Penn HA et al. [10], по данным которых эффективность ДЛТ для конкрементов почек размером менее 10 мм составляет 92%, 10-20 мм – 5989%, более 20 мм – 39-70%. Поэтому при крупных и коралловидных камнях единственной почки ДЛТ служит, в основном, в качестве дополнительной лечебной опции для разрушения оставшихся фрагментов камней после применения других, прежде всего, эндоскопических методов лечения. В то же время, согласно рекомендациям Американской Урологической Ассоциации (AUA), ДЛТ не должна рассматриваться в качестве обязательного финального метода в комбинации с ПНЛ [11]. Вследствие этих обстоятельств опыт использования ДЛТ как монотерапии при данных формах мочекаменной болезни (МКБ) в мировой практике невелик. Например, в работе М.Ф. Трапезниковой и соавт. [12] среди 49 пациентов с нефролитиазом единственной почки, подвергнутых ДЛТ, только 4 пациента имели размер камня более 20 мм.
Большую работу по исследованию возможностей ДЛТ в виде монотерапии камней единственной почки провел С.А. Москаленко [13]. Из 130 пациентов с единственной почкой, включенных в его исследование, в 13 случаях имело место наличие крупных и в 2 случаях – коралловидных камней. При крупных камнях среднее число сеансов ДЛТ на 1 пациента составило 2,8±1,1, а положительный результат (фрагментация камня до размеров менее 4 мм и отхождение фрагментов) в сроки до 1 месяца после лечения не наблюдали ни в одном случае, в сроки до 3 месяцев – в 2 cm in size) without stenting. // Indian J Urol. 2010. Vol. 26, N 3. P. 359-363.
17. Бешлиев Д.А. Опасности, ошибки, осложнения дистанционной литотрипсии, их лечение и профилактика: Дис. … д-ра мед. наук. М., 2003. 356 с.
18. Hesse A, Miersch WD. Special aspects of stone composition and aetiology of different types of urinary calculi. // Int Urol Nephrol. 1989. Vol. 21, N 3. P. 257-260.
19. Różański W, Miękoś E, Górkiewicz Z, Szkodziński A. Crush endurance of urinary stones. // Urol Pol. 1995. Vol. 48. P. 1.
20. El-Nahas AR, Shoma AM, Eraky I, El-Kenawy MR, El-Kappany HA. Percutaneous endopyelotomy for secondary ureteropelvic junction obstruction: prognostic factors affecting late recurrence. // Scand J Urol Nephrol. 2006. Vol. 40, N 5. P. 385-390.
21. Mehrabi S, Karimzadeh Shirazi K. Results and complications of spinal anesthesia in percutaneous nephrolithotomy // Urol J. 2010. Vol. 7, N 1. P. 22-25.
22. Rastinehad AR, Andonian S, Smith AD, Siegel DN. Management of hemorrhagic complications associated with percutaneous nephrolithotomy. // J Endourol. 2009. Vol. 23, N 10. P. 1763-1767.
23. Srinivasan AK, Herati A, Okeke Z, Smith AD. Renal drainage after percutaneous nephrolithotomy // J Endourol. 2009. Vol. 23, N 10. P. 1743-1749.
24. Chen L, Xu QQ, Li JX, Xiong LL, Wang XF, Huang XB. Systemic inflammatory response syndrome after percutaneous nephrolithotomy: an assessment of risk factors. // Int J Urol. 2008. Vol. 15, N 12. P. 1025-1028.
25. Cadeddu JA, Chen R, Bishoff J, Micali S, Kumar A, Moore RG, Kavoussi LR. Clinical significance of fever after percutaneous nephrolithotomy. // Urol. 1998. Vol. 52, N 1. P. 48-50.
26. Segura JW. Staghorn calculi. // Urol Clin North Am. 1997. Vol. 24, N 1. P. 71-80.
27. Mahboub MR, Shakibi MH. Percutaneous nephrolithotomy in patients with solitary kidney. // Urol J. 2008. Vol. 5, N 1. P. 24-27.
28. Xu R, Yi L, Wang X, Zhao H, Dong Z, Jiang H, Wu H, Zhao X, Liu R. Efficacy and safety of percutaneous nephrolithotomy for treatment of staghorn stones in solitary kidney. // Zhong Nan Da Xue Xue Bao Yi Xue Ban. 2012. Vol. 37, N 6. P. 621-624.
29. Resorlu B, Kara C, Oguz U, Bayindir M, Unsal A. Percutaneous nephrolithotomy for complex caliceal and staghorn stones in patients with solitary kidney. // Urol Res. 2011. Vol. 39, N 3. P. 171-176.
30. Wang Y, Hou Y, Jiang F, Wang Y, Wang C. Percutaneous nephrolithotomy for staghorn stones in patients with solitary kidney in prone position or in completely supine position: a single-center experience. // Int Braz J Urol. 2012. Vol. 38, N 6. P. 788-794.
31. Huang Z, Fu F, Zhong Z, Zhang L, Xu R, Zhao X. Chinese minimally invasive percutaneous nephrolithotomy for intrarenal stones in patients with solitary kidney: a single-center experience. // PLoS One. 2012. Vol. 7, N 7. P. e40577. doi: 10.1371/journal.pone.0040577.
32. Akman T, Binbay M, Tekinarslan E, Ozkuvanci U, Kezer C, Erbin A, Berberoglu Y, Yaser-Muslumanoglu A. Outcomes of percutaneous nephrolithotomy in patients with solitary kidneys: a single-center experience. // Urol. 2011. Vol. 78, N 2. P. 272-276.
33. Canes D, Hegarty NJ, Kamoi K, Haber GP, Berger A, Aron M, Desai MM. Functional outcomes following percutaneous surgery in the solitary kidney. // Urol. 2009. Vol. 181, N 1. P. 154-160.
34. Берников Е.В., Мазуренко Д.А., Лисицин В.Н., Веренинов П.В. Современная диагностика и лечение коралловидных камней почек. // Вопросы урологии и андрологии. 2013. Том 2, № 2. С. 39-43.
35. Комяков Б.К., Гулиев Б.Г., Алексеев М.Ю., Лубсанов Б.В. Перкутанная нефролитотрипсия при камнях единственной и аллотрансплантированной почки. // Урология. 2011. N 5. С. 55-60.
36. Комяков Б.К., Гулиев Б.Г., Алексеев М.Ю. Чрескожное эндоскопическое лечение камней единственной и пересаженной почки. // Бюллетень медицинских Интернет-конференций. 2011. Том 1, N 4. P. 38-50.
37. Garg S, Mandal AK, Singh SK, Naveen A, Ravimohan M, Aggarwal M, Mete UK, Santosh K. Ureteroscopic laser lithotripsy versus ballistic lithotripsy for treatment of ureteric stones: a prospective comparative study. // Urol Int. 2009. Vol. 82, N 3. P. 341-345.
38. Leijte JA, Oddens JR, Lock TM. Holmium laser lithotripsy for ureteral calculi: predictive factors for complications and success. // J. Endourol. 2008. Vol. 22, N 2. P. 257-260.
39. Atis G, Gurbuz C, Arikan O, Kilic M, Pelit S, Canakci C, Gungor S, Caskurlu T. Retrograde intrarenal surgery for the treatment of renal stones in patients with a solitary kidney. // Urol. 2013. Vol. 82, N 2. P. 290-294.
40. Knoll T, Jessen JP, Honeck P, Wendt-Nordahl G. Flexible ureterorenoscopy versus miniaturized PNL for solitary renal calculi of 10-30 mm size. // World J Urol. 2011. Vol. 29, N 6. P. 755-759.
41. Akman T, Binbay M, Ozgor F, Ugurlu M, Tekinarslan E, Kezer C, Aslan R, Muslumanoglu AY. Comparison of percutaneous nephrolithotomy and retrograde flexible nephrolithotripsy for the management of 2-4 cm stones: a matched-pair analysis. // BJU Int. 2012. Vol. 109, N 9. P. 1384-1389.
42. Lai D, He Y, Dai Y, Li X. Combined minimally invasive percutaneous nephrolithotomy and retrograde intrarenal surgery for staghorn calculi in patients with solitary kidney. // PLoS One. 2012. Vol. 7, N 10. P. e48435. doi: 10.1371/journal.pone.0048435.
43. Xu G, Li X, He Y, He Z. Staged single-tract minimally invasive percutaneous nephrolithotomy and flexible ureteroscopy in the treatment of staghorn stone in patients with solitary kidney. // Urol Res. 2012. Vol. 40, N 6. P. 745-749.
44. El-Husseiny T, Buchholz N. The role of open stone surgery. //Arab J Urol. 2012. Vol. 10, N 3. P. 284-288.
45. Anoia EJ, Resnick MI. Open Stone Surgery. // Urinary stone disease: the practical guide to medical and surgical management [edited by Marshall L. Stoller, Maxwell V. Meng]. Totowa, New Jersey: Humana Press, 2007. P. 639-650.
46. Акулин С.М. Осложнения оперативных вмешательств при лечении больных коралловидным нефролитиазом (лечение и профилактика): Дис. … канд. мед. наук. М., 2010. 212 с.
47. Hruza M, Turk C, Frede T, Rassweiler J. Importance of open and laparoscopic stone surgery. // Urologe A. 2008. Vol. 47, N 5. P. 578–586.
48. Gaur DD, Trivedi S, Prabhudesai MR, Madhusudhana HR, Gopichand M. Laparoscopic ureterolithotomy. Technical considerations and long-term followup. // BJU Int. 2002. Vol. 89, N 4. P. 339–343.
49. Kaouk JH, Gill IS, Desai MM, Banks KL, Raja SS, Skacel M, Sung GT. Laparoscopic anatrophic nephrolithotomy feasibility study in a chronic porcine model. // J. Urol. 2003. Vol. 169, N 2. P. 691–696.
50. Deger S, Tuellmann M, Schoenberger B, Winkelmann B, Peters SA, Loening SA. Laparoscopic anatrophic nephrolithotomy. // Scand J Urol Nephrol. 2004. Vol. 38, N 3. P. 263–265.
51. Simforoosh N, Aminsharifi A. Laparoscopic management in stone disease. // Curr Opin Urol. 2013. Vol. 23, N 2. P. 169-174.
52. Tefekli A, Tepeler A, Akman T, Akçay M, Baykal M, Karadağ MA, Muslumanoglu AY, de la Rosette J. The comparison of laparoscopic pyelolithotomy and percutaneous nephrolithotomy in the treatment of solitary large renal pelvic stones. // Urol Res. 2012. Vol. 40, N 5. P. 549-555.
53. Al-Hunayan A, Khalil M, Hassabo M, Hanafi A, Abdul-Halim H. Management of solitary renal pelvic stone: laparoscopic retroperitoneal pyelolithotomy versus percutaneous nephrolithotomy. // Endourol. 2011. Vol. 26, N 6. P. 975-978.