какую стадию испытания проходит спутник
Российские вакцины не прошли все фазы клинического исследования?
Клинические исследования во всем мире являются неотъемлемым этапом разработки препаратов, который предшествует его регистрации и широкому медицинскому применению. В ходе клинических исследований новый препарат изучается для получения данных о его эффективности и безопасности. На основании этих данных уполномоченный орган здравоохранения принимает решение о регистрации препарата или отказе в регистрации.
Проведение клинических исследований в РФ регламентируют: Федеральный закон от 12.04.2010 N 61-ФЗ «Об обращении лекарственных средств» (Статья 40. Проведение клинического исследования лекарственного препарата для медицинского применения), ГОСТ Р 56701-2015 от 2016-07-01 ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ (УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 11 ноября 2015 г. N 1762-ст.), ГОСТ Р 52379-2005 от 2006-04-01 НАДЛЕЖАЩАЯ КЛИНИЧЕСКАЯ ПРАКТИКА (УТВЕРЖДЕН Приказом Федерального агентства по техническому регулированию и метрологии от 27 сентября 2005 года N 232-ст), Правила надлежащей клинической практики ОСТ 42-511-99 (согласно международного стандарта этических норм и качества научных исследований Good Clinical Practice; GCP), Приказ Минздрава России от 01.04.2016 N 200н «Об утверждении правил надлежащей клинической практики» (Зарегистрировано в Минюсте России 23.08.2016 N 43357), приказ Минздрава России от 09.01.2014 № 2н «Об утверждении порядка проведения оценки соответствия медицинских изделий в форме технических испытаний, токсикологических исследований, клинических испытаний в целях государственной регистрации медицинских изделий».
Обычно выделяют четыре фазы клинических испытаний. Фаза I. Цель этапа — убедиться, что препарат можно применять у людей. Фаза II. Цель этапа — дополнительно оценить безопасность лекарства и выяснить, работает ли препарат. Фаза III. Цель этапа — сравнить новый препарат со стандартным лечением. Фаза IV называется постмаркетинговой — этот этап клинического испытания начинается, когда готовое лекарство уже поступает в продажу.
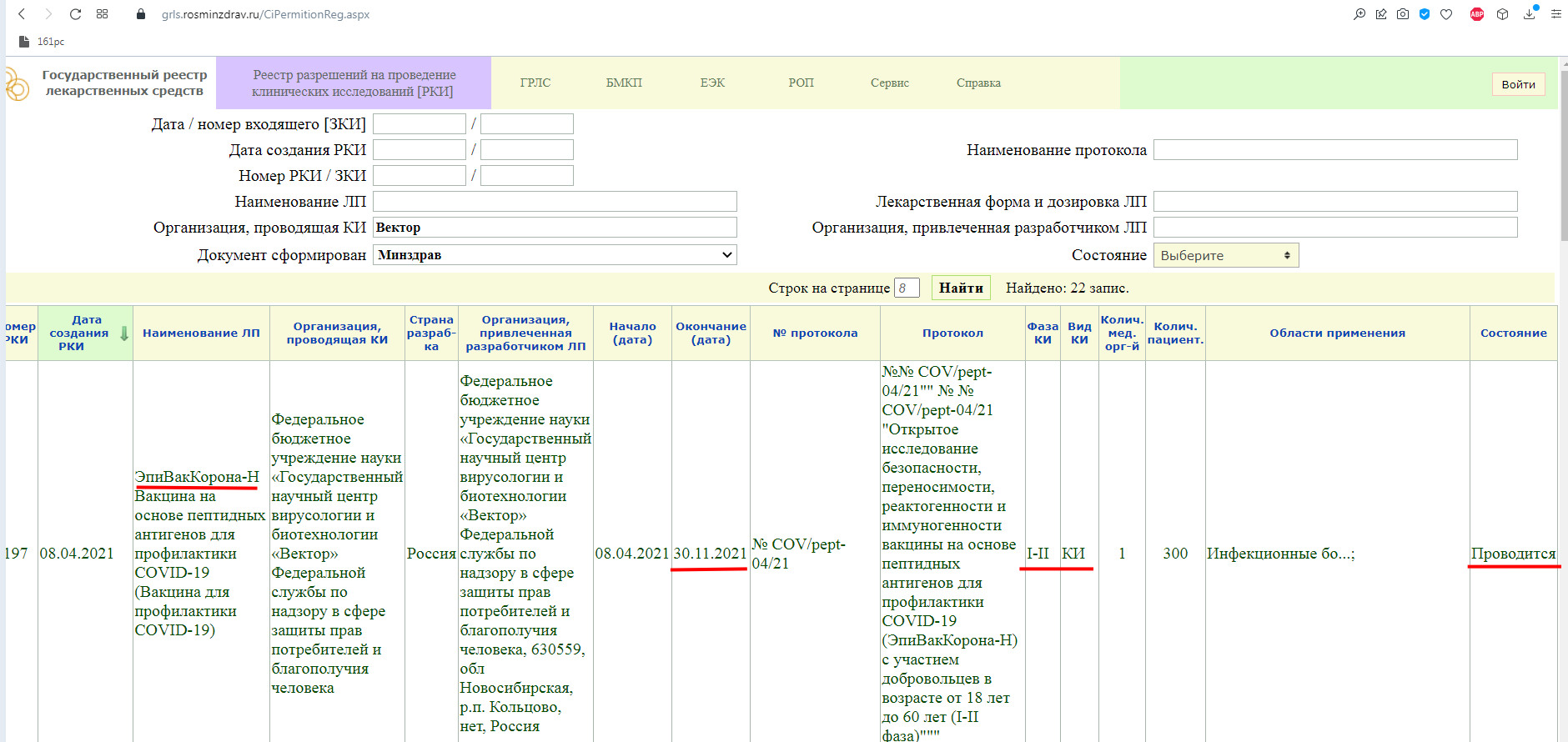
Существует государственный реестр лекарственных средств, который содержит перечень лекарственных препаратов, прошедших государственную регистрацию (Федеральный закон от 12.04.2010 N 61-ФЗ «Об обращении лекарственных средств» Статья 33), другими словами реестр разрешений на проведение клинических исследований (РКИ).
В настоящий момент, у Российской Федерации известно существование нескольких вакцин от коронавируса: «Спутник V» и «Спутник Лайт» («Гам-КОВИД-Вак», Национального исследовательского центра эпидемиологии и микробиологии имени Н. Ф. Гамалеи), «ЭпиВакКорона» (Федерального бюджетного учреждения науки «Государственный научный центр вирусологии и биотехнологии Вектор» Роспотребнадзора), «КовиВак» (Федерального научного центра исследований и разработки иммунобиологических препаратов имени М.П. Чумакова Российской академии наук).
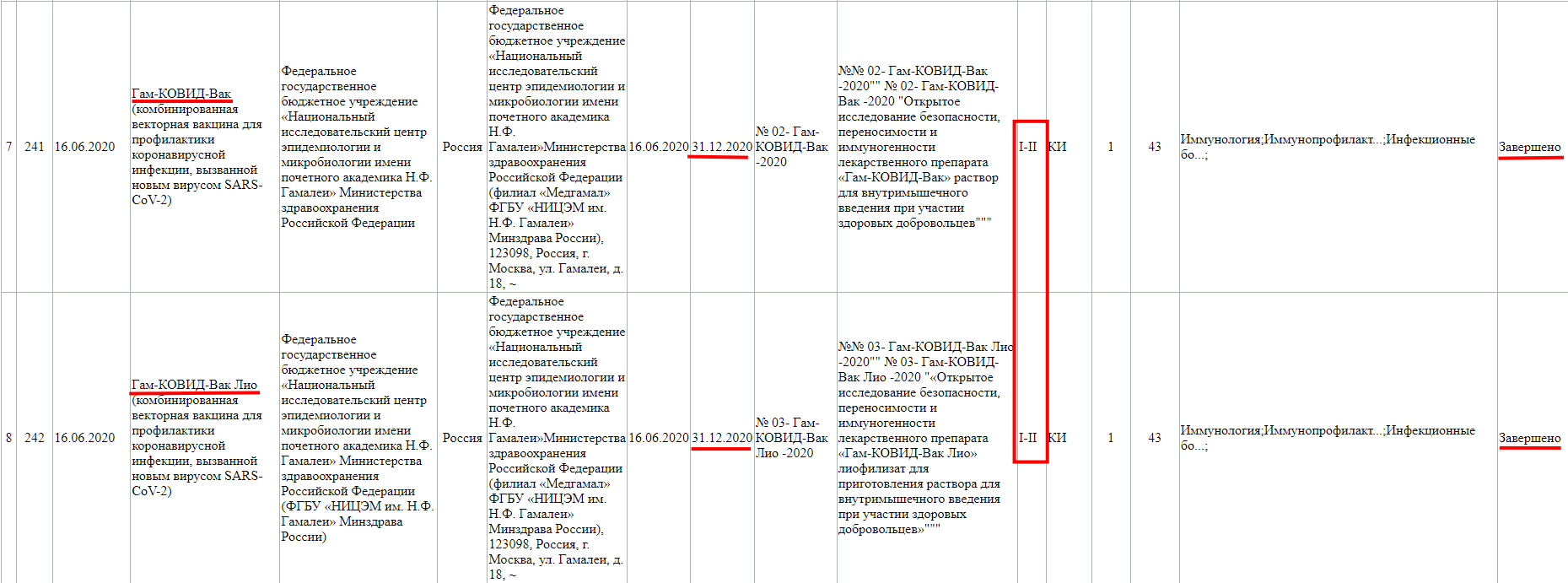
Как мы видим, в настоящий момент, проводится фаза клинического исследования 1-2 с участием добровольцев от 18 до 60 лет, и завершится она 30 ноября 2021 года.
Так же, проводится фаза клинического исследования 3-4 с участием добровольцев от 18 лет, и завершится она 31 августа 2021 года.
Завершенная фаза 3 клинического исследования, с участием добровольцев от 60 лет, и завершилась она 15 мая 2021 года.
Фаза клинического исследования 1-2 с участием добровольцев от 18 до 60 лет, проводится до 30 декабря 2021 года.
Тут так же видно, что проводится фаза клинического исследования 3 с участием добровольцев от 18 до 60 лет, и завершится она 30 декабря 2022 года.
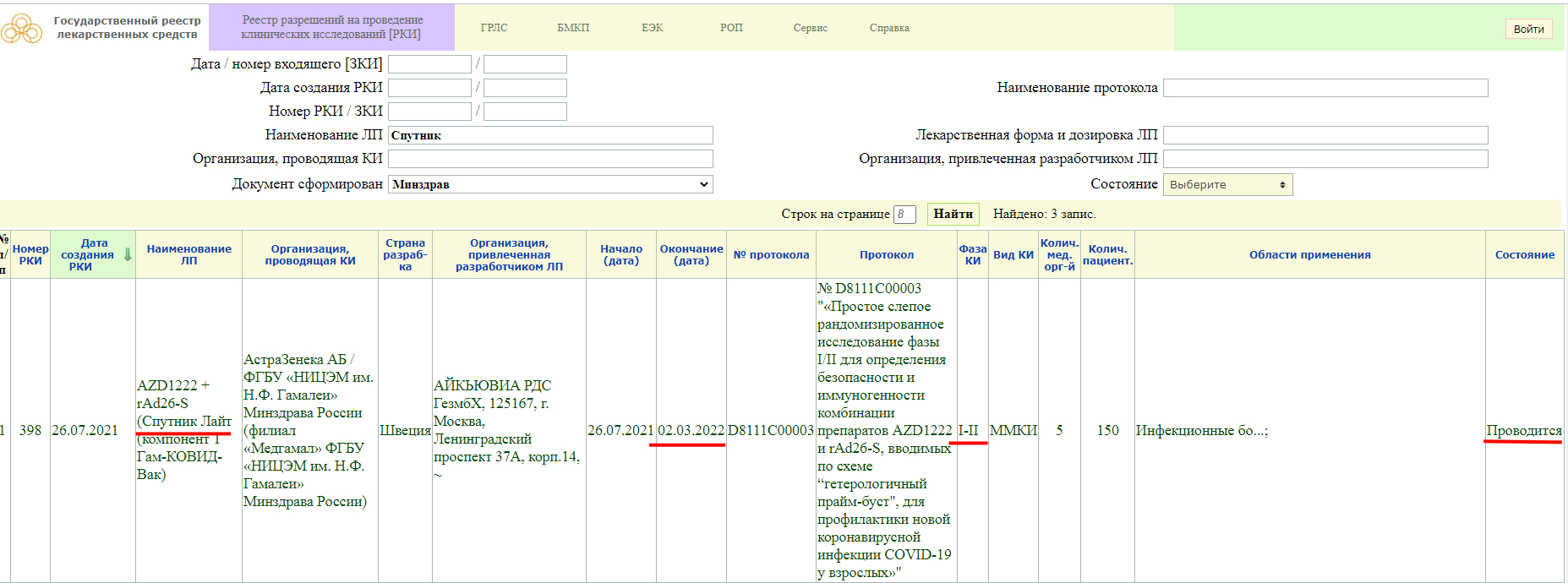
Как мы видим, в настоящий момент, у «Спутника Лайт» проводится фаза клинического исследования 1-2, и завершится она 2 марта 2022 года. Кстати обратите внимание, страна разработки Швеция.
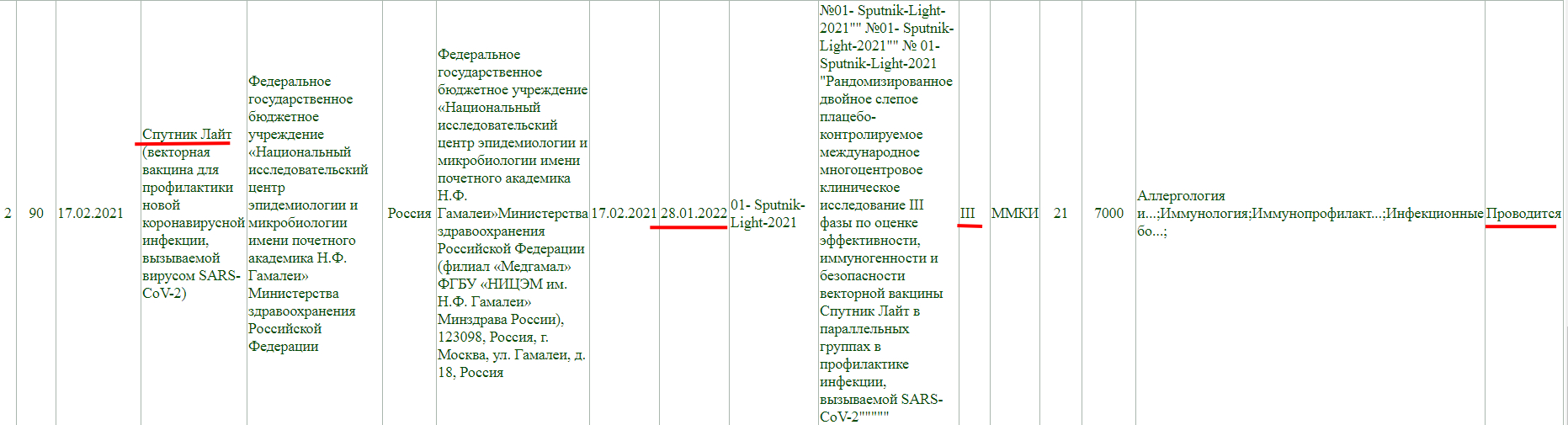
Так же, проводится фаза клинического исследования 3, и завершится она 28 января 2022 года.
Фаза клинического исследования 1-2, проводится до 31 декабря 2021 года.
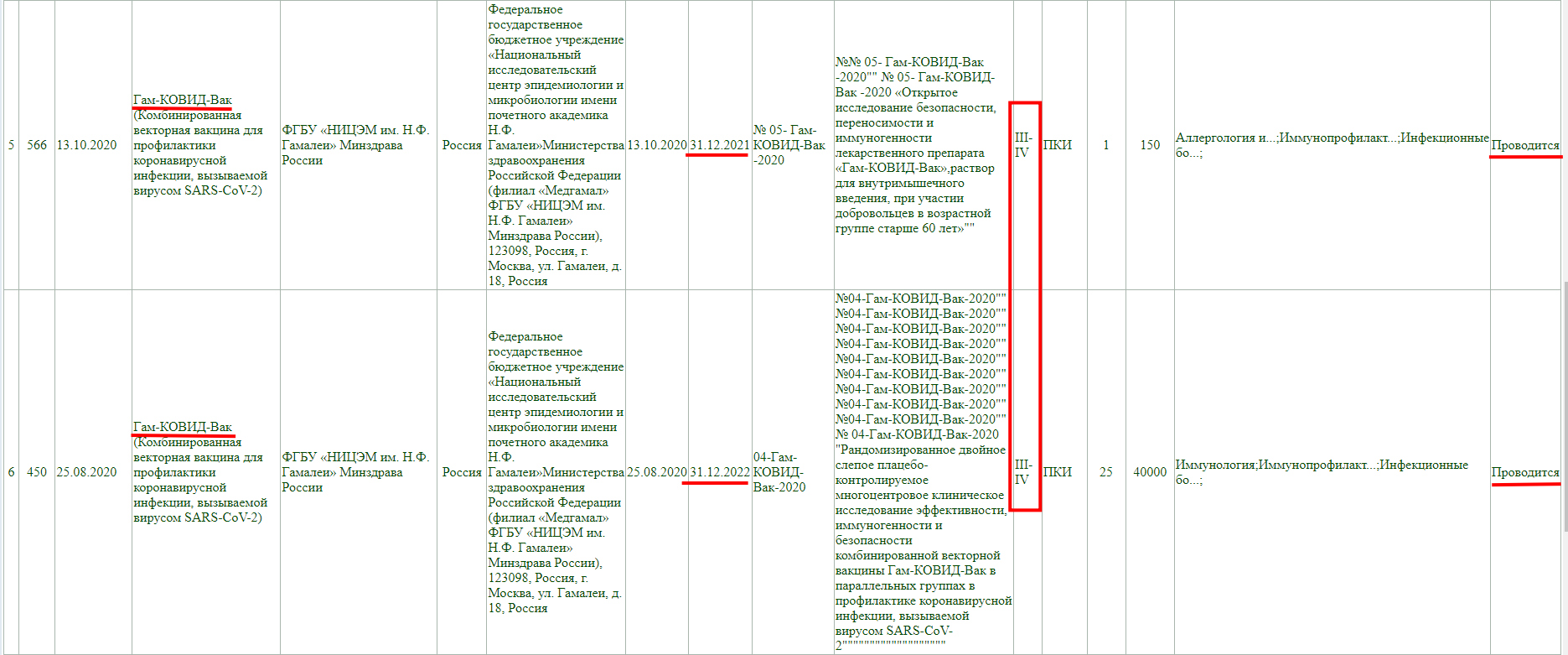
Как и у остальных, клинические исследования не завершены, и в настоящий момент проводится фаза 3 с участием добровольцев от 18 до 60 лет, а завершится она 30 декабря 2022 года.
Тут аналогично, клинические исследования не завершены, проводится фаза 3-4, и завершится она 30 декабря 2022 года.
А тут клиническое исследование завершено, но только фазы 1-2.
Кроме того, отсутствие данных о клинических испытаниях вакцины «Спутник V» необходимых для ее регистрации в Европе, 15 мая 2021 года, уже сообщало одно из крупнейших в мире международных агентств новостей и финансовой информации, Reuters.
И в завершение, по данным ВОЗ на 14 марта 2021 г., российские вакцины против COVID-19, в перечне безопасных и эффективных, отсутствуют.
Минздрав изменил рекомендации для вакцины «Спутник Лайт»: ее будут использовать только для ревакцинации
Если население мира не будет прививаться, появятся новые виды более опасных штаммов вируса
В России начинаются нерабочие дни для сдерживания заболеваемости COVID-19
Евгений Сатановский: у России хватает всего для уничтожения США, а по мелочам разбирается Мария Захарова
На селекторном совещании в Минобороны РФ снова обсуждали коронавирус
Российские вакцины не прошли все фазы клинического исследования?
В России за сутки скончались 1 160 человек с COVID-19
МВД потребовало, чтобы нелегальные мигранты покинули Россию до 15 июня
Глава Крыма Аксёнов: «Сам получу сертификат фармацевта, надоело враньё»
Как в России наказывали сотрудников магазинов и врачей за нарушения санитарного режима
Как в России наказывали сотрудников магазинов и врачей за нарушения санитарного режима
Станьте членом КЛАНА и каждый вторник вы будете получать свежий номер «Аргументы Недели», со скидкой более чем 70%, вместе с эксклюзивными материалами, не вошедшими в полосы газеты. Получите премиум доступ к библиотеке интереснейших и популярных книг, а также архиву более чем 700 вышедших номеров БЕСПЛАТНО. В дополнение у вас появится возможность целый год пользоваться бесплатными юридическими консультациями наших экспертов.
В России завершилась третья фаза испытаний «Спутник V»
Московский Центр им. Гамалеи завершил третью фазу испытаний вакцины от коронавируса «Спутник V», в котором в том числе участвовали пожилые люди. Об этом на заседании президиума координационного совета при правительстве по борьбе c коронавирусом заявил министр здравоохранения Михаил Мурашко.
«Мы проводили III фазу клинического исследования вакцины «Гам-КОВИД-Вак», или «Спутник V», которая завершилась с участием пациентов старше 60 лет», — сказал он.
Мурашко сообщил, что испытания показали высокую эффективность и безопасность вакцины, готовится итоговый отчет. «Получив уже новые данные о больших, даже огромных объемах исследования, в котором были задействованы более 23 тыс. человек, фактически мы видим хороший профиль безопасности, и институт Гамалеи разрабатывает новые показания для вакцинации и использования вакцины», — сказал министр.
Минздрав выдал разрешение на проведение III и IV фазы постклинических исследований «Спутника V» в августе. Они начались 25 августа и должны закончиться в декабре 2022 года, в них примут участие 40 тыс. человек. Около 10 тыс. добровольцев должны получить не препарат, а плацебо — вещество без явных лечебных свойств, говорил глава Центра им. Гамалеи Александр Гинцбург.
Российскую вакцину «Спутник V» зарегистрировали в России 11 августа 2020 года. Она стала первым в мире зарегистрированным препаратом от COVID-19. Применение этой вакцины для пожилых Минздрав одобрил в конце декабря.
Клинические испытания
Клинические испытания
Прежде чем приступать к клиническим испытаниям, вакцина прошла в полном объеме все стадии доклинических испытаний по эффективности и безопасности, которые включали эксперименты на различных видах лабораторных животных, в том числе на 2-х видах приматов.
Фаза 1 и 2 клинических испытаний вакцины были завершены 1 августа 2020 года. Все добровольцы хорошо перенесли испытания, не было зарегистрировано непредвиденных и серьезных нежелательных явлений, вакцина индуцировала формирование высокого как антительного, так и клеточного иммунного ответа. Ни один участник нынешнего клинического испытания не заразился коронавирусом после введения вакцины. Высокая эффективность вакцины была подтверждена высокоточными тестами на антитела в сыворотках крови добровольцев (в том числе проводили анализ на антитела, которые нейтрализуют коронавирус), а также способностью иммунных клеток добровольцев активироваться в ответ на S белок шипа коронавируса, что говорит о формировании и антительного и клеточного иммунного ответа в результате вакцинации.
Пострегистрационные клинические исследования с участием более 31 000 человек в России и Беларуси начались 25 августа 2020 года. Ряд стран, таких как ОАЭ, Индия и Венесуэла, начали местные клинические исследования вакцины «Спутник V». Вакцина получила регистрационное свидетельство Минздрава России 11 августа и в соответствии с правилами в связи с чрезвычайной ситуацией, принятыми во время пандемии COVID-19, может использоваться для вакцинации населения в России.
В ходе клинических испытаний фазы III вакцины «Спутник V» продемонстрировал высокую эффективность, иммуногенность и безопасность.
«Спутник V» обеспечивает полную защиту от клинических случаев тяжелой степени COVID-19 «Спутник V» гарантирует устойчивый гуморальный (выработка антител, являющихся первой линией защиты) и клеточный (долгосрочная защита) иммунный ответ.
Результаты клинических испытаний фазы III подтвердили высокий уровень безопасности и иммуногенности вакцины «Спутник V», в том числе для пожилых людей.
По результатам анализа 3,8 млн вакцинированных россиян эффективность вакцины «Спутник V» составила 97,6%.
Активное вещество вакцины Спутник V и способ его использования имеет патентную защиту на территории России, которая принадлежит Национальному исследовательскому центру эпидемиологии и микробиологии имени почетного академика Н. Ф. Гамалеи.
Опубликованы результаты третьей фазы испытаний вакцины «Спутник»
Российские исследователи из Центра Гамалеи выпустили отчет о третьей фазе клинических испытаний коронавирусной вакцины ГамКовидВак («Спутник-V»). По результатам испытаний на 19 866 добровольцах, из которых 14 964 получили вакцину, а 4902 — плацебо, эффективность «Спутника» составила 91,6 процента. Никаких опасных для жизни побочных эффектов организаторы испытаний не заметили. Они зафиксировали несколько смертей, однако сочли, что их причины не связаны с вакцинацией. Вакцина также оказалась эффективна на выборке пожилых (60-87 лет) добровольцев. Далее разработчики планируют проверять препарат на детях и подростках. Исследование опубликовано в журнале The Lancet.
Коронавирусная вакцина, разработанная Центром Гамалеи, получила регистрацию в России еще в августе 2020 года. Тогда предполагалось, что ее можно будет использовать для расширенных клинических испытаний — в них планировали набрать около сорока тысяч человек. Однако кампания по вакцинации в России началась в декабре 2020 года, когда третья фаза испытаний не была закончена. Все, что было известно, к тому моменту — промежуточные показатели эффективности вакцины, которые разработчики оценили сначала в 92, а потом в 91,4 процента (о том, как их считают и какие выводы из этого можно сделать, мы писали в материале «Магия чисел»).
Сейчас исследователи из Центра Гамалеи впервые опубликовали подробный отчет о третьей фазе испытаний. В аналитическую выборку вошли данные о добровольцах, которые получили обе дозы вакцины к 24 ноября 2020 года. Их оказалось 19 866: из них 14 964 досталась настоящая вакцина, а 4902 — плацебо, роль которого выполнял буферный раствор (в него вошли все ингредиенты «Спутника», кроме непосредственно аденовирусного вектора). Всего в рамках клинических испытаний инъекции должны получить около 33 тысяч человек, итоги по полной выборке исследователи планируют подвести позднее.
Всех участников испытаний исследователи проверяли перед первой инъекцией — на отсутствие вирусной РНК на слизистой (методом ПЦР), антител к коронавирусу в крови, а также тяжелых болезней крови и сердца, ВИЧ, гепатита и алкогольной зависимости. Беременные и кормящие женщины, а также несовершеннолетние в испытаниях не участвовали. Средний возраст участников составил 45,3 года, при этом мужчин как в группе плацебо, так и в группе вакцины было больше, чем женщин (61 процент против 39).
После первой инъекции добровольцев просили вести электронные дневники здоровья, отвечать на регулярный обзвон врачей и сообщать им обо всех побочных эффектах и подозрительных симптомах, которые могли быть признаком COVID-19. Кроме того, перед второй инъекцией все участники проходили еще один ПЦР-тест.
На 24 ноября исследователи зафиксировали 175 случаев заболевания ковидом (79 в группе вакцины и 96 в группе плацебо) после первой инъекции. Из 175 66 возникли в первые две недели после прививки — то есть до того, как успевает сформироваться иммунологическая память. Еще 31 доброволец заболел в последнюю неделю перед второй инъекцией. На основании этих данных исследователи подсчитали, что эффективность первой дозы самой по себе составляет 73-86 процента. Несмотря на то, что они не планируют сокращать график инъекций, эти данные могут служить подспорьем для клинических испытаний вакцины «Спутник-лайт», состоящей из единственного укола.
После второй инъекции исследователи зафиксировали еще 78 случаев ковида: 16 (0,1 процента) в группе вакцины и 62 (1,3 процента) — в группе плацебо. Это соответствует средней эффективности в 91,6 процента (p
Случаи заболевания COVID-19 в группе плацебо (красный) и вакцины (синий)
Lancet опубликовал результаты третьей фазы испытаний «Спутника V». Главные выводы
Автор фото, Artem Geodakyan/TASS
Авторитетный научный журнал Lancet опубликовал результаты третьей фазы клинических испытаний российской вакцины «Спутник V», разработанной исследовательским Центром имени Гамалеи.
Согласно предварительным данным, эффективность вакцины против заражения коронавирусом SARS-CoV-2 составила 91,6%. Как подчеркивают ученые, такая же эффективность была и в группе людей старше 60 лет. Как заявил на брифинге, посвященном публикации, глава центра Гамалеи Александр Гинцбург, ученые пришли к выводу, что иммунитет после «Спутника» может сохраняться «по крайней мере два года и более».
По словам главы РФПИ Кирилла Дмитриева, вакцина эффективна против обнаруженных в Великобритании и ЮАР новых штаммов коронавируса.
По данным исследователей, «Спутник» «на 100% защищает» от среднего и тяжелого течения Covid-19. Во время исследования было несколько смертей добровольцев, но с введением вакцины они не связаны, говорится в статье Lancet.
Эффективность
Согласно промежуточным результатам исследования, проведенного на 20 тысячах человек, вакцина показала эффективность 91,6% против Covid-19.
ПЦР-тесты на коронавирус исследуемым проводили при первичном скрининге и перед введением второй дозы, сообщается в статье. Тест также проводили, если участники сообщали о симптомах ОРВИ.
В рамках вторичного анализа авторы разграничивали исследование эффективности вакцины против среднего или тяжелого течения Covid-19. Сообщается, что через 21 день после первой дозы не наблюдалось случаев среднего или тяжелого течения заболевания в группе вакцинированных и 20 случаев наблюдалось в группе плацебо, что эквивалентно 100-процентной эффективности против среднего или тяжелого течения болезни.
Побочные эффекты
Большинство нежелательных побочных эффектов были легкими, включая симптомы гриппа, головную боль, боль в месте инъекции и астению (слабость или вялость).
Действие вакцины на людей старше 60
Автор фото, Reuters
Авторы отмечают, что, так как случаи болезни были обнаружены только тогда, когда участники самостоятельно сообщали о симптомах, анализ эффективности включает в себя лишь болезнь с ее симптоматическим проявлением, и необходимы дальнейшие исследования для понимания эффективности вакцины относительно бессимптомного Covid-19 и его передачи. Средний период наблюдения за участниками составлял 48 дней с момента первой дозы, поэтому исследование не может оценить полную продолжительность защиты, отмечается в статье.
Хотя формат исследования не позволяет оценить эффективность одократного введения вакцины, результаты говорят о том, что частично защита начинает работать уже через 16-18 дней после первой иммунизации, говорится в исследовании. С 15 по 21 день эффективность против среднего или тяжелого течения болезни составила 73,6%, но необходимы дальнейшие исследования, чтобы сделать какие-либо надежные выводы из этих наблюдений.
Аденовирусные векторные вакцины использовались ранее, и их безопасность подтверждена несколькими клиническими исследованиями, говорится в статье.