Гликолиз что образуется в результате
Процесс гликолиза его реакции, аэробный и анаэробный (Таблица, схема)
Аэробный процесс гликолиза (10 реакций), уравнение (с образованием пирувата):
Анаэробный процесс гликолиза (11 реакций), уравнение (с образованием лактата):
Схема процесса гликолиза и его реакции
Таблица процесс гликолиза его реакции
Для распада и частичного окисления молекулы глюкозы требуется протекание 11 сложных последовательных реакций.
Ферменты, Активаторы, ингибиторы
Подготовительная стадия гликолиза
Стадия активации глюкозы проходит в 5 реакций, в ходе которых 1 молекула гексозы (глюкозы) расщепляется на 2 молекулы триоз-глицеральдегидфосфата
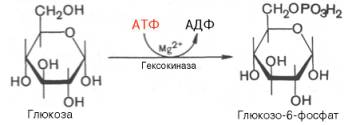
1. Необратимая реакция фосфорилирования глюкозы
Ингибиторы: глюкозо-6-Ф, фосфоенолпируват.
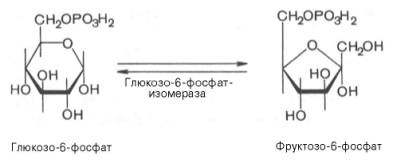
2. Обратимая реакция изомеризации глюкозо-6-фосфата
Во второй реакции происходит изомеризация (внутримолекулярные перестройки) глюкозо-6-фосфата во фруктозо-6-фосфат.
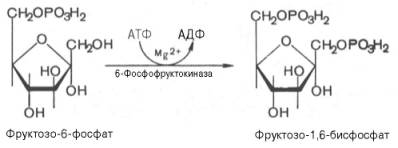
3. Необратимая реакция фосфорилирования фруктозо-6-фосфата (ключевая стадия гликолиза)
Ингибиторы: АТФ, цитрат, НАДН.
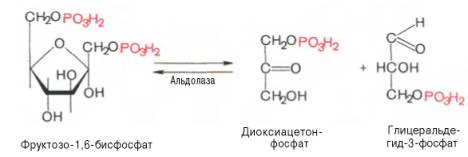
4. Обратимая реакция дихотомического расщепления фруктозо-1,6-дифосфата
В четвертой реакции гликолиза происходит расщепление фруктозо-1,6-дифосфата на две молекулы глицеральдегид-3-фосфата.
5. Обратимая реакция изомеризации дигидроксиацетона-3-фосфат в глицеральдегид-3-фосфат
В пятой реакции происходит изомеризация полученных триозофосфатов. На этом заканчивается первая стадия гликолиза.
Стадия генерации АТФ
Проходит в 6 реакций (или 5), в ходе которых энергия окислительных реакций трансформируется в химическую энергию АТФ (субстратное фосфорилирование).
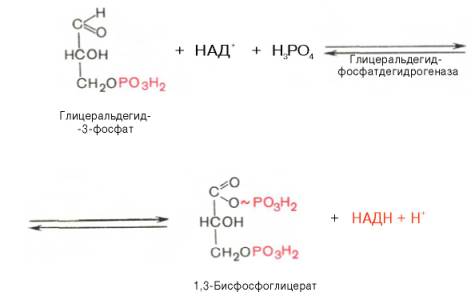
6. Окисление глицеральдегид-3-фосфата до 1,3-дифосфоглицерата (реакция гликолитической оксиредукции)
В шестой реакции происходит окисление альдегидной группы до карбоксильной. Выделившийся Н+ акцептируется NAD, который восстанавливается до NADH. Освобождающаяся энергия затрачивается для образования высокоэнергетической связи 1,3-бифосфоглицерата (1,3-бифосфоглицериновая кислота).
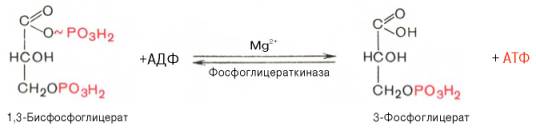
7. Субстратное фосфорилирование АДФ (7)
В седьмой реакции фосфорильная группа 1,3-бифосфоглицерата переносится на ADP, в результате чего образуется АТР (напоминаем, что следует иметь в виду две параллельные цепи реакций, с участием двух молекул триоз, образовавшихся из одной молекулы гексозы, следовательно, синтезируется не одна, а две молекулы АТР).
8. Реакция изомеризации 3-фосфоглицерата в 2-фосфоглицерат
В восьмой реакции гликолиза происходит перенос фосфатной группы с третьего атома углерода на второй. В результате образуется 2-фосфоглицерат (2-фосфоглицериновая кислота).
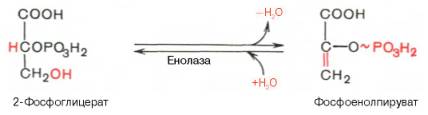
9. Реакция енолизации
Девятая реакция сопровождается внутримолекулярными окислительно-восстановительными процессами, в результате которых образуется фосфоенолпируват (фосфоенолпировиноградная кислота) с высокоэнергетической связью во втором атоме углерода и отщепляется молекула воды
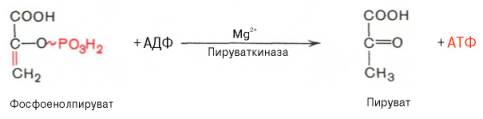
10. Реакция субстратного фосфорилирования
В ходе десятой реакции фосфорильная группа переносится на ADP. При этом синтезируется АТР и пируват (пировиноградная кислота). Эта реакция также необратима, поскольку высокоэкзергонична.
11. Реакция обратимого восстановления пировиноградной кислоты до молочной кислоты (в анаэробных условиях)
Если после гликолиза следует аэробное расщепление, пируват мигрирует в матрикс митохондрий, где, взаимодействуя с коэнзимом-А, участвует в образовании ацетил-СоА. В анаэробных условиях пируват при участии NADH восстанавливается до лактата (молочной кислоты), который при этом является конечным продуктом гликолиза. Затем в аэробных условиях лактат может обратно превратиться в пируват и окислиться в митохондриях.
_______________
Источник информации:
1. Биология для поступающих в вузы / Г.Л. Билич, В.А. Крыжановский. — 2008.
2. Биология в таблицах и схемах / Спб. — 2004.
ГЛИКОЛИЗ
Гликолиз (от греч. glycys – сладкий и lysis – растворение, распад) – это последовательность ферментативных реакций, приводящих к превращению глюкозы в пируват с одновременным образованием АТФ.
При аэробных условиях пируват проникает в митохондрии, где полностью окисляется до СО2 и Н2О. Если содержание кислорода недостаточно, как это может иметь место в активно сокращающейся мышце, пируват превращается в лактат.
Итак, гликолиз – не только главный путь утилизации глюкозы в клетках, но и уникальный путь, поскольку он может использовать кислород, если
последний доступен (аэробные условия), но может протекать и в отсутствие кислорода (анаэробные условия).
Анаэробный гликолиз – сложный ферментативный процесс распада глюкозы, протекающий в тканях человека и животных без потребления кислорода. Конечным продуктом гликолиза является молочная кислота. В процессе гликолиза образуется АТФ. Суммарное уравнение гликолиза можно представить следующим образом:
Последовательность реакций анаэробного гликолиза, так же как и их промежуточные продукты, хорошо изучена. Процесс гликолиза катализируется одиннадцатью ферментами, большинство из которых выделено в гомогенном, клисталлическом или высокоочищенном виде и свойства которых достаточно известны. Заметим, что гликолиз протекает в гиало-плазме (цитозоле) клетки.
Первой ферментативной реакцией гликолиза является фосфорилирование, т.е. перенос остатка ортофосфата на глюкозу за счет АТФ. Реакция катализируется ферментом гексокиназой:
Образование глюкозо-6-фосфата в гексокиназной реакции сопровождается освобождением значительного количества свободной энергии системы и может считаться практически необратимым процессом.
Наиболее важным свойством гексокиназы является ее ингибирование глюкозо-6-фосфатом, т.е. последний служит одновременно и продуктом реакции, и аллостерическим ингибитором.
Фермент гексокиназа способен катализировать фосфорилирование не только D-глюкозы, но и других гексоз, в частности D-фруктозы, D-маннозы и т.д. В печени, кроме гексокиназы, существует фермент глюкокиназа, который катализирует фосфорилирование только D-глюкозы. В мышечной ткани этот фермент отсутствует (подробнее см. главу 16).
Второй реакцией гликолиза является превращение глюкозо-6-фос-фата под действием фермента глюкозо-6-фосфатизомеразы во фруктозо-6-фосфат:
Эта реакция протекает легко в обоих направлениях, и для нее не требуется каких-либо кофакторов.
Третья реакция катализируется ферментом фосфофруктокиназой; образовавшийся фруктозо-6-фосфат вновь фосфорилируется за счет второй молекулы АТФ:
Данная реакция аналогично гексокиназной практически необратима, протекает в присутствии ионов магния и является наиболее медленно текущей реакцией гликолиза. Фактически эта реакция определяет скорость гликолиза в целом.
Четвертую реакцию гликолиза катализирует фермент альдолаза. Под влиянием этого фермента фруктозо-1,6-бисфосфат расщепляется на две фосфотриозы:
Эта реакция обратима. В зависимости от температуры равновесие устанавливается на различном уровне. При повышении температуры реакция сдвигается в сторону большего образования триозофосфатов (дигидро-ксиацетонфосфата и глицеральдегид-3-фосфата).
Пятая реакция – это реакция изомеризации триозофосфатов. Катализируется ферментом триозофосфатизомеразой:
Равновесие данной изомеразной реакции сдвинуто в сторону дигид-роксиацетонфосфата: 95% дигидроксиацетонфосфата и около 5% глице-ральдегид-3-фосфата. В последующие реакции гликолиза может непосредственно включаться только один из двух образующихся триозофосфатов, а именно глицеральдегид-3-фосфат. Вследствие этого по мере потребления в ходе дальнейших превращений альдегидной формы фосфотриозы ди-гидроксиацетонфосфат превращается в глицеральдегид-3-фосфат.
Образованием глицеральдегид-3-фосфата как бы завершается первая стадия гликолиза. Вторая стадия – наиболее сложная и важная. Она включает окислительно-восстановительную реакцию (реакция гликолитической оксидоредукции), сопряженную с субстратным фосфорилированием, в процессе которого образуется АТФ.
В результате шестой реакции глицеральдегид-3-фосфат в присутствии фермента глицеральдегидфосфатдегидрогеназы, кофермента НАД и неорганического фосфата подвергается своеобразному окислению с образованием 1,3-бисфосфоглицериновой кислоты и восстановленной формы НАД (НАДН). Эта реакция блокируется йод- или бромацетатом, протекает в несколько этапов:
1,3-Бисфосфоглицерат представляет собой высокоэнергетическое соединение (макроэргическая связь условно обозначена знаком «тильда»
). Механизм действия глицеральдегидфосфатдегидрогеназы сводится к следующему: в присутствии неорганического фосфата НАД + выступает как акцептор водорода, отщепляющегося от глицеральдегид-3-фосфата. В процессе образования НАДН глицеральдегид-3-фосфат связывается с молекулой фермента за счет SH-групп последнего. Образовавшаяся связь богата энергией, но она непрочная и расщепляется под влиянием неорганического фосфата, при этом образуется 1,3-бисфосфоглицериновая кислота.
Седьмая реакция катализируется фосфоглицераткиназой, при этом происходит передача богатого энергией фосфатного остатка (фосфатной группы в положении 1) на АДФ с образованием АТФ и 3-фосфогли-цериновой кислоты (3-фосфоглицерат):
Таким образом, благодаря действию двух ферментов (глицеральде-гидфосфатдегидрогеназы и фосфоглицераткиназы) энергия, высвобождающаяся при окислении альдегидной группы глицеральдегид-3-фосфата до карбоксильной группы, запасается в форме энергии АТФ. В отличие от окислительного фосфорилирования образование АТФ из высокоэнергетических соединений называется субстратным фосфорилированием.
Восьмая реакция сопровождается внутримолекулярным переносом оставшейся фосфатной группы, и 3-фосфоглицериновая кислота превращается в 2-фосфоглицериновую кислоту (2-фосфоглицерат).
Девятая реакция катализируется ферментом енолазой, при этом 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится высокоэргической:
Енолаза активируется двухвалентными катионами Mg 2+ или Мn 2+ и ингибируется фторидом.
Десятая реакция характеризуется разрывом высокоэргической связи и переносом фосфатного остатка от фосфоенолпирувата на АДФ (субстратное фосфорилирование). Катализируется ферментом пируваткиназой:
В результате одиннадцатой реакции происходит восстановление пировиноградной кислоты и образуется молочная кислота. Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАДН, образовавшегося в шестой реакции:
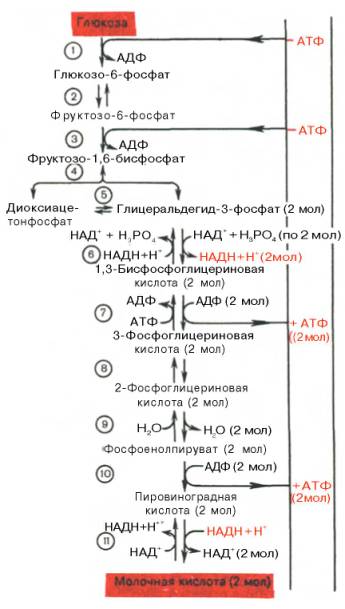
Последовательность протекающих при гликолизе реакций представлена на рис. 10.3.
Рис. 10.3. Последовательность реакций гликолиза.
Реакция восстановления пирувата завершает внутренний окислительно-восстановительный цикл гликолиза. НАД + при этом играет роль промежуточного переносчика водорода от глицеральдегид-3-фосфата (6-я реакция) на пировиноградную кислоту (11-я реакция), при этом сам он регенерируется и вновь может участвовать в циклическом процессе, получившем название гликолитический оксидоредукции.
Биологическое значение процесса гликолиза заключается прежде всего в образовании богатых энергией фосфорных соединений. На первых стадиях гликолиза затрачиваются 2 молекулы АТФ (гексокиназная и фосфофрук-токиназная реакции). На последующих образуются 4 молекулы АТФ (фосфоглицераткиназная и пируваткиназная реакции). Таким образом, энергетическая эффективность гликолиза в анаэробных условиях составляет 2 молекулы АТФ на одну молекулу глюкозы.
Как отмечалось, основной реакцией, лимитирующей скорость гликолиза, является фосфофруктокиназная. Вторая реакция, лимитирующая скорость и регулирующая гликолиз – гексокиназная реакция. Кроме того, контроль гликолиза осуществляется также ЛДГ и ее изоферментами.
В тканях с аэробным метаболизмом (ткани сердца, почек и др.) преобладают изоферменты ЛДГ1 и ЛДГ2 (см. главу 4). Эти изоферменты инги-бируются даже небольшими концентрациями пирувата, что препятствует образованию молочной кислоты и способствует более полному окислению пирувата (точнее, ацетил-КоА) в цикле трикарбоновых кислот.
В тканях человека, в значительной степени использующих энергию гликолиза (например, скелетные мышцы), главными изоферментами являются ЛДГ5 и ЛДГ4. Активность ЛДГ5 максимальна при тех концентрациях пирувата, которые ингибируют ЛДГ1. Преобладание изоферментов ЛДГ4 и ЛДГ5 обусловливает интенсивный анаэробный гликолиз с быстрым превращением пирувата в молочную кислоту.
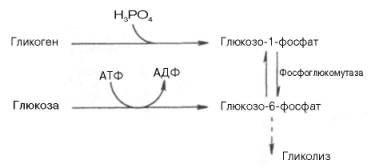
Как отмечалось, процесс анаэробного распада гликогена получил название гликогенолиза. Вовлечение D-глюкозных единиц гликогена в процесс гликолиза происходит при участии 2 ферментов – фосфорилазы а и фосфо-глюкомутазы. Образовавшийся в результате фосфоглюкомутазной реакции глюкозо-6-фосфат может включаться в процесс гликолиза. После образования глюкозо-6-фосфата дальнейшие пути гликолиза и гликогенолиза полностью совпадают:
В процессе гликогенолиза в виде макроэргических соединений накапливаются не две, а три молекулы АТФ (АТФ не тратится на образование глюкозо-6-фосфата). Кажется, что энергетическая эффективность глико-генолиза выглядит несколько более высокой по сравнению с процессом гликолиза, но эта эффективность реализуется только при наличии активной фосфорилазы а. Следует иметь в виду, что в процессе активации фосфо-рилазы b расходуется АТФ (см. рис. 10.2).
Гликолиз
Гликолиз (греч. glykys сладкий + lysis разрушение, распад)
ферментативный процесс анаэробного негидролитического расщепления углеводов (главным образом глюкозы) в клетках человека и животных, сопровождающийся синтезом аденозинтрифосфорной кислоты (АТФ), основного аккумулятора химической энергии в клетке, и заканчивающийся образованием молочной кислоты (лактата). У растений и микроорганизмов процессами, аналогичными Г., являются различные виды брожения (Брожение). Г. является наиболее важным анаэробным путем распада углеводов (Углеводы), играющим значительную роль в обмене веществ и энергии (Обмен веществ и энергии). В условиях недостаточности кислорода единственным процессом, поставляющим энергию для осуществления физиологических функций организма, оказывается Г., а в аэробных условиях Г. представляет первую стадию окислительного превращения глюкозы (Глюкоза) и других углеводов до конечных продуктов их распада — СО2 и Н2О (см. Дыхание тканевое). Интенсивный Г. происходит в скелетных мышцах, где он обеспечивает возможность развития максимальной активности мышечного сокращения в анаэробных условиях, а также в печени, сердце, головном мозге. Реакции Г. протекают в цитозоле.
Отдельные реакции и промежуточные продукты Г. хорошо изучены, а ферменты Г., обнаруживаемые у всех живых организмов, выделены в кристаллическом состоянии. Большинство реакций Г. обратимо, однако суммарный процесс сопровождается уменьшением свободной энергии и необратим: его равновесие смещено в сторону образования лактата.
На первой стадии Г. (табл., реакции 1—5) происходит фосфорилирование молекулы глюкозы (при этом расходуется энергия АТФ) и расщепление гексозы с образованием двух взаимопревращающихся триозофосфатов — диоксиацетонфосфата и глицеральдегид-3-фосфата. На первой стадии в Г. вовлекаются и другие простые сахара (как правило, путем превращения в глюкозо-6-фосфат), а также полисахариды. Образование фосфорных производных сахаров способствует превращению циклических форм сахаров в более реакционно-способные формы — ациклические. Гликолитическое расщепление Гликогена, осуществляемое главным образом в мышцах и печени, называется гликогенолизом. Первой реакцией гликогенолиза является фосфоролиз гликогена при участии фермента гликогенфосфорилазы с образованием глюкозо-1-фосфата, в реакции, катализируемой фосфоглюкомутазой, превращающегося в глюкозо-6-фосфат, который затем подвергается дальнейшим гликолитическим превращениям. У растений субстратом Г. может служить крахмал.
Реакции и ферменты гликолиза
Вторая стадия Г. (табл., реакции 6—11) является общей для всех сахаров, участвующих в Г., и состоит в превращении глицеральдегид-3-фосфата в лактат. Центральным звеном этой стадии является гликолитическая оксидоредукция, включающая окислительно-восстановительные реакции, сопряженные с аккумуляцией энергии в виде АТФ в процессе фосфорилирования аденозиндифосфорной кислоты (АДФ) на уровне субстрата. Энергия, высвобождающаяся в результате превращения глицеральдегид-3-фосфата в 3-фосфоглицерат (табл., реакции 6, 7), запасается в виде макроэргических фосфатных связей АТФ. Образование АТФ происходит также при разрыве макроэргической фосфатной связи фосфоенолпировиноградной кислоты (фосфоенолпирувата) и переносе фосфорильного остатка на АДФ. Внутренний окислительно-восстановительный цикл Г. завершается восстановлением пировиноградной кислоты или пирувата (α-кетопропионовой кислоты). Эта простейшая кетокислота занимает центральное место в превращении углеводов и участвует в обмене аминокислот (Аминокислоты) в качестве субстрата трансаминирования. В аэробных условиях пируват подвергается окислительному декарбоксилированию при участии пируватдегидрогеназного мультиферментного комплекса с образованием ацетил-кофермента А (ацетил-КоА); это превращение является одной из стадий тканевого дыхания, итогом которой служит включение углеводов в цикл трикарбоновых кислот в качестве энергетического субстрата. Ацетил-КоА участвует также в метаболизме липидов (см. Жировой обмен) и других физиологически важных соединений (например, ацетилхолина).
Завершающей реакцией Г. является катализируемое ферментом лактатдегидрогеназой (Лактатдегидрогеназа) превращение пирувата в лактат (α-оксипропионовую кислоту). Т.о., с учетом затрат АТФ на первой стадии Г. и образования АТФ на второй стадии балансовое уравнение гликолиза из глюкозы и гликогена — (глюкоза)n — выглядит следующим образом:
(глюкоза)n + 3Фнеорг. + 3АДФ = 2лактат + (глюкоза) n-1, где Фнеорг. — неорганический фосфат. При полном аэробном расщеплении одной молекулы глюкозы (через стадию образования ацетил-КоА из пирувата) образуется 38 молекул АТФ.
В процессе Г. происходят три практически необратимые реакции (табл., реакции 1, 3, 10), поэтому синтез глюкозы в гликолитическом пути невозможен. В связи с этим синтез глюкозы и других углеводов из неуглеводных предшественников (продуктов Г., аминокислот и других соединений), называемый глюконеогенезом (устаревшее реакция Пастера — Мейергофа), происходит в обход необратимых реакций Г. с использованием альтернативных, термодинамически благоприятных путей. Вследствие практической необратимости реакции, катализируемой пируваткиназой, фосфорилирование пирувата достигается за счет обходных реакций. Вначале происходит карбоксилирование пирувата в митохондрнях за счет энергии АТФ и при участии митохондриального фермента пируваткарбоксилазы Образовавшаяся щавелевоуксусная кислота (оксалоацетат), которая не способна проникать через мембрану митохондрий для участия в последующих реакциях глюконеогенеза, происходящих в цитозоле, восстанавливается с образованием яблочной кислоты (малата) за счет восстановительных эквивалентов НАД․Н в реакции, катализируемой митохондриальной малатдегидрогеназой. Малат диффундирует в цитозоль, где окисляется при участии НАД + и малатдегидрогеназы цитозоля с образованием внемитохондриального оксалоацетата. Последний подвергается декарбоксилированию и фосфорилированию при участии гуанозинтрифосфата (ГТФ) и фермента пируваткарбоксикиназы образованием фосфоенолпирувата. Т.о., на образование 1 молекулы фосфоенолпирувата из пирувата расходуется по 1 молекуле АТФ и ПФ. У некоторых животных, растений и микроорганизмов обнаружены альтернативные пути образования фосфоенолпирувата из пирувата, в частности прямой одностадийный процесс. В результате обращения реакций Г. 2 молекулы фосфоенолпирувата превращаются к 1 молекулу фруктозо-1,6-дифосфата, из которого в обход фосфофруктокиназной реакции Г., путем необратимого гидролиза фосфатной группы в положении 1 при участии фермента фруктозодифосфатазы образуется фруктозо-6-фосфат. Образующийся из него глюкозо-6-фосфат в обход гексокиназной реакции Г. дефосфорилируется с образованием свободной глюкозы при участии фермента глюкозо-6-фосфатазы или в результате фосфоглюкомутазной реакции превращается в глюкозо-1-фосфат — ключевое промежуточное соединение в биосинтезе моно- и дисахаридов, гликогена, крахмала, структурных полисахаридов. Балансовое уравнение образования глюкозы (глюконеогенеза) из пирувата выглядит следующим образом: 2пируват (СН3СОСООН) + 2НАД․Н + 2Н + + 4АТФ + 2ГТФ = глюкоза (С6Н12О6) + 2НАД + + 4АДФ +2ГДФ + 6Фнеорг.. Наряду с пируватом предшественниками глюкозы в глюконеогенезе могут быть любые соединения, превращающиеся в процессе катаболизма в пируват или в промежуточные продукты цикла трикарбоновых кислот (см. Обмен веществ и энергии), а также образующийся при гидролизе жиров глицерин.
Скорость Г. и ее координация со скоростями других метаболических процессов, в первую очередь глюконеогенеза и цикла трикарбоновых кислот, обеспечивается действием разнообразных регуляторных механизмов. Общая скорость Г. определяется доступностью субстрата, использованием АТФ и концентрацией ферментов Г. Существенную роль в регуляции скорости Г. на уровне ферментов играют приведенные выше три практически необратимые реакции Г. Наиболее важным лимитирующим скорость Г. ферментом является фосфофруктокиназа, активность которой ингибируется АТФ, НАД․Н, лимонной кислотой (цитратом) и жирными кислотами и стимулируется АДФ и АМФ, Активности гексокиназы и пируваткиназы также регулируются (по принципу обратной связи) АДФ, АТФ, промежуточными продуктами Г. и цикла трикарбоновых кислот. Основными пунктами контроля глюконеогенеза на уровне ферментов является регуляция реакций, катализируемых пируваткарбоксилазой (активация ацетил-КоА) и фруктозодифосфатазой (ингибирование АМФ и активация АТФ), т.е. глюконеогенез зависит от наличия избытка субстрата дыхания и энергии для синтеза глюкозы. У животных и человека в регуляции Г. принимают участие Гормоны. Так, Инсулин осуществляет контроль за Г. на генетическом уровне, являясь индуктором образования ключевых ферментов Г. (гексокиназы, фосфофруктокиназы, пируваткиназы) и репрессором синтеза ферментов глюконеогенеза. Противоположным действием обладают катехоламины, глюкагон, АКТГ (в печени) и паратгормон (в почках).
В клетке осуществляется тонкая регуляция окислительного и анаэробного обмена. Регуляторным механизмом поддержания энергетического баланса клеток за счет переключения их с Г., или брожения, на тканевое дыхание — более экономный путь получения энергии при расщеплении углеводов с использованием более разнообразных субстратов — является эффект Пастера, который заключается в снижении скорости или полном прекращении Г. в присутствии кислорода. Эффект Пастера типичен для факультативно анаэробных клеток, способных как к Г. (брожению), так и к дыханию, и наблюдается у многих микроорганизмов, растений и животных.
Интенсивность Г. в аэробных условиях (так называемого аэробного Г.) обычно невелика, и ее повышение обычно свидетельствует о нарушении клеточного метаболизма. В норме интенсивный аэробный Г. обнаружен в эритроцитах, где количество образующегося лактата в аэробных и анаэробных условиях почти одинаково, а также в эмбриональной, регенерирующей тканях и ткани некоторых злокачественных опухолей. В клетках злокачественных опухолей наблюдается эффект Пастера, но в аэробных условиях образование лактата в них подавляется не полностью; интенсивность аэробного Г. в опухолевых клетках значительна (на счет аэробного Г. относят до 50% образующейся энергии). Результатом эффекта Пастера является резкое снижение скорости потребления глюкозы и отсутствие накопления лактата, поскольку образующийся в процессе гликолиза НАД-Н окисляется не пируватом, а с помощью так называемого глицерофосфатного челночного механизма (глицерол-3-фосфат — диоксиацетонфосфат) и ферментов дыхательной цепи переноса электронов. В опухолевых клетках накопление лактата происходит и в аэробных условиях, несмотря на нормальное функционирование цикла трикарбоновых кислот и дыхательной цепи, что обусловлено снижением активности цитоплазматической глицерол-3-фосфатдегидрогеназы и неэффективностью функционирования глицерофосфатного челночного механизма.
Механизмы эффекта Пастера до конца не выяснены. Установлено, что угнетение Г. осуществляется под действием дыхания, сопряженного с окислительным фосфорилированием. К основным механизмам эффекта Пастера относят ингибирование фосфофруктокиназы продуктами аэробною окисления (АТФ, цитратом), конкуренцию между Г. и дыханием за АДФ и неорганический фосфат, используемых для синтеза АТФ. В клетках, характеризующихся высоким уровнем аэробного Г. (например, в опухолевых клетках), наблюдают «обратный эффект Пастера», или эффект Крабтри, — торможение дыхания глюкозой. При этом дефицит образования АТФ количественно восполняется за счет Г.
Клинические признаки преобладания Г. над аэробным распадом углеводов наблюдаются при гипоксических состояниях, обусловленных нарушениями кровообращения и дыхания, высотной болезнью, анемией, наркозом, тяжелой физической нагрузкой, местным нарушением кровообращения, снижением активности тканевых окислительных ферментов, при некоторых инфекционных болезнях и интоксикациях, гиповитаминозах, сахарном диабете, поражениях паренхимы печени.
Для характеристики интенсивности протекания Г. используют определение концентрации в биологическом материале продуктов Г. пирувата и лактата, а также определение активности ферментов Г., например лактатдегидрогеназы.
При некоторых физиологических и патологических состояниях отмечают изменение содержания пирувата в биологических жидкостях и тканях человека. В крови здоровых людей, главным образом в форменных элементах, содержится 0,5—1 мг/100 мл пирувата. Содержание пирувата в моче в норме составляет 2 мг/100 мл, суточное выведение его с мочой — 10—25 мг. Накопление пирувата происходит после массивной нагрузки организма глюкозой, при гипоксии, тяжелой мышечной работе. Повышение содержания пирувата в крови (пируватемия) наблюдают при гиповитаминозе В1 тяжелой сердечной недостаточности, ревмокардите, болезнях печени и почек, заболеваниях легких, инфекционных болезнях, злокачественных новообразованиях, сахарном диабете, интоксикациях и др. При тяжелой почечной недостаточности и в ряде других случаев повышается выведение пирувата с мочой. Количественное определение пирувата проводят обычно колориметрическими методами, основанными на его взаимодействии с нитропруссидом натрия, α- или β-нафтолом, 2,4-динитрофенилгидразином, салициловым альдегидом и др. Наиболее чувствительным является ферментативный метод определения пирувата по его восстановлению в присутствии НАД․Н и фермента лактатдегидрогеназы с регистрацией скорости окисления НАД․Н спектрометрически при длине волны 340 нм.
Содержание лактата в крови человека в норме должно быть ниже 1 ммоль/л. Оно возрастает при патологических состояниях, сопровождающихся усилением мышечных сокращений (эпилепсии, столбняке, тетании и др.), гипоксических состояниях (сердечной или легочной недостаточности, анемии и др.), злокачественных новообразованиях, острым гепатите, интоксикациях, сахарном диабете в стадии декомпенсации. Повышение концентрации лактата в крови, как правило, связано с усилением его образования в мышцах и уменьшением превращения глюкозы в гликоген в печени. При интенсивной мышечной работе содержание лактата в крови может возрастать в 5—10 раз. Наследственно обусловленное накопление лактата в крови (лактацидоз) проявляется у детей раннего возраста клинической картиной ацидоза, выраженными дыхательными нарушениями. У больных детей отмечают задержку психомоторного развития, мышечную гипотонию, однако с возрастом часто наступает улучшение.
Образование лактата в организме тесно связано с образованием пирувата. Их количественное соотношение характеризует соотношение гликолитического и окислительного превращений углеводов. В крови здоровых людей величина отношения пируват/лактат в среднем равна 10 (9,3—14,3), а ее изменение свидетельствует о нарушении нормального метаболизма.
Для определения лактата в крови используют ряд колориметрических методов. Наиболее широко в исследовании нарушений углеводного метаболизма применяют метод Баркера — Саммерсона, основанный на том, что из лактата в присутствии серной, фосфорной кислот и солей меди образуется уксусный альдегид, который реагирует с n-оксидифенилом с образованием окрашенного в фиолетовый цвет соединения. Интенсивность окраски пропорциональна концентрации лактата в пробе. Наиболее точным и чувствительным методом определения лактата является ферментативный метод, основанный на дегидрировании лактата в присутствии лактатдегидрогеназы и НАД со спектрофотометрической регистрацией количества образовавшегося НАД․Н.
Библиогр.: Рахимов К.Р. и Демидова А.И. Углеводы и механизмы их усвоения, Ташкент, 1986; Уайт А. и др. Основы биохимии, пер. с англ., т. 2, М., 1981.
Гликолиз (глико- (Глик-) + греч. lysis распад, разрушение, растворение)
ферментативный процесс расщепления глюкозы, протекающий без потребления кислорода, приводящий к образованию молочной кислоты и сопровождающийся образованием АТФ; Г. является источником энергии в анаэробных условиях, например в работающей скелетной мышце.