Гипопротеинемия что это такое
Нарушение белкового обмена
Белок имеет важную функцию в организме, так как является пластическим материалом, из которого идет строительство клеток, тканей и органов организма человека. Помимо этого, белок – основа гормонов, ферментов и антител, которые выполняют функции роста организмы и защищают его от воздействия негативных факторов окружающей среды. При нормальном обмене белка в организме, у человека высокий иммунитет, отличная память и выносливость. Белки влияют на полноценный обмен витаминов и минеральных солей. Энергетическая ценность 1 г белка составляет 4 ккал (16,7 кДж).
При недостатке белков в организме возникают серьезные нарушения: замедление роста и развития детей, изменения в печени взрослых, деятельности желез внутренней секреции, состава крови, ослабление умственной деятельности, снижение работоспособности и сопротивляемости к инфекционным заболеваниям.
Белковый обмен играет важную роль в процессе жизнедеятельности организма. Нарушение белкового обмена вызывает снижение активности, также понижается сопротивляемость к инфекциям. При недостаточном количестве белков в детском организме – возникает замедление роста, а также снижение концентрации. Необходимо понимать, что нарушения возможны на разных этапах синтеза белка, но все они опасны для здоровья и полноценного развития организма.
Этапы синтеза белков:
На всех этапах могут существовать нарушения, которые имеют свои особенности. Рассмотрим их детальнее.
Первый этап: Всасывание и синтез
Основное количество белков человек получает из пищи. Поэтому при нарушении переваривания и всасывания развивается белковая недостаточность. Для нормального синтеза белков необходимо правильное функционирование системы синтеза. Нарушения этого процесса могут быть приобретенными или наследственными. Также уменьшение количества синтезируемого белка может быть связано с проблемами в работе иммунной системы. Важно знать, что нарушения в процессе всасывания белков приводит к алиментарной недостаточности (дистрофия тканей кишечника, голодание, несбалансированный состав пищи по аминокислотной составляющей). Также нарушение процессов синтезирования белков чаще всего ведут к изменению количества синтезированного белка или к образованию белка с измененной молекулярной структурой. В результате происходят гормональные изменения, дисфункция нервной и иммунной системы, также возможны геномные ошибки.
Второй этап: Обмен аминокислот
Нарушения обмена аминокислот также могут быть связаны с наследственными факторами. Проблемы на этом этапе чаще всего проявляются в нехватке тирозина. Это, в частности, провоцирует врожденный альбинизм. Более страшное заболевание, спровоцированное нехваткой тирозина в организме – наследственная тирозенемия. Хроническая форма заболевания сопровождается частой рвотой, общей слабостью, болезненной худобой (вплоть до возникновения анорексии). Лечение состоит в соблюдении специальной диеты с высоким содержание витамина D. Нарушения обмена аминокислот приводятк дисбалансу процессов трансаминирования (образования) и окислительного разрушения аминокислот. Влиять на негативное развитие этого процесса может голодание, беременность, заболевания печени, а также инфаркт миокарда.
Третий этап: конечный обмен
При конечных этапах белкового обмена, может возникнуть патология процесса образования азотистых продуктов и их конечного выведения с организма. Подобные нарушения наблюдаются при гипоксии (кислородном голодании организма). Также следует обращать внимание на такой фактор, как белковый состав крови. Нарушение содержания белков в плазме крови может указывать на проблемы с печенью. Также катализатором развития болезни могут быть проблемы с почками, гипоксия, лейкоз. Восстановлением белкового обмена занимается терапевт, а также врач-диетолог.
Симптомы нарушения белкового обмена
При большом наличии белка в организме, может быть его переизбыток. Это связано в первую очередь с неправильным питанием, когда рацион больного почти полностью состоит из белковых продуктов. Врачи выделяют следующие симптомы:
Избыток белка также может привести к подагре и ожирению. Фактором риска при возникновения подагры может быть чрезмерное употребление в пищу большого количества мяса, особенно с вином и пивом. Подагрой чаще болеют мужчины пожилого возраста, для которых характерна возрастная гиперурикемия.
Симптомы подагры:
Симптомы ожирения:
При наличии вышеуказанных проблем, необходимо снизить потребление белковых продуктов, пить больше чистой воды, заниматься спортом. Если же организму наоборот не хватает белков для синтеза, он реагирует на ситуацию следующим образом: возникает общая сонливость, резкое похудание, общая мышечная слабость и снижение интеллекта. Отметим, что в «группу риска» попадают вегетарианцы и веганы, которые по этическим причинам не употребляют животный белок. Людям, которые придерживаться подобного стиля питания, необходимо дополнительно принимать внутрь витаминные комплексы. Особенно обратить внимание на витамин B12 и D3.
Наследственные нарушения обмена аминокислот
Важно знать, что при наследственном нарушении синтеза ферментов, соответствующая аминокислота не включается в метаболизм, а накапливается в организме и появляется в биологических средах: моче, кале, поте, цереброспинальной жидкости. Если смотреть на клиническую картину проявления этого заболевания, то она определяется в первую очередь появлением большого колличества вещества, которое должно было метаболизироваться при участии заблокированного фермента, а также дефицитом вещества, которое должно было образоваться.
Нарушения обмена тирозина
Нарушения белкового состава крови
Также стоит упомянуть о нарушениях белкового состава в крови. Изменения в количественном и качественном соотношении белков крови наблюдаются почти при всех патологических состояниях, которые поражают организм в целом, а также при врожденных аномалиях синтеза белков. Нарушение содержания белков плазмы крови может выражаться изменением общего количества белков (гипопротеинемия, гиперпротеинемия) или соотношения между отдельными белковыми фракциями (диспротеинемия) при нормальном общем содержании белков.
Гипопротеинемия возникает из-за снижения количества альбуминов и может быть приобретенной (при голодании, заболеваниях печени, нарушении всасывания белков) и наследственной. К гипопротеинемии может привести также выход белков из кровеносного русла (кровопотеря, плазмопотеря) и потеря белков с мочой.
Гипопротеинемия что это такое
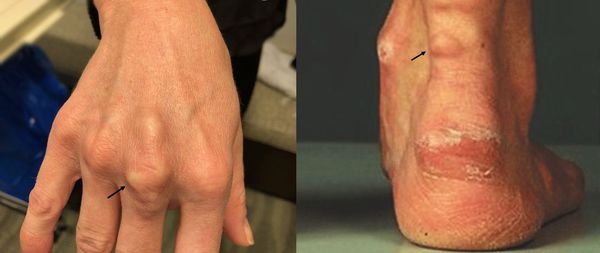
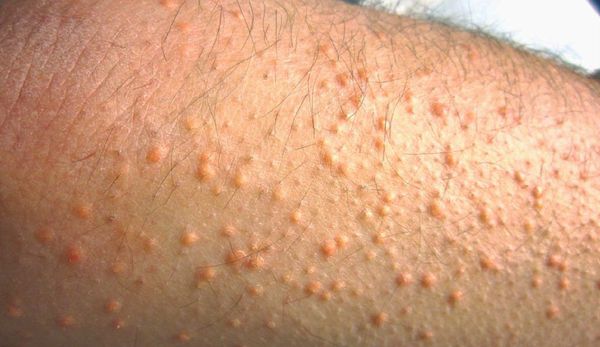
Белковая недостаточность представляет собой болезненное состояние организма, связанное с недостаточным поступлением и усвоением белка либо с его усиленным распадом. Истинный дефицит поступления белков с пищей может развиваться у лиц, длительное время недоедающих, придерживающихся так называемых монодиет, или у вегетарианцев. Вторичный дефицит белка, связанный с его усиленным распадом, может сопровождать целый ряд заболеваний, например тяжелые формы инфекционных заболеваний, ожоги, патологии почек, наследственные нарушения обмена веществ. Белки являются основным строительным материалом организма, поэтому даже легкие формы белковой недостаточности, внешне протекающие бессимптомно, влияют на способность противостоять инфекции или на скорость заживления ран, замедляют рост ногтей и волос, вызывают сухость кожи. Тяжелая белковая недостаточность может нарушить нормальную работу всех органов и систем. Особенно опасен дефицит белка в детском возрасте, так как он способен повлиять на развитие умственных способностей, формирование мышц, замедлить рост ребенка.
Своевременное выявление белковой недостаточности и установление ее причины крайне важно, так как позволяет избежать опасных для жизни осложнений.
Дефицит белка, белковая дистрофия, белково-энергетическая недостаточность.
Легкие формы белковой недостаточности чаще всего протекают бессимптомно. Исключение могут составлять наследственно обусловленные дефициты отдельных аминокислот (структурных компонентов молекулы белка), характерные признаки которых наблюдаются в раннем детском возрасте.
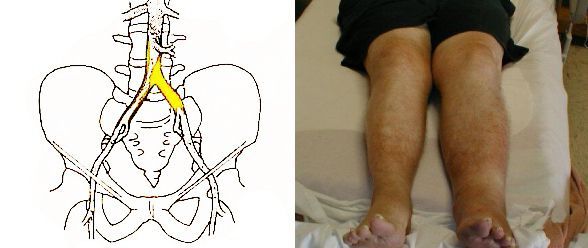
Внешние проявления дефицита белка:
Проявления со стороны нервной системы:
Проявления со стороны костно-мышечной системы:
Со стороны органов пищеварения:
Кто в группе риска?
Общая информация о заболевании
Белки относятся к числу основных питательных веществ, выполняющих в организме следующие функции.
Реализация этих функций происходит за счет белкового обмена – постоянно протекающих процессов образования (синтеза) и распада белка.
Основные причины белковой недостаточности:
В зависимости от степени выраженности недостаток белка может приводить к:
Белковая недостаточность в первую очередь может быть заподозрена у пациентов с дефицитом массы тела, а также у лиц с симптомами заболеваний, для которых характерен дефицит белков. Для подтверждения диагноза проводится комплекс исследований.
Дополнительные (инструментальные) методы исследования
Объем диагностических исследований зависит от предполагаемой причины белковой недостаточности и должен определяться лечащим врачом. К числу основных методов диагностики относятся:
Лечение белковой недостаточности направлено на восполнение объема белка и нормализацию белкового обмена. Одновременно лечится основное заболевание.
Оно может включать в себя следующие пункты.
Гиперпротеинемия
Гиперпротеинемия – это увеличение концентрации общего белка в плазме крови более 84 г/л. Данное состояние может развиться вследствие широкого спектра причин – от обильного потоотделения и беременности до различных воспалительных заболеваний и злокачественных новообразований. Само по себе высокое содержание белка не имеет клинических признаков, за исключением моноклональных гаммапатий, при которых гиперпротеинемия является ключевым патогенетическим звеном синдрома гипервязкости крови (СГВ). Уровень белка исследуется в плазме натощак. Для коррекции данного расстройства необходима терапия основного заболевания.
Классификация
Высокая концентрация белка может наблюдаться и у абсолютно здоровых людей (физиологическая гиперпротеинемия). Такое происходит при беременности, взятие крови на анализ через 30 минут после длительного пребывания в горизонтальном положении. По этиопатогенезу различают 2 типа гиперпротеинемий:
Гиперпротеинемия может возникать за счет увеличения какой-либо белковой фракции. Выделяют:
Причины ложной гиперпротеинемии
Развитие данной разновидности гиперпротеинемии связано с увеличением относительного содержания белка из-за значительного уменьшения количества жидкости в крови. При этом гиперпродукция белка отсутствует. Типично для:
Степень гиперпротеинемии почти всегда умеренная и быстро регрессирует после коррекции водного дефицита.
Причины истинной гиперпротеинемии
Инфекции
Одна из наиболее распространенных причин данного состояния. При попадании инфекционного агента (бактерий, вирусов, паразитов) в организм человека происходит их фагоцитирование. В процессе фагоцитоза микроорганизмов лейкоциты начинают вырабатывать пептидные факторы и провоспалительные цитокины (интерлейкины, интерферон, фактор некроза опухолей).
Эти вещества в совокупности с активацией симпато-адреналовой системы стимулируют образование в печени белков острой фазы (С-реактивного белка, белков системы комплемента, серомукоидов) и иммуноглобулинов (антител) в B-лимфоцитах. Возрастание концентрации белка отмечается примерно через 5-6 часов после начала острого или обострения хронического инфекционного заболевания и достигает максимума через 48-72 часа.
Уровень гиперпротеинемии коррелирует с активностью патологического процесса, однако редко достигает больших значений (степень в основном умеренная). Показатели белка выше при бактериальных (пневмония, пиелонефрит) и паразитарных (малярия, трипаносомоз) инфекциях, а также при генерализованных инфекциях любой этиологии (сепсис). Концентрация протеина достаточно быстро нормализуется после стихания воспаления под влиянием специфической терапии.
Воспалительные заболевания
К данной группе преимущественно относятся патологии аутоиммунной природы – ревматоидный артрит, системные болезни соединительной ткани (СКВ, системная склеродермия), воспалительные заболевания кишечника (болезнь Крона, неспецифический язвенный колит). Точный патогенетический механизм гиперпротеинемии при хронических воспалительных аутоиммунных заболеваниях до сих пор неизвестен.
Предполагается, что под влиянием неизвестного этиологического фактора происходит усиленная выработка воспалительных белков (главным образом СРБ) и глобулинов (аутоантител) в рамках иммунной аутоагрессии. Гиперпротеинемия появляется только в период обострения заболевания, почти всегда незначительная или умеренная. После наступления рецидива гиперпротеинемия может сохраняться некоторое время (от нескольких дней до нескольких недель).
Моноклональные гаммапатии (парапротеинемии)
Эту группу заболеваний стоит подозревать при высокой и длительно сохраняющейся гиперпротеинемии. К ним относятся множественная миелома (миеломная болезнь Рустицкого-Каллера), макроглобулинемия Вальденстрема, болезнь легких цепей. В основе патогенеза лежит гиперпродукция опухолевыми плазматическими клетками белков-парапротеинов, аномальных по молекулярному строению и иммунологическим свойствам: макроглобулинов, моноклональных иммуноглобулинов, легких цепей каппа или лямбда.
Отличительной чертой данного вида гиперпротеинемии является то, что она служит не только диагностическим маркером, но и напрямую определяет степень тяжести болезни. Из-за особенностей физических свойств парапротеинов они в несколько раз повышают вязкость крови, что значительно нарушает кровообращение во всех органах и тканях, особенно в головном мозге.
Гиперпротеинемия при этих заболеваниях может привести к коматозному состоянию (парапротеинемическая кома). Концентрация белка нарастает медленно, в течение нескольких лет, параллельно опухолевой прогрессии. Уровень общего белка увеличивается примерно на 15-20%. Его снижение происходит только после удаления избытка паарпротеинов из системного кровотока с помощью экстракорпоральных методов очищения крови (плазмаферез).
Редкие причины
Диагностика
Сама по себе гиперпротеинемия представляет собой довольно редкое явление, поэтому ее обнаружение требует особого внимания и дифференциальной диагностики. При получении биохимического анализа крови с высоким содержанием белка сначала необходимо обратиться к врачу-терапевту. Важное значение имеют анамнестические данные: возраст пациента, диагностированные ранее хронические заболевания.
Уточняется, что предшествовало появлению высокого уровня протеина – обильное потоотделение, длительная диарея и т.д. Также при физикальном осмотре больного выясняется наличие тех или иных симптомов, что может помочь в установлении причины отклонения в анализах, например, лихорадка при инфекциях, боли в суставах при аутоиммунной ревматологической патологии, боли в костях и повторяющиеся носовые кровотечения при парапротеинемиях. Для выявления причины данного лабораторного феномена назначается следующее обследование:
Коррекция
Для борьбы с гиперпротеинемией необходимо лечение основного заболевания, на фоне которого она развилась. Физиологическая гиперпротеинемия не требует никакого вмешательства, так как не является признаком болезни или патологического состояния. Для коррекции гемоконцентрационной гиперпротеинемии достаточно устранить дефицит жидкости перорально либо внутривенным введением кристаллоидных растворов. В остальных случаях проводится следующие мероприятия:
Прогноз
Гиперпротеинемия в подавляющем большинстве случаев не несет никаких неблагоприятных последствий для пациента. Прогноз определяется тем заболеванием, которое послужило причиной развития этого лабораторного феномена. Исключением являются высокие показатели белка при моноклональных гаммапатиях, когда гиперпротеинемия может стать причиной коматозного состояния, трофических язв и гангрены конечностей, хронической почечной недостаточности. Поэтому любое превышение референсных значений белка, особенно высокое и стойкое, требует обращения к врачу.
Гипопротеинемия
Гипопротеинемия – это патологическое состояние, которое характеризуется снижением в плазме крови концентрации общего белка менее 64 г/л. Причинами выступает голодание, заболевания почек и печени. Клиническая картина может быть разнообразной – от бессимптомного течения до появления периферических отеков, выпота в брюшную, грудную, перикардиальную полости, повышенной восприимчивости к инфекциям. Уровень белка исследуется в плазме натощак. Для устранения гипопротеинемиии проводится компенсация дефицита белка и лечение основного заболевания.
Классификация
Низкое содержание белка может наблюдаться и у здоровых людей (физиологическая гипопротеинемия), например, у детей в возрасте до 3 месяцев или женщин в III триместре беременности. Также концентрация общего белка может оказаться сниженной при длительной госпитализации у лежачих больных. По происхождению патологические гипопротеинемии разделяют на:
1. Гемодилюционные (ложные). Уменьшение уровня белка происходит за счет его «разбавления» избытком жидкой части крови (гиперволемия) при водной интоксикации, олиго- или анурии, первичном гиперальдостеронизме, синдроме неадекватной секреции антидиуретического гормона.
2. Истинные. При данной разновидности гипопротеинемия развивается за счет снижения синтеза белка, повышенных его потерь с мочой либо ускоренного распада. В свою очередь подразделяются на:
По снижению содержания отдельной фракции белков выделяют:
Причины гипопротеинемии
Заболевания почек
Самая частая причина гипопротеинемии – болезни почек, сопровождающиеся нефротическим синдромом, одним из ключевых компонентов которого является гипоальбуминемия. Падение уровня белка патогенетически напрямую связано с протеинурией. Вследствие повреждения гломерулярного аппарата почек подоциты клубочков теряют отрицательный заряд, из-за чего нарушается основной фильтрационный барьер для альбуминов и они экскретируются с мочой. В результате уровень белка в крови снижается. К заболеваниям, при которых наблюдается нефротический синдром, относятся:
В большинстве случаев нефротического синдрома происходит либо незначительное, либо умеренное снижение содержания белка в крови. При моноклональных гаммапатиях, особенно при амилоидозе, показатели белка могут достигнуть довольно низких цифр. Гипопротеинемия возникает медленно, прогрессирует параллельно развитию основного заболевания. После достижения ремиссии под влиянием специфического лечения уровень белка достаточно быстро приходит в норму.
Болезни печени
Основной орган, где происходит образование практически всех белков организма человека, – это печень. При массивной гибели гепатоцитов нарушается синтетическая функция органа, в том числе белковообразовательная. В первую очередь снижается фракция альбуминов. Гипоальбуминемия наряду с другими показателями служит одним из критериев оценки тяжести печеночной недостаточности. Заболевания печени, при которых встречается гипоальбуминемия:
В зависимости от степени прогрессии печеночной недостаточности гипопротеинемия может возникнуть как остро, в течение нескольких часов (например, при остром вирусном гепатите или токсическом поражении печени), так и постепенно, в течение недель или месяцев (при циррозе печени). Уровень падения белка может быть как незначительным, так и опускаться до очень низких показателей, что иногда требует, помимо терапии основного заболевания, дополнительного введения альбумина.
Заболевания, сопровождающиеся мальабсорбцией
Потери белка через желудочно-кишечный тракт наблюдаются гораздо реже. Гипопротеинемия может развиться из-за нарушения усвоения белка, поступающего в организм с пищей. Это возникает при недостаточности панкреатических и кишечных ферментов, расщепляющих белки (хронический панкреатит), или воспалительном поражении кишечной стенки, препятствующем всасыванию аминокислот из просвета тонкого кишечника в кровоток (неспецифический язвенный колит или болезнь Крона).
Также мальабсорбция с нарушением всасывания питательных веществ, в т.ч. белков, встречается при атрофии кишечных ворсинок вследствие их поражения аутоантителами (целиакия глютеновая). Гипопротеинемия при данных заболеваниях может быть тяжелой, особенно при панкреатите и целиакии, что часто требует дополнительного возмещения белкового дефицита.
Преходящая мальабсорбция может наблюдаться при острых кишечных инфекциях – сальмонеллезе, дизентерии, иерсиниозе и пр. Однако, чтобы добиться нормализации уровня белка, в этих случаях достаточно антибактериальной терапии и возобновления питания больного.
Иммунодефицитные состояния
В отличие от других вышеперечисленных причин, низкий уровень белка при иммунодефицитных состояниях возникает за счет фракции глобулинов, а точнее, иммуноглобулинов (антител), что собственно и служит основным звеном патогенеза нарушений гуморального иммунитета. Причиной падения концентрации белков могут быть мутации генов, регулирующих выработку иммуноглобулинов (первичные иммунодефициты) – это синдром Вискотта-Олдрича, синдром Джоба.
Из приобретенных иммунодефицитов гипопротеинемия чаще всего встречается при ВИЧ-инфекции на стадии синдрома приобретенного иммунодефицита (СПИДа), а также при злокачественных лимфомах, хроническом лимфолейкозе. Степень гипопротеинемии при этих заболеваниях довольно значительная, показатели общего белка могут достаточно продолжительное время оставаться ниже референсных значений даже после проведения лечения.
Редкие причины
При данных патологических состояниях падение в крови концентрации белка наблюдается редко и в тяжелых случаях. Основными звеньями патогенеза гипопротеинемии выступают усиленный переход альбуминов из сосудистого русла в интерстициальное пространство (за счет резкого увеличения проницаемости стенок капилляров) и ускоренный катаболизм белков. К таким причинам относятся:
Диагностика
Ввиду большого количества причин гипопротеинемии ее обнаружение требует подробной дифференциальной диагностики. При получении биохимического анализа крови с высоким содержанием белка сначала необходимо обратиться к врачу-терапевту. При физикальном осмотре больного обращают внимание на клинические признаки гипопротеинемии – периферические отеки или пастозность нижних конечностей, увеличение объема живота за счет асцита, приглушение сердечных тонов.
При сборе анамнеза уточняют, какими хроническими заболеваниями страдает пациент, состоит ли он на учете у какого-то специалиста. Эта информация может помочь в диагностическом поиске причин отклонения в анализе. Назначаются следующие дополнительные методы обследования:
Коррекция
Гемодилюционные и физиологические гипопротеинемии разрешаются самостоятельно и не требуют никакого медицинского вмешательства. Лечение гипопротеинемии преследует две главные цели – коррекция белкового дефицита и терапия основного заболевания. Для этого проводятся следующие мероприятия:
Прогноз
Выраженная гипопротеинемия может повлечь за собой неблагоприятные последствия для пациента. Падение уровня альбуминов снижает онкотическое давление плазмы крови, что приводит к пропотеванию жидкости в полости тела (брюшную, плевральную, перикардиальную). Также при низкой концентрации белка повышается уровень холестерина в крови, возникает жировая дистрофия печени и нарушается выработка противоинфекционных белков – иммуноглобулинов, белков системы комплемента. Поэтому обнаружение гипопротеинемии требует обращения к врачу.
Что такое гиперлипопротеинемия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Колесниченко Ирины Вячеславовны, кардиолога со стажем в 24 года.
Определение болезни. Причины заболевания
Это состояние является частным случаем дислипидемии.
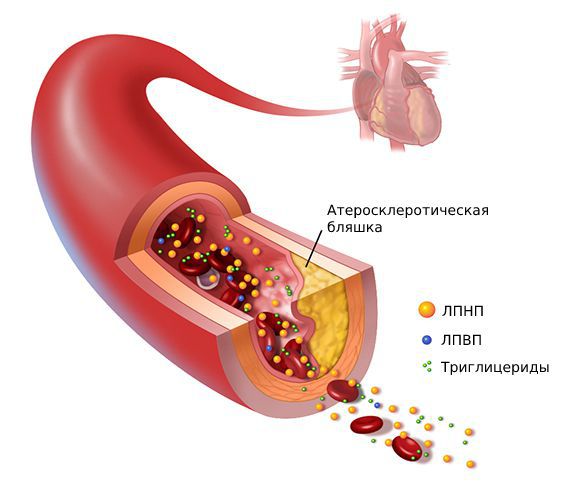
Заболевание может долго протекать без симптомов и выявляться случайно после сдачи анализов. При длительном течении болезни развивается атеросклероз, который приводит к сужению сосудов. Симптомы зависят от того, какие артерии поражены:
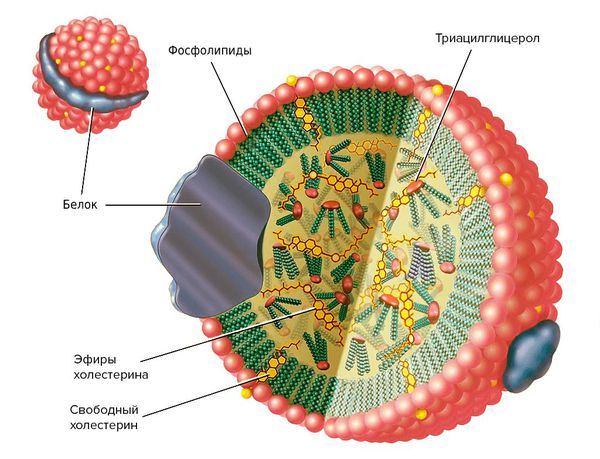
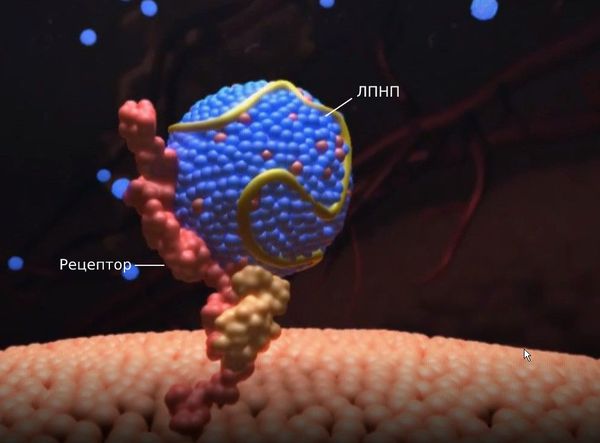
Липопротеины — это растворимые в воде частицы, состоящие из жиров (липидов) и белков (апопротеинов). Они очень важны для организма, поскольку переносят витамины, гормоны и жиры, которые поступают с пищей и синтезируются в печени.
Распространённость
Причины гиперлипопротеинемии
Гиперлипопротеинемии бывают первичными и вторичными. Первичные формы имеют врождённую природу, но встречаются довольно редко: ими страдают 0,25 % населения.
К врождённым гиперлипидемиям относятся:
Вторичные гиперлипопротеинемии обусловлены различными заболеваниями, приёмом некоторых лекарств и неправильным образом жизни.
Наиболее часто заболевание развивается при сахарном диабете, хронической почечной недостаточности, нефротическом синдроме, гипотиреозе, ожирении, желчнокаменной болезни, холестазе, анорексии, частичной или полной потере жировой ткани (липодистрофии), болезнях накопления гликогена, сильном стрессе, сепсисе, беременности, остром гепатите, системной красной волчанке и лимфоме.
Лекарства, которые могут привести к гиперлипопротеинемии:
К развитию гиперлипопротеинемии часто приводит неправильный образ жизни на фоне хронических заболеваний. К неблагоприятным факторам относятся:
Также важно отметить причины, из-за которых снижается уровень ЛПВП. Помимо курения, к ним относятся недостаточное питание и ожирение. Концентрация защитных липопротеинов может уменьшаться при приёме бета-блокаторов и анаболических стероидов.
Уровень общего холестерина может быть выше нормы и у здоровых людей, например при неправильной подготовке к анализу крови и во время беременности.
Гиперлипопротеинемия при беременности
У беременных женщин уровень общего холестерина повышается в 1,5–2 раза. Он резко возрастает в начале II триместра, когда активно формируется плацента. Холестерин — это основа для её клеток, поэтому чем больше срок беременности, тем выше его уровень.
Симптомы гиперлипопротеинемии
Гиперлипопротеинемия может длительное время протекать бессимптомно. Повышенный уровень вредных липидов выявляется при анализах, но клинические симптомы долго не возникают.
При врождённых гиперлипопротеинемиях, вызванных генетическими факторами, симптомы появляются рано. Уровень холестерина при врождённых формах болезни всегда выше 6,5 ммоль/л. Он колеблется от 7 до 13 ммоль/л и выше.
Симптомы первичной гиперлипопротеинемии
К характерным проявлениям гомозиготной семейной гиперхолестеринемии, при которой человек наследует дефектный ген от обоих родителей, относятся:
При семейной гипертриглицеридемии в крови повышается уровень триглицеридов (до 2,8–8,5 ммоль/л) и липопротеинов очень низкой плотности.
Симптомы вторичной гиперлипопротеинемии
При вторичных гиперлипопротеинемиях симптомы зависят от расположения поражённых атеросклерозом артерий, степени и количества вовлечённых сосудов.
Долгое время уровень вредных липопротеинов растёт, а содержание защитных липопротеинов снижается, но симптомы отсутствуют. Они появляются по мере развития атеросклероза.
К таким признакам относятся:
В зависимости от того, какие артерии повреждены атеросклерозом, возникают следующие симптомы:
Патогенез гиперлипопротеинемии
Первичные гиперлипопротеинемии вызваны мутациями в генах, которые ответственны за образование и работу рецепторов к липопротеинам низкой плотности. При гетерозиготной форме семейной гиперхолестеринемии ЛПНП-рецепторы могут быть наполовину полноценными, а при гомозиготной форме — практически полностью отсутствовать. Из-за этого дефекта рецепторы не захватывают липопротеины, они хуже распадаются и не выводятся из организма, поэтому их уровень в крови растёт.
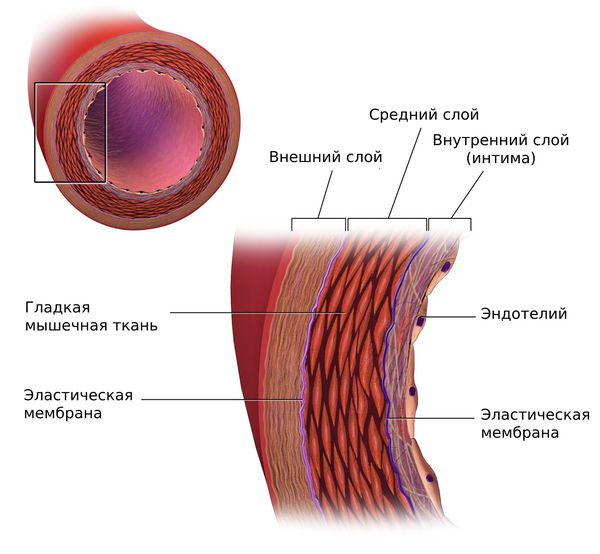
При вторичных гиперлипопротеинемиях повреждается внутренняя оболочка артерий и в неё активно проникают липопротеины.
Липопротеины подразделяются на два вида:
Атерогенность зависит от размеров и физико-химических свойств липопротеиновых частиц.
Липопротеины очень низкой плотности и липопротеины низкой плотности (ЛПОНП и ЛПНП) являются атерогенными и проникают во внутреннюю оболочку артерий (интиму) при повреждении эндотелия.
Дисфункцию эндотелия артерий вызывают:
Под влиянием этих факторов эндотелий разрыхляется и истончается. Расширяются щели между клетками, возникает отёк, клетки и волокнистые структуры внутренней оболочки артерий разъединяются, и частицы атерогенных липопротеинов проникают в интиму артерий.
Затем к этим частицам присоединяется глюкоза. Процесс модификации липопротеинов называется гликозилированием, или гликированием. Он особенно интенсивен при сахарном диабете и избытке глюкозы в крови. В результате нарушается взаимодействие ЛПНП с рецепторами клеток, замедляется распад липопротеинов и, следовательно, развивается гиперлипопротеинемия. Гликирование защитных ЛПВП ускоряет их распад.
Второй путь модификации липопротеинов низкой плотности — пероксидация, или перекисное окисление. Это важнейший фактор развития атеросклероза. В организме постоянно образуются свободные радикалы: ионы, атомы или молекулы с одним неспаренным электроном на своей орбите. Поскольку у них есть свободное место для электрона, они стремятся отнять его у других молекул. Так окисляются любые соединения, с которыми они соприкасаются. Пероксидация ЛПНП делает их высокоатерогенными.
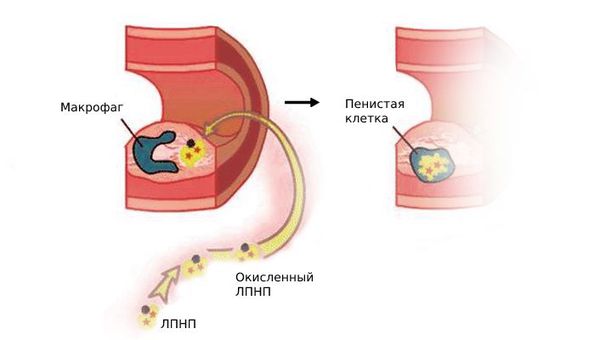
Следующий этап атерогенеза — пропитывание интимы артерий циркулирующими лейкоцитами (моноцитами), которые трансформируются в макрофаги. Они захватывают модифицированные ЛПНП, содержание холестерина в макрофагах быстро нарастает, и они превращаются в пенистые клетки.
Пенистые клетки остаются в интиме артерий и погибают. При этом они выделяют накопленный холестерин, который образует липидные пятна и полоски, а затем атеросклеротические бляшки.
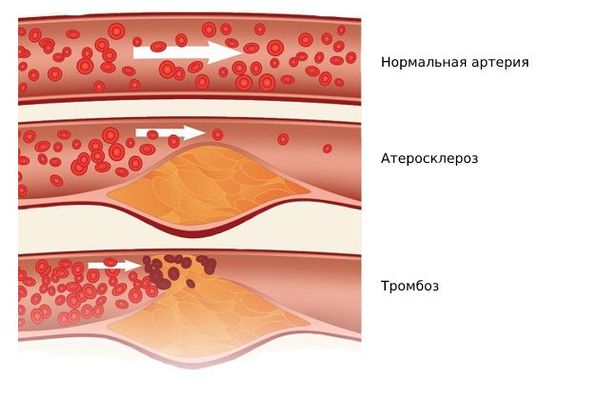
Одним из наиболее серьёзных осложнений атеросклероза является тромбоз в области бляшки — частичная или полная закупорка артерии тромбом. Образованию тромба предшествуют надрывы и разрывы фиброзной покрышки бляшки, а также повреждение эндотелия самой бляшкой. Иногда атеросклеротическая бляшка становится источником эмболий, при которых её оторвавшийся кусочек закупоривает какой-либо сосуд.
Осложнением атеросклеротической бляшки также является атерокальциноз — отложение солей кальция в стенке сосудов.
Классификация и стадии развития гиперлипопротеинемии
Наиболее распространена классификация липопротеинов в зависимости от плотности:
По участию в развитии атеросклероза липопротеины подразделяются на три класса:
Типы гиперлипопротеинемии
Гиперлипопротеинемии подразделяются на следующие типы:
Также широко применяется классификация гиперлипопротеинемий, предложенная Фредриксоном и соавторами в 1967 году:
Осложнения гиперлипопротеинемии
Диагностика гиперлипопротеинемии
Диагностика гиперлипопротеинемий состоит из осмотра, лабораторных исследований и инструментальных методов.
Осмотр
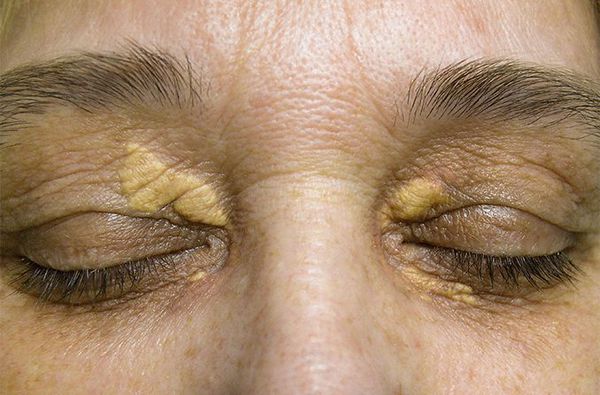
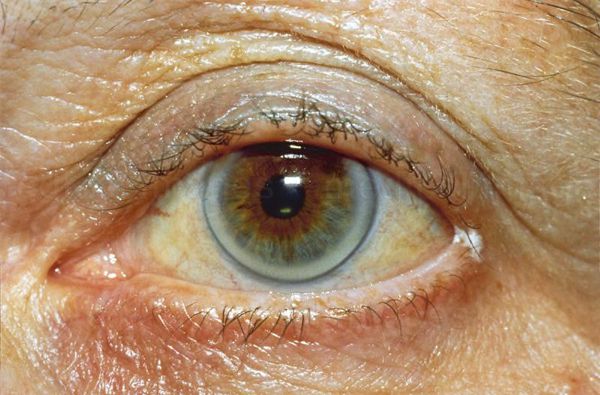
При осмотре врач обращает внимание на признаки, указывающие на нарушение обмена липидов:
Измерение артериального давления
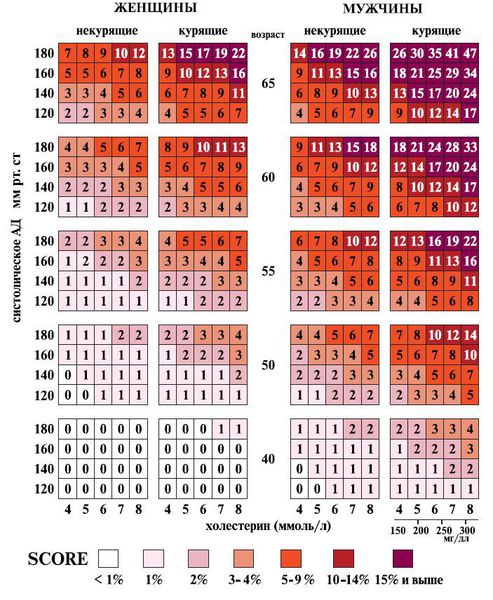
Шкала SCORE — это тест-калькулятор для оценки сердечно-сосудистого риска.
Сердечно-сосудистый риск зависит от сочетания следующих факторов:
По шкале SCORE пациенты попадают в категории низкого, умеренного, высокого и очень высокого риска.
Полученное значение показывает вероятность смерти от сердечно-сосудистого заболевания в ближайшие 10 лет.
Также всем пациентам необходимо проверить состояние печени. Для этого исследуется уровень печёночных ферментов (АСАТ, АЛАТ). Анализ позволяет определить, можно ли назначать статины — препараты для снижения уровня липопротеинов.
Не менее важно проверить состояние щитовидной железы. Для этого исследуется уровень тиреотропного гормона (ТТГ), так как гипотиреоз может быть причиной нарушений липидного обмена и требует коррекции.
Также при гиперлипопротеинемии необходимо определить уровень глюкозы в крови, поскольку сахарный диабет способствует быстрому развитию атеросклероза.
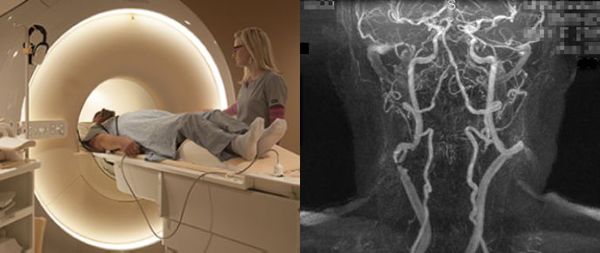
Инструментальные методы диагностики
Для выявления атеросклероза используются:
Лечение гиперлипопротеинемии
Диета
Если у пациента нет симптомов, то лечение начинают со специальной диеты. Коррекция питания позволяет уменьшить уровень холестерина на 5–10 %.
Важно помнить, что холестерин не только поступает извне, но и образуется в организме. Поэтому полностью отказываться от продуктов, содержащих жиры, не стоит.
Медикаментозное лечение
При сердечно-сосудистых заболеваниях, сахарном диабете, хронической болезни почек и высоком риске по шкале SCORE показан приём препаратов, снижающих холестерин. Однако в ряде случаев пациентам даже с умеренным риском может потребоваться медикаментозная терапия. Она поможет уменьшить вероятность развития атеросклероза.
Группы препаратов для лечения гиперлипопротеинемии:
Статины
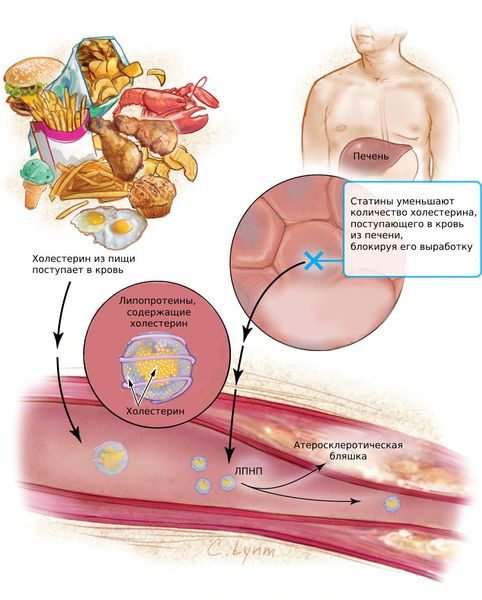
Статины (Аторвастатин, Розувастатин, Питавастатин) — это наиболее эффективные средства для снижения холестерина. Они блокируют фермент, который участвует в его образовании и тем самым подавляет выработку холестерина в печени. Статины снижают содержание липопротеинов низкой плотности (ЛПНП) и триглицеридов (ТГ).
Статины предотвращают развитие атеросклероза коронарных и церебральных артерий, а при длительном приёме уменьшают размер бляшек в сосудах. Эти препараты необходимы пациентам с гиперлипопротеинемией и атеросклерозом для профилактики инфаркта миокарда и инсульта.
Перед тем, как начать принимать статины, необходимо определить липидный профиль, а также проверить состояние печени по содержанию в крови печёночных ферментов (АСАТ, АЛАТ). Статины применяют в безопасных дозировках до достижения целевых уровней ЛПНП. Дозировка зависит от кардиоваскулярного риска пациента.
Для оценки безопасности и эффективности назначенной дозы через месяц после начала приёма необходимо повторно провести анализы на липидный профиль, АСАТ и АЛАТ. Эффект проявляется в течение первой недели от начала лечения. Через две недели он составляет 90 % от максимального действия. Наибольший эффект достигается к четвёртой неделе и затем остаётся постоянным.
Если целевой уровень ЛПНП достигнут и препарат не влияет отрицательно на печень, то статин в данной дозировке применяют длительно. Липидный профиль, АСАТ и АЛАТ контролируют через каждые 3–6 месяцев. При повышении печёночных ферментов выше трёх норм препарат перестают применять.
Помимо снижения холестерина, статины положительно влияют на состояние внутренней оболочки артерий, стабилизируют атеросклеротические бляшки и улучшают текучесть крови.
Статины обычно хорошо переносятся, но у некоторых пациентов возникают побочные эффекты, например боль в мышцах. Принимать препараты следует под постоянным контролем врача, вовремя корректировать их дозу или использовать в комбинации с другими лекарствами.
Фибраты
Фибраты (Фенофибрат) стимулируют активность фермента липопротеинлипазы и тем самым ускоряют распад липопротеинов. Они снижают не только холестерин, но и триглицериды (ТГ). Это препараты выбора у больных с сахарным диабетом, у которых чаще всего повышены ТГ.
Ингибиторы всасывания холестерина в кишечнике
Секвестранты желчных кислот
Секвестранты (Холестирамин, Колестипол) — ионообменные смолы, которые не дают желчным кислотам всасываться в кишечнике. Истощение запасов этих кислот активирует их синтез из холестерина в печени. Применяются у пациентов с холестазом.
Приём препаратов данной группы часто вызывает побочные эффекты: метеоризм, задержку стула, тошноту, боль или дискомфорт в верхнем отделе живота, что ограничивает их применение.
Моноклональные антитела
N-3 жирные кислоты
Гиполипидемическую терапию важно назначать вовремя, чтобы предотвратить развитие атеросклероза и его осложнений.
Прогноз. Профилактика
При ранней диагностике гиперлипопротеинемии и своевременном снижении уровня атерогенных липопротеинов прогноз благоприятный.
Заболевание может долго протекать без симптомов и выявиться только при профилактическом исследовании, поэтому необходимо регулярно определять липидный профиль. Это поможет избежать атеросклероза и его серьёзных осложнений: инфаркта миокарда, инсульта и т. д.
Если дислипидемия диагностирована при развившемся атеросклерозе, то следует изменить питание и начать медикаментозное лечение. Если удаётся добиться целевых уровней липидов в крови, то прогноз благоприятный. В таком случае сердечно-сосудистый риск значительно снижается. Пациенту необходимо следовать рекомендациям врача и регулярно делать липидограмму.
Прогноз неблагоприятный при значительном повышении уровня липидов в крови, сопутствующих заболеваниях, таких как артериальная гипертензия, сахарный диабет, хроническая болезнь почек и осложнения атеросклероза. Такие пациенты находятся в группах высокого и очень высокого риска с большой смертностью.
Профилактика гиперлипопротеинемии
Цель первичной профилактики — уменьшить влияние возможных причин гиперлипопротеинемии. Для этого нужно правильно питаться, не курить, больше двигаться и по возможности исключить препараты, нарушающие обмен липидов.
Также для профилактики атеросклероза следует: