Гипогонадизмом что это такое
Гипогонадизм у мужчин: причины, признаки, принципы лечения
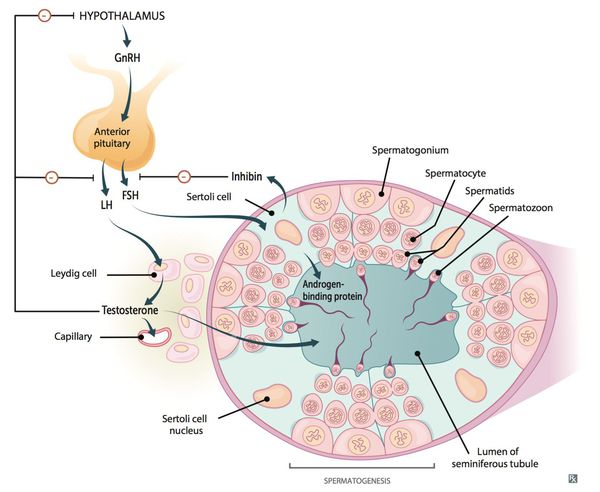
У здорового мужчины вырабатываемые половые гормоны обеспечивают нормальное развитие половых органов, формирование половых признаков и белково-жировой обмен. Если по какой-то причине синтез гормонов сбивается, развивается гипогонадизм. Это недостаточность половых желез и нарушение выработки половых гормонов. Такие процессы ведут к серьезным проблемам, которые решаются совместно эндокринологами и андрологами. Предлагаем подробнее изучить причины, симптомы и принципы лечения гипогонадизма у мужчин.
Основные симптомы и проявления заболевания
Гипогонадизм развивается из-за недостатка половых гормонов. Из-за дефицита страдают органы, которые зависят от этих гормонов. Симптомы гипогонадизма могут проявляться по-разному. Имеют значение возраст возникновения заболевания и причина снижения количества гормонов.
Если не началось половое созревание
Если сбой произошел до начала полового созревания, то оно происходит с задержкой. У мальчика отмечается очень высокий рост, его руки и ноги выглядят слишком длинными, а грудная клетка — маленькой по сравнению с другими частями. Оволосения по мужскому типу тоже не происходит, поскольку это зависит от половых гормонов.
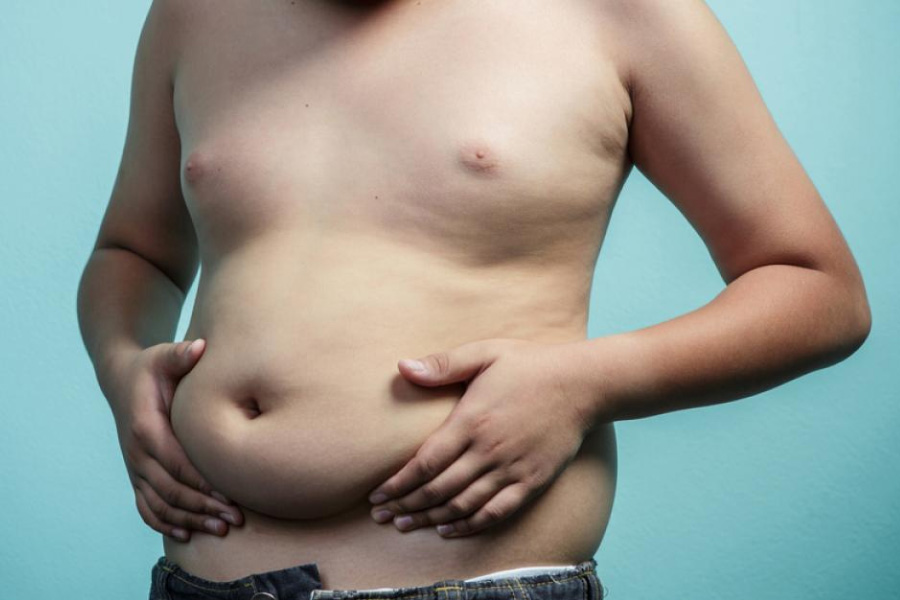
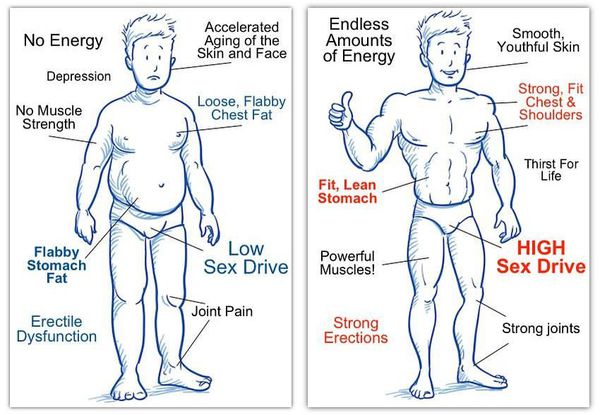
Ожирение при гипогонадизме — еще один характерный признак. Из-за недостатка тестостерона оно развивается по женскому типу. Кроме него формируется гинекомастия — увеличение молочных желез, и наблюдается недоразвитый половой член небольших размеров.
По окончании полового созревания
Если выработка гормонов была нарушена после пубертатного периода, признаки гипогонадизма выражены не так ярко. У мужчины уменьшаются яички, снижается оволосение тела, начинает развиваться ожирение с откладыванием жира по женскому типу. Кожа теряет эластичность и становится тонкой, появляются проблемы с половой функцией, может развиваться бесплодие.
Самый первый признак — уменьшение размера яичек. Этого не происходит, только если болезнь начала развиваться недавно. При ее прогрессировании нарушается сперматогенез — развитие мужских половых клеток. Яички теряют свою основную функцию, что приводит к бесплодию с прекращением выработки тестостерона. Вторичные половые признаки постепенно регрессируют. На фоне этого у мужчины могут быть слабость, утомляемость и ослабление мышц.
Классификация и причины гипогонадизма
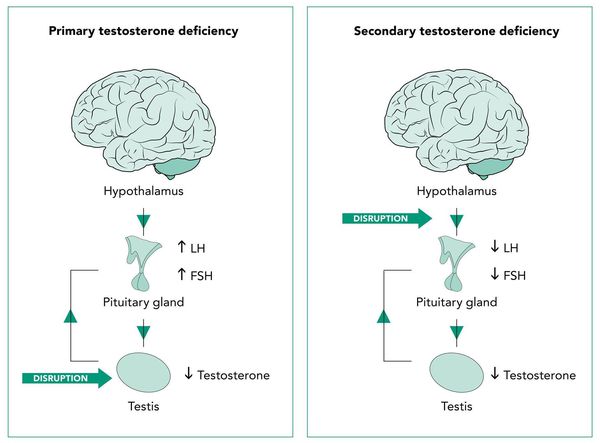
Основная причина гипогонадизма — снижение объема или нарушение выработки половых гормонов. Это может быть вызвано заболеваниями яичек или проблемами в регуляции синтеза гормонов на уровне гипофиза и гипоталамуса. В зависимости от причины выделяют первичный и вторичный гипогонадизм. Первичный — это тот, что спровоцирован проблемами в яичках, и его могут вызывать:
Вторичный гипогонадизм вызывают заболевания гипофиза и гипоталамуса. Это могут быть опухоли, воспаления, сосудистые проблемы. К распространенным причинам относятся:
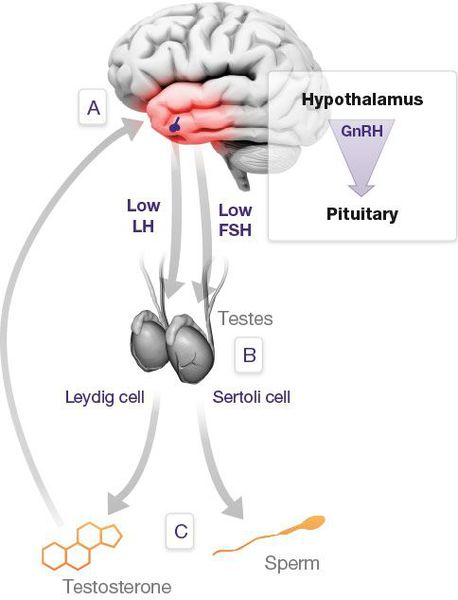
Первичную и вторичную форму различает уровень гонадотропных гормонов (гормонов передней доли гипофиза — ФСГ (фолликулостимулирующего) и ЛГ (лютеинизирующего), регулирующих половых железы. В зависимости от этого выделяют:
Отсюда легко сделать вывод, что гипергонадотропная форма вызвана нарушением в работе яичек, а гипо-и нормогонадотропная — проблемами в гипоталамо-гипофизарной системе.
Есть подозрение на гипогонадизм — что делать?
Если у мужчины есть симптомы дефицита тестостерона как признака гипогонадизма, необходимо обратиться к андрологу или урологу-андрологу. На основании жалоб пациента врач сможет предположить, в чем проблема, вызвавшая такое состояние.
Для постановки диагноза оцениваются половые органы и вторичные половые признаки, выявляются характерные признаки заболевания. Подтвердить диагноз и выявить причину помогают рентген турецкого седла (там находится гипофиз), анализ спермы, анализ крови на половые и гонадотропные гормоны.
Лечение гипогонадизма зависит от причины, поэтому определяется в индивидуальном порядке. Взрослым назначают заместительную терапию гормонами, мальчикам — негормональными препаратами. При первичной форме принимают тестостерон, при вторичной — гонадотропины. Если причина — опухоль, то в рамках лечения ее могут удалить хирургическим путем.
Поскольку эффективность лечения напрямую зависит от правильности диагностики, мужчине важно вовремя обратиться к врачу и пройти все назначенные исследования. В клинике Dr. AkNer работают урологи-андрологи с большим опытом в лечении гипогонадизма. Для получения консультации запишитесь на прием, воспользовавшись формой обратной связи или контактным номером.
Гипогонадизм
Гипогонадизм — патологическое состояние, развивающееся на фоне дисфункции тестикул у мужчин и яичников у женщин. Заболевание приводит к недоразвитию внутренних и наружных половых органов, вторичных половых признаков. Часто страдающие от синдрома пациенты сталкиваются с нарушениями жирового и белкового обмена.
Мужской гипогонадизм
Заболевание протекает в хронической форме. Лечение направлено на нормализацию выработки половых гормонов и устранение симптомов патологии. Терапевтический курс разрабатывается эндокринологами совместно с урологами.
Классификация патологии
Врачи выделяют два типа гипогонадизма. Первичная форма заболевания развивается на фоне дефекта половых желёз, провоцирующего угнетение функций текстикулярной ткани. Патологический процесс становится следствием хромосомных нарушений, возникших в период внутриутробного развития плода. В раннем возрасте мальчики могут проявлять психический инфантилизм.
Вторичный гипогонадизм формируется при структурных изменениях в гипофизе пациента. Мозговой придаток теряет свои регулирующие функции, что приводит к недостаточной выработке половых гормонов в организме мужчины. Течение заболевания осложняется психическими расстройствами.
Причины мужского гипогонадизма
Заболевание развивается при снижении секреторной функции яичек, нарушении процесса гормонального синтеза или изменениях в тканях гипофиза. Первичная форма патологии обуславливается:
Отдельные случаи гипогонадизма рассматриваются врачами как идиопатические — точные причины снижения секреторной функции яичек у пациентов остаются неизвестными.
Симптомы патологии
Клиническая картина заболевания определяется возрастом пациента и степенью андрогенной недостаточности. Пороки внутриутробного развития плода могут приводить к формированию двуполых наружных половых органов.
Поражения половых желёз в допубертатном возрасте становится причиной задержки полового развития. Мальчики отличаются высоким ростом, чрезмерно удлинёнными конечностями, недоразвитой грудной клеткой и плечевым поясом. Скелетная мускулатура остаётся слабой. Некоторые пациенты сталкиваются с признаками ожирения по женскому типу и гипогенитализмом. Мужчины страдают от гинекомастии, отсутствия волосяного покрова на лице и теле. Часто заболевание осложняется эректильной дисфункцией и отсутствием влечения к женщинам.
Диагностика заболевания
Уролог проводит осмотр пациента и фиксирует в анамнезе антропометрические данные. Важная часть диагностики — оценка степени полового созревания мужчины. Пальпация гениталий позволяет врачу обнаружить клинические симптомы гипогонадизма.
Лицам, страдающим от дисфункции желёз, назначаются различные анализы. Изучение эякулята в лабораторных условиях направлено на выявление признаков олиго– или азоспермии. Исследования крови дает возможность понять количество гормонов (тестостерона, пролактина и эстрадиола), вырабатываемых половыми железами.
Лечение мужского гипогонадизма
Терапевтический курс для пациента разрабатывается эндокринологом после консультаций с урологом. Терапия позволяет устранить причину заболевания и компенсировать отставание в развитии, которое проявилось у ребёнка до начала пубертатного периода. Назначение гормональных препаратов детям призвано предотвратить злокачественное перерождение текстикулярных тканей и развитие бесплодия.
Состав терапевтического курса зависит от клинической формы гипогонадизма. Большинство мужчин получают препараты тестостерона в виде инъекций. В отдельных случаях страдающим от патологии назначаются модуляторы рецепторов эстрогена и ингибиторы ароматазы.
Женский гипогонадизм
Женщины, страдающие от рассматриваемого заболевания, сталкиваются с недоразвитием и гипофункцией яичников. Первичная форма патологии развивается на фоне врождённых дефектов половых желёз. Недостаток половых гормонов вызывает ускоренный синтез гонадотропинов. При анализе крови сотрудники лабораторий фиксируют низкий уровень эстрогенов. Их недостаток приводит к атрофическим изменениям половых органов и молочных желёз. Повреждения яичников, проявившееся до наступления пубертатного возраста, приводит к отсутствию у девушек вторичных половых признаков.
Причины развития заболевания
Заболевание первичной формы становится следствием врождённых генетических нарушений, инфекционных поражений, воздействия ионизирующего облучения, хирургических вмешательств, синдрома поликистозных яичников и т. д. Вторичный гипогонадизм развивается у женщин на фоне патологии гипоталамуса и гипофиза. Этот процесс приводит к недостаточной секреции гонадотропинов, регулирующих функцию половых желёз. Гипоталамо-гипофизарная дисфункция — осложнение, проявляющееся при воспалительных процессах в головном мозге или быстром росте злокачественных новообразований.
Симптомы женского гипогонадизма
Женщины репродуктивного возраста могут столкнуться с нарушением менструального цикла и аменореей. Дисфункция яичников приводит к недоразвитию гениталий и молочных желёз, отсутствию волосяного покрова лобке. Развитие патологии до начала пубертатного периода становится причиной отсутствия у девушек вторичных половых признаков. Постпубертатное развитие гипогонадизма провоцирует прекращение менструаций и атрофию тканей наружных половых органов.
Диагностика патологии
Диагностические процедуры включают в себя гинекологический осмотр и серию лабораторных анализов. Исследование биоматериалов позволяет убедиться в повышенном уровне гонадотропинов в крови (фолликулостимулирующего и лютеинизирующего гормонов). Сонография продемонстрирует признаки гипоплазии матки и уменьшения яичников.
Лечение женского гипогонадизма
Пациентки, страдающие от первичной формы заболевания, получают заместительную гормональную терапию на основе препаратов этинилэстрадиола. На следующем этапе лечения девушкам назначаются эстрогены и гестагены. Гормональная терапия противопоказана женщинам, проходящим лечение на фоне злокачественных поражений молочных желёз, органов репродуктивной системы, почек, печени и т. д.
Вопросы и ответы
Источники
При подготовке статьи использовались следующие материалы:
Что такое андрогенный дефицит (гипогонадизм у мужчин)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скатова Бориса Васильевича, уролога со стажем в 27 лет.
Определение болезни. Причины заболевания
Андрогенный дефицит у мужчин (мужской гипогонадизм) — это клинический и биохимический синдром, характеризующийся снижением уровня мужских половых гормонов (прежде всего тестостерона), возникающий на фоне функциональной недостаточности яичек. [3] [14] [15]
Последние научные исследования убедительно доказали огромную роль дефицита основного мужского полового гормона — тестостерона — в формировании и развитии большинства урологических заболеваний у мужчин, в том числе рака предстательной железы и почек.
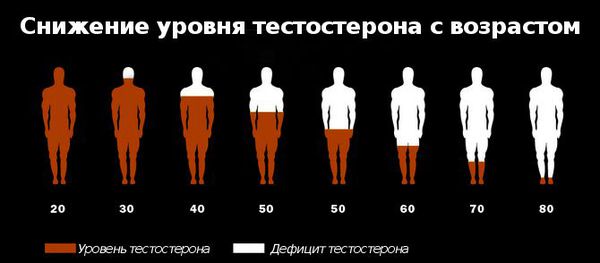
Существует устойчивое мнение, что проблемы, связанные с низким тестостероном, бывают только у пожилых мужчин. На самом деле это далеко не так. Современные данные показывают, что развитие андрогенного дефицита может наступить в любом возрасте. [16] [17] [18]
Первое современное мультицентровое мегаисследование мирового значения возрастного андрогенного дефицита MMAS (2000) выявило основные тенденции к снижению уровня общего тестостерона в крови у мужчин на 0,8% в год. [19] Наряду с этим, концентрация глобулина, связывающего половые гормоны (ГСПС), увеличивается на 1,6% в год, что позволяет позиционировать ГСПС как диагностический фактор возрастного андрогенного дефицита. [20]
Дальнейшее изучение проблемы показало, что уровень андрогенной недостаточности у мужчин 41–80 лет составляет более 35%, что является серьёзным показателем. [21] По исследованиям C. McHenry Martin (2013 год), более 6 млн американских мужчин имеют пониженную концентрацию гормона тестостерона в крови, что проявляется депрессией, пониженной работоспособностью и сердечно-сосудистыми заболеваниями. [23] А исследование, проведённое в Швеции среди мужчин в возрасте 33–46 лет, показало, что частота нарушений эрекции в этих группах отражала низкий уровень общего тестостерона в крови, который оказался ниже у 45-летних испытуемых по сравнению с мужчинами в возрасте 33 лет. [24]
Таким образом, дефицит андрогенов является значимым фактором для каждого мужчины и требует постоянного внимания как со стороны самого пациента, так и со стороны врачей различных специальностей.
Причины андрогенного дефицита
I. Тестикулярные причины (связанные с нарушением работы яичек). Их принято разделять на приобретённые и врождённые.
II. Другие причины АД:
Симптомы андрогенного дефицита
К симптомам андрогенного дефицита относятся следующие признаки:
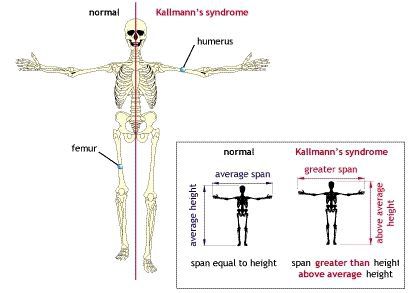
Если андрогенная недостаточность возникла до начала полового созревания, то тело приобретает характерную высокорослость с евнухоидными пропорциями. При этом размах рук превышает длину тела, а ноги оказываются длиннее туловища. В результате, такие пациенты сидя выглядят низкорослыми («сидячая карликовость»), а стоя — очень высокими («стоячий гигантизм»).
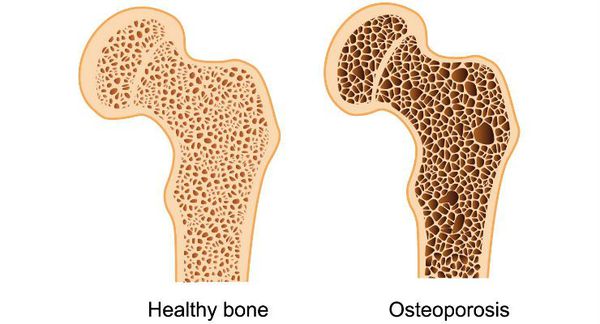
Длительная андрогенная недостаточность приводит к хрупкости костей (остеопорозу), что может сопровождаться патологическими переломами позвонков и бедренных костей, болями в спине.
Дефицит андрогенов прямо не ведёт к увеличению подкожной жировой ткани, но распределение жира приобретает женский характер (отложения на бёдрах, ягодицах, нижней части живота). Мышечная масса тела, наоборот, уменьшается.
В том случае, если андрогенный дефицит возник до наступления полового созревания, длина гортани не увеличивается и огрубление голоса не происходит.
Несмотря на высокий рост, таких пациентов принимают за женщин, особенно по телефону, что порождает у них дополнительные комплексы.
Сохраняется прямая граница волос надо лбом, борода не растёт или растёт очень плохо, почти не требует бритья. Оволосение тела очень скудное.
Ещё один типичный признак — раннее появление тонких морщин вокруг глаз и рта. Кроме того, в результате отсутствия стимуляции сальных желёз кожа остаётся сухой. Анемия и плохое кровоснабжение определяют сильную бледность кожи.
Также важный признак — снижение или полное отсутствие способности различать запахи (вероятность синдрома Кальмана). Такие больные не способны ощущать, например, запах ванилина, лаванды и другие ароматы, но сохраняют способность различать вещества, раздражающие тройничный нерв (нашатырный спирт).
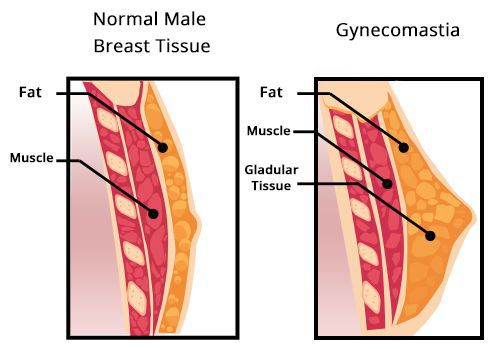
Снижение уровня тестостерона может вызвать увеличение грудных желёз у мужчин. В большинстве случаев, гинекомастия бывает двухсторонней, очень редко — односторонней. При выраженном, особенно одностороннем увеличении, пациента направляют на маммографию для исключения рака грудных желёз.
Увеличение груди сопровождается ощущением стеснения в груди и повышенной чувствительностью сосков. Нередко гинекомастия развивается у мальчиков при половом созревании (в возрасте 12–14 лет), но через 2–3 года исчезает. При ожирении картина становится ярче и сохраняется дольше. Иногда увеличение грудных желёз происходит у мужчин при старении.
В сочетании с маленькими плотными яичками, гинекомастия типична для синдрома Клайнфельтера.
Быстрое развитие гинекомастии может говорить о наличии гормонально-активной опухоли яичек. Характерная триада симптомов включает гинекомастию, утрату полового влечения и опухоль яичка. Причиной гинекомастии могут быть и общие заболевания: цирроз печени или почечная недостаточность.
Патогенез андрогенного дефицита
Патогенез андрогенного дефицита многообразен и зависит от конкретных причин. Рассмотрим основные моменты патогенеза андрогенной недостаточности.
Возрастной андрогенный дефицит
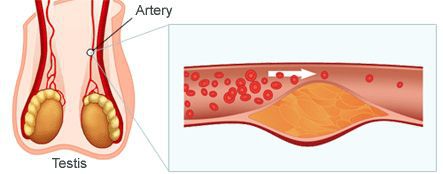
Патогенетические звенья возрастного андрогенного дефицита у мужчин запускаются, прежде всего, атеросклеротическими факторами, которые постепенно облитерируют (заращивают) заинтересованные сосуды. Это приводит к снижению кровотока в мужских гонадах, соответственно — к уменьшению синтеза тестостерона клетками Лейдига.
По мере прогрессирования процесса увеличивается чувствительность заднего отдела головного мозга — гипоталамуса — к тестостерону.
Параллельно, происходит увеличение концентрации в крови гонадотропинов, что ещё более усугубляет ситуацию.
Андрогенный дефицит при синдроме Кальмана
Интересен механизм развития патологических нарушений при синдроме Кальмана. В период развития нормального плода предшественники гонадотропин-рилизинг-зависимых гормонов — специальных нейронов — перемещаются из обонятельного эпителия слизистой носа к своей постоянной точке в гипоталамусе. У эмбриона с синдромом Кальмана, сцепленным с Х-хромосомой, это движение нарушается. Предшественники гонадотропин-рилизинг-зависимых гормонов не выходят из обонятельного эпителия и поэтому не влияют на специфические клетки гипофиза.
Основная характеристика синдрома Кальмана — незавершённое половое созревание или полное его отсутствие. Средний объём яичек у больных с синдромом Кальмана составляет не более 3 мл.
Витаминная недостаточность
Современные исследования показали огромную значимость недостатка витамина D у мужчин, в развитии андрогенного дефицита и снижения уровня тестостерона. Недостаток витамина D — это новая эпидемия XXI века, которая вызвана значительным снижением пребывания на солнце людей, которые проживают севернее 35-й параллели.
По большому счёту, витамин D вовсе не является витамином. Скорее это провитамин, точнее — гормон, который регулирует многие процессы в организме. Понятие «витамин D» подразумевает несколько одинаковых по строению форм витамина D, принадлежащих к классу сексостероидов — D1, D2, D3, D4, D5. Только D3 является истинным витамином D.
Витамин D образуется из продуктов питания и под воздействием солнечных лучей (ультрафиолета). Для преобразования в активную форму он должен пройти двухступенчатый процесс гидроксилирования:
Последние работы по синтезу тестостерона показали прямую корреляцию (взаимосвязь) между соотношением уровня витамина D и андрогенным недостатком у мужчин.
Так, масштабное европейское исследование EMAS (2012) доказало прямые соотношения между концентрациями витамина D и тестостерона у мужчин. Уровень 25-(OH) витамина D3 хорошо соотносился с уровнем общего и свободного тестостерона и недостаточно взаимодействовал с концетрацией эстрадиола и лютеинизирующего гормона (ЛГ), с учётом возраста.
Дефицит витамина D достоверно отражал динамику у мужчин с компенсированным и вторичным гипогонадизмом.
Сложилось мнение, что дефицит витамина D и связанная с ним андрогенная недостаточность являются важными эндокринологическими механизмами у мужчин, нарушающими соотношение жиросинтезирующих (пролактин, инсулин, кортизол) и жиросжигающих гормонов (гормон роста, катехоламины, половые и тиреоидные гормоны). Данная проблема находится в стадии широкого изучения. [29]
Стрессовые факторы
В стрессовых ситуациях в организме происходит перенапряжение симпатоадреналовой системы, в коре надпочечников вырабатывается большое количество различных гормонов и биологически активных веществ:
Кортизол синтезируется при стрессовых ситуациях, которые сочетаются с неудовлетворительным питанием и сопутствующими физическими перегрузками, пытается поддержать уровень глюкозы в крови.
В случае затяжного хронического стресса образуется повышение его физиологической концентрации, что негативно отражается на основном мужском гормоне — тестостероне — и резко уменьшает его концентрацию в крови.
Классификация и стадии развития андрогенного дефицита
По уровню основного мужского гормона тестостерона:
По характеру поражения:
С учётом времени выявления по отношению к половому созреванию:
В зависимости от причины:
По преимуществу клинических проявлений:
Осложнения андрогенного дефицита
При отсутствии полноценной терапии больного с андрогенным дефицитом симптоматика усугубляется, и те симптомы, которые проявлялись в лёгкой степени, становятся прямыми осложнениями нарастающего андрогенного дефицита.
К осложнениям андрогенного дефицита относятся:
Диагностика андрогенного дефицита
Анамнез заболевания
Обращается внимание на снижение общего тонуса организма, плохой рост бороды и усов, отсутствие спонтанных утренних и ночных эрекций, ослабление сексуального влечения и эротических фантазий.
Выясняется, какими заболеваниями болел пациент на протяжении жизни, были ли травмы, повреждения яичек, имелись ли подобные проблемы у родителей и близких родственников.
Нужно знать, какие лекарственные препараты принимал и принимает сейчас пациент, подвергался ли он внезапным термическим и химическим воздействиям.
Также следует учитывать интенсивность физических нагрузок и вредные привычки (курение, пристрастие к алкоголю).
Физикальное обследование
При осмотре пациента необходимо обращать внимание на клинические проявления андрогенного дефицита (выпадение волос, снижение массы тела, увеличение грудных желёз и т. д.).
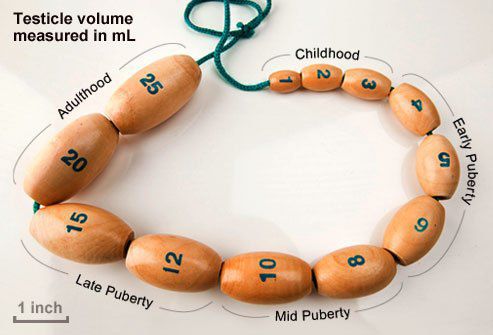
У здоровых мужчин объём каждого яичка составляет в среднем 18 мл и колеблется от 12 до 30 мл. Уменьшение объёма яичек может говорить о наличии андрогенного дефицита.
Вспомогательные методы диагностики
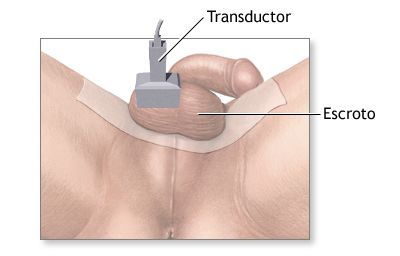
Нормальные яички и их придатки на эхограмме выглядят гомогенными (однородными) структурами.
С помощью ультразвука можно достоверно установить объём яичек, что очень важно. По формуле объёма эллипсоида получают точные результаты, имеющие большое значение для контроля лечения (например, при лечении гипогонадизма гонадотропинами).
Лабораторная диагностика
С помощью лабораторных исследований определяются следующие показатели:
Лечение андрогенного дефицита
Основная цель лечения — улучшение самочувствия пациента и его сексуального здоровья путём восстановления уровня тестостерона в крови до нормальных значений.
Выбор метода терапии определяется формой заболевания, факторами риска и планами пациента по рождению ребёнка.
Следует иметь в виду временное снижения уровня тестостерона на фоне острых или хронических заболеваний, которые должны быть исключены при тщательном обследовании и повторном измерении уровня андрогенов. Терапия складывается из назначения:
Тестостеронотерапия
Показания для назначения препаратов тестостерона:
Противопоказания к назначению заместительной терапии тестостероном:
Принципы терапии
Выбор препарата тестостерона должен быть осознанным решением пациента. Лечащий врач должен показать больному преимущества и недостатки различных форм заместительной терапии и остановиться на оптимальном варианте.
Тестостероны короткого действия могут быть эффективнее пролонгированных форм на начальном этапе заместительной терапии.
Для возмещения андрогенного дефицита существуют различные формы препаратов тестостерона:
Все они имеют разную концентрацию тестостерона и различную биодоступность.
Следует понимать, что каждый человек индивидуален, поэтому важной задачей становится постоянный мониторинг прироста тестостерона на фоне заместительной терапии андрогенами. Учитывается и тот факт, что в среднем за сутки у взрослого мужчины образуется 8-15 мг эндогенного тестостерона.
В настоящее время таблетированные формы для коррекции андрогенного дефицита практически не используются ввиду низкой эффективности и влияния на слизистую желудочно-кишечного тракта. Подкожные импланты также не нашли широкого применения.
Из инъекционных форм получили распространение препараты с длительным андрогенным эффектом: «Небидо» и «Омнадрен 250». Сохраняют своё значение тестостероны короткого и среднего действия — «Тестостерона пропионат» и «Сустанон 250».
Из накожных препаратов неплохо себя зарекомендовал «Андрогель».
«Тестостерона пропионат» — «эталонный» препарат тестостерона короткого действия (работает до 2-3 суток). Он может применяться для лечения андрогенного дефицита в случаях, когда требуется быстро и эффективно поднять уровень тестостерона:
Кроме того, его применяют короткими курсами при олигоспермии.
«Тестостерона пропионат» является самым первым и «старейшим» препаратом тестостерона в мире, который назначают и по сей день. Уже в 1940 году, сразу после синтеза тестостерона из холестерина Нобелевскими лауреатами А. Бутенандтом и Л. Ружичкойс (1939 год), с помощью препарата стали лечить мужской климакс.
«Тестостерона пропионат» является «золотым эталоном» для всех андрогенных и стероидных препаратов. Именно от него отталкиваются все производители при создании новых препаратов андрогенной группы.
Андрогенно/анаболический индекс «Тестостерона пропионата» равен 1/1, то есть он одинаково анаболичен и андрогенен. Эффективность препарата высока в связи с тем, что удельная масса короткого эфира пропионата меньше, чем у длинных эфиров. И чем короче эфир, тем меньше тестостерон работает в организме, и тем больше его концентрация. К примеру, после инъекции 100 мг тестостерона ципионата в организм поступает 69,90 мг действующего вещества, остаток — масса эфира. При инъекции «Тестостерона пропионата» масса основного тестостерона будет равна 83,72 мг, масса эфира пропионата, в свою очередь, гораздо меньше.
Курс терапии индивидуален, его необходимо рассчитывать для каждого больного индивидуально. Однако следует понимать, что реальная эффективная дозировка составляет не менее 400 мг в неделю для взрослого мужчины. Период активности вещества длится до трёх суток. Курс терапии может составлять до шести недель.
Препарат не вызывает такую задержку жидкости, как «длинные» эфиры тестостерона. В целом он обладает меньшими побочными эффектами, чем другие тестостероны, именно благодаря своему короткому периоду активности.
При использовании тестостерона могут проявиться определённые недостатки терапии:
«Сустанон 250» — мощный стероид с большой андрогенной силой. Он представляет собой уникальную комбинацию четырёх эфиров тестостерона. Такое сочетание значительно повышает биодоступность и распределение препарата в организме. На протяжении 40 лет его используют спортсмены различных силовых видов спорта.
Андрогенный эффект наступает спустя 2-3 дня после первой инъекции. Оптимальная периодичность инъекций — 1 раз в 3 недели. Предпочтительный курс лечения — 6-8 недель, максимум — 10 недель. После медикаментозной паузы возможен повторный курс инъекций препарата.
«Сустанон 250» разработан голландской фармацевтической компанией «Органон» ещё в 1970-х годах для постепенного распределения тестостерона в организме. Это достигается благодаря разной скорости распределения и выведения эфиров тестостерона, входящих в состав препарата: период полураспада тестостерона пропионата — 23-49 часов, фенилпропионата — 47-100 часов, изокапроната — 119–132 часов, деканоата — до 11 суток. Максимальная концентрация тестостерона в организме наблюдается уже через два дня после введения «Сустанона».
В целом препарат хорошо переносится, однако у него, как и у всех тестостеронов, есть «но»…
Эфиры тестостерона, входящих в состав «Сустанона 250» быстро преобразуются в эстрадиол — женский половой гормон из группы эстрогенов. Повышенная концентрация эстрогена приводит к таким побочным эффектам, как отёки, увеличение жировой массы и грудных желёз. Предотвратить эти нежелательные эффекты могут анти-эстрогены — кломифен, тамоксифен.
Иногда следует чередовать приём «Сустанона» с антагонистами ароматазы, например с «Аримидексом», эффективно блокирующим выработку эстрогенов.
К другим побочным эффектам препарата следует отнести:
Для лучшего усвоения препарата и предотвращения психических реакций (депрессий и нервных срывов) обязательно посещение спортзала — не реже 3 раз в неделю.
«Омнадрен 250» является полным аналогом препарата «Сустанон 250», производится по лицензии польской фармацевтической компанией Jelfa S.A.
«Небидо» — наиболее популярный препарат-депо касторового масла для внутримышечных инъекций, содержащий тестостерона ундеканоат. После инъекции препарат постепенно высвобождается и затем расщепляется сывороточными эстеразами на тестостерон и ундекановую кислоту.
Возрастание концентрации тестостерона определяться уже на следующий день после инъекции. В 1 мл содержится 250 мг препарата, в последнее время обычно используют дозу 1000 мг (4 мл).
Препарат находится в организме до трёх месяцев. Кратность инъекции — 1 раз в 10-14 недель. «Небидо» присущи все побочные обычные эффекты тестостеронов.
«Андрогель» выпускают в виде геля, упакованного в пакетики. Один такой пакетик (саше) содержит 50 мг чистого тестостерона. Кроме того, появились флаконы этого препарата с дозатором. Наносится ежедневно на кожу предплечий и живота утром и поле душа. Всасывается в организм всего до 15% от нанесённой дозы.
Хорошим «бонусом» является локальный эффект «миолифтинга», которого нет у других препаратов. При нанесении геля на проблемные участки тела происходит улучшение функционального состояния кожи и мышц в этой зоне, «уходят» лишние жировые отложения. Этот эффект позволяет использовать «Андрогель» в комплексной терапии, совместно с пролонгированными формами тестостерона.
Кроме того, препарат можно использовать в комплексной терапии хронического простатита, обострения которого совпадают с сезонными колебаниями тестостерона. «Андрогель» помогает устранить дисбаланс и улучшить состояние.
При длительном применении «Андрогель» может оказать отрицательные эффекты, присущие тестостеронам:
Интересен вопрос о применении, так называемых тестостероновых бустеров (тестобустеров) — химических и биологических добавок, стимулирующих выработку собственного эндогенного тестостерона. И хотя широких международных клинических исследований по тестобустерам не проводилось, и иногда данные об эффектах достаточно противоречивы, их использование может быть оправдано при незначительных и транзиторных колебаниях уровня тестостерона в крови.
Наиболее популярные тестобустеры:
Заместительная витаминная терапия
При восполнении дефицита витамина D достаточно быстро в норму приходят показатели андрогенного обмена, повышается уровень тестостерона.
К препаратам, корректирующим уровень витамина D относятся:
Дозировка препаратов подбирается индивидуально, в зависимости от уровня дефицита витамина D.
Возможна передозировка витамина препаратов витамина D.
К ранним признакам гипервитаминоза витамина D относятся:
К поздним симптомам гипервитаминоза витамина D относят:
Противопоказания к применению препаратов витамина D:
ХГЧ-терапия
Мужские препараты, содержащие ХГЧ, увеличивают выработку тестостерона в яичках путём стимуляции клеток Лейдига. К таким препаратам относятся:
При назначении препаратов ХГЧ следует проводить терапию, стимулирующую сперматогенез.
Прогноз. Профилактика
При вовремя начатом лечении прогноз благоприятный (за исключением наследственных форм андрогенной недостаточности и критических стадий возрастного андрогенного дефицита).
К методам профилактики андрогенного дефицита относятся: