Гипертрофия левого желудочка сердца что это значит у взрослого мужчины на экг
Кардиология
Гипертрофия левого желудочка обычно возникает у пациентов с гипертонической болезнью. Это поражение сердца опасно тем, что может привести к смерти человека. Вообще, согласно статистике, смертность при гипертрофии левого желудочка возникает в 4% случаев.
Это, как мы уже отметили, может быть гипертоническая болезнь или пороки сердца, как врожденные, так и приобретенные, частые и значительные нагрузки. Высок риск развития гипертрофии у спортсменов, грузчиков, представителей других профессий, которые требуют состояния пограничной загруженности.
Очень опасна резкая и интенсивная нагрузка, которой подвергается сердце людей, которые ведут преимущественно сидящий образ жизни, но в определенной жизненной ситуации вынуждены подвергнуть себя физическим нагрузкам. Это же относится к курящим и тем, кто ежедневно употребляет спиртные напитки. Гипертрофия левого желудочка опасна тем, что миокард получает резкую и высокую нагрузку, и если он с ней не справится, то может наступить инфаркт или инсульт.
Гипертрофия левого желудочка бывает как врожденной, так и приобретенной, на фоне развития основного заболевания.
Если говорить о симптомах данного поражения сердца, то его самым ярким проявлением является стенокардия. Она возникает при сжатии сосудов, которые питают сердечную мышцу. Также к симптомам гипертрофии левого желудочка можно отнести мерцательную аритмию и проявления в виде фибрилляции предсердий и голодания миокарда.
В ряде случаев сердце может замирать на несколько мгновений, что приводит к потере сознания пациентом. Отмечаются одышка, головные боли, нарушения сна, боль в сердце, общая слабость и плохое самочувствие.
Сама гипертрофия левого желудочка может быть симптомом одного из следующих заболеваний:
Лечение гипертрофии левого желудочка состоит в применении препаратов, которые снижают симптомы нарушений сердечно-сосудистой системы. Также пациенту рекомендуется соблюдать диету, отказаться от вредных привычек, в том числе от курения и употребления спиртного.
Нельзя исключить при гипертрофии левого желудочка и оперативное вмешательство.
При выявлении любых из перечисленных симптомов следует обратиться к врачу-кардиологу
Записаться на прием Вы можете по телефону 8 (928) 337-60-60.
Гипертрофия миокарда сердца — особенности заболевания
Гипертрофия миокарда сердца — это увеличение, разрастание мышечной массы стенки сердца. Такие изменения приводят к изменению размеров, формы органа, утолщению межжелудочковой перегородки.
Симптомы
Как правило, данная патология обнаруживается случайно, в процессе проведения ЭКГ или Эхо-КГ. Специалисты выделяют такие основные признаки гипертрофии миокарда:
Развитие стенокардии происходит в результате сжатия сосудов, обеспечивающих необходимым питанием сердечную мышцу. В конечном итоге происходит увеличение мышцы в размерах. Она начинает потреблять больше кислорода в комплексе с питательными веществами. У пациентов, страдающих от гипертрофии миокарда сердца, также может возникать состояние, в процессе которого замирает сердце на несколько мгновений (не бьется вообще). В этом случае человек теряет сознание.
Диагностика
Как правило, заболевание выявляется при ультразвуковом исследовании. МРТ сердца считается наиболее простым, информативным методом. В определенных случаях заболевание диагностируют при помощи ЭКГ. К дополнительным исследованиям относят: вентрикулографию, коронарографию, а также радиоизотопное исследование.
Профилактика
К числу эффективных профилактических действий по предотвращению развития заболевания относят:
В случае контроля препаратами удается поддерживать нормальный уровень сахара, а также контролировать остальные факторы риска, возникающие при сахарном диабете. Соблюдение таких профилактических мер позволяет избегать развития гипертрофии миокарда сердца.
Лечение гипертрофии миокарда
Для проведения квалифицированного лечения необходимо продиагностировать заболевание, а также определить его характер, особенности течения. На основе этих данных подбирается оптимальный способ лечения. В большинстве случаев лечение гипертрофии миокарда состоит в приеме препарата верампила с бета-блокаторами. Комплексное применение лекарств позволяет снизить симптоматику заболевания, а также нормализовать общее состояние больного. В роли дополнительной терапии необходимо соблюдать назначенную диету, а также отказаться от курения, приема алкоголя. Кроме того, необходимо сокращение количества соли, потребляемых продуктов с максимально высоким содержанием жиров. При лечении физические нагрузки должны быть умеренными.
В особо тяжелых случаях требуется хирургическое вмешательство. В этом случае специалист удаляет гипертрофированную часть мышцы. В процессе лечения состояние пациента отслеживается при помощи ЭКГ.
Реабилитация
Как известно, после проведенного лечения, операционного вмешательства требуется полноценная реабилитация. Лечебная диета является неотъемлемой составляющей реабилитационного процесса. В таком случае питаться необходимо до 6 раз в день небольшими порциями. Мучные изделия при этом нужно ограничить, жирные, копченые блюда также исключаются из рациона. Уровень физических нагрузок необходимо снизить. Полноценная реабилитация позволяет пациенту намного оперативнее восстановиться после проведенного лечения.
Записаться на приём
Запишитесь на приём и получите профессиональное обследование в нашем центре
Какие признаки увеличенного сердца и чем это опасно
Кардиомегалия — это состояние, при котором по той или иной причине сердце увеличивается в размерах. Большое сердце может быть вариантом нормы. К примеру, у спортсменов, занятых физическим трудом или беременных сердце перекачивает большие объемы крови. После родов, ухода из большого спорта, смены трудовой деятельности размеры постепенно возвращаются к нормальным показателям. Если этого не происходит, пациенту потребуется консультация кардиолога и, возможно, лечение. Проблема может быть врожденной (чаще обнаруживается у детей) и приобретенной — от такого состояния страдают взрослые.
Почему увеличено сердце?
Увеличение размеров сердца отмечается как на фоне сердечно-сосудистых заболеваний, так и из-за болезней, никак не связанных с кровеносной системой. Причины и последствия увеличенного сердца у взрослого:
Причины увеличения сердца могут быть различны, но такое состояние рано или поздно приводит к сердечной недостаточности, которая достаточно опасна. От сердечно-сосудистых заболеваний гибнет больше людей, чем от других болезней, например, онкологии. Проблемы с кровообращением могут привести к сердечному приступу и инсульту, инвалидизации человека. Еще одна угроза — разрастание соединительной ткани, что ведет к снижению эластичности стенок и атрофии мышцы. В группе риска люди преклонного возраста, но это не означает, что молодежи не нужно проходить периодическое обследование.
Признаки увеличенного сердца
На первых порах кардиомегалия протекает без выраженных клинических проявлений. Человек может долгое время вообще не знать о проблеме, а патологию часто обнаруживают случайно, например, на рентгене или флюорографии. Обследуйтесь, если вы входите в группу риска — опасность гипертрофии сердца в том, что она может долгие годы не давать о себе знать и обнаруживается, когда мышца уже достаточно повреждена.
О заболевании сердечной мышцы могут свидетельствовать следующие симптомы:
Синдром «бычьего сердца» хорошо диагностируется кардиологами, но на выяснение причин, вызвавших патологию, может уйти время. Могут понадобиться обследования других органов — щитовидной железы, почек, печени, легких, иммунной системы.
Диагностика, профилактика, лечение
Хотя осложнения кардиологических патологий весьма опасны, в действительности большинство ССЗ можно предотвратить с помощью профилактики. Даже если человек уже заболел, тяжелых последствий можно избежать. Благодаря современному лечению можно затормозить болезнь на ранней стадии и не допустить необратимых последствий.
Физиологическая гипертрофия — это временное состояние: чаще всего спортсменам или людям физического труда требуется обычное наблюдение. Патологически гипертрофированное сердце нуждается в лечении, которое подбирается в зависимости от причин кардиомегалии. Если проблема в сердечных клапанах, проводят операцию и протезирование. АГ, болезни почек и органов дыхания лечат медикаментами. При риске образования тромбов назначают антитромботические препараты. Таким образом, какой-то единой терапии не существует, ведь причины патологии могут быть совершенно разными.
Заниматься самолечением при кардиомегалии бессмысленно, а порой и вредно. Без специальных обследований установить причину патологии невозможно: человек может думать, что осложнение связано с сердцем, а в действительности корни проблемы могут крыться в почках или другом органе. Но пациент может сделать свою жизнь лучше с помощью мер профилактики: умеренных физических нагрузок, контроля давления, коррекции питания, избавления от вредных привычек. Для постановки диагноза делают:
В Октябрьском сосудистом центре республики Башкортостан можно пройти необходимую диагностику, получить консультацию и лечение у профессионалов. В центре пациентам оказывают всестороннюю помощь и обнаруживают признаки гипертрофии уже на первом осмотре. Врачи назначают только необходимый объем исследований, по результатам которых ставят диагноз и подбирают адекватную терапию.
Что такое сердечная недостаточность? Причины возникновения, диагностику и методы лечения разберем в статье доктора Гринберг М. В., кардиолога со стажем в 32 года.
Определение болезни. Причины заболевания
Сердечная недостаточность — синдром, при котором нарушена способность сердца перекачивать кровь. Заболевание проявляется одышкой, повышенной утомляемостю, хрипами в лёгких, отёками голеней и стоп.
Выделяют острую и хроническую формы:
Распространённость
В России хроническая сердечная недостаточность чаще регистрируется у женщин. Возможно, это связано с более пристальным их вниманием к своему здоровью.
Причины хронической сердечной недостаточности
Сердечная недостаточность не является самостоятельным заболеванием, это результат развития многих сердечно-сосудистых болезней. Она возникает в основном из-за атеросклероза, ишемической болезни сердца и гипертонии.
Другие факторы риска:
Причины острой сердечной недостаточности
Острая сердечная недостаточность может возникнуть как обострение хронической формы заболевания, а также на фоне инфаркта миокарда, разрыва хорд митрального клапана и других тяжёлых состояний.
Симптомы сердечной недостаточности
В начале заболевания симптомы сердечной недостаточности отмечаются исключительно при физических нагрузках.
Реакция со стороны сердца. Из-за нарушения кровообращения появляется одышка — частое и глубокое дыхание, не соответствующее уровню нагрузки. При повышении давления в лёгочных сосудах возникает кашель, иногда с кровью. При физической активности и употреблении большого количества пищи может усилиться сердцебиение. Пациент жалуется на чрезмерную утомляемость и слабость. С течением времени симптомы нарастают и теперь беспокоят не только при физической активности, но и в состоянии покоя.
Реакции со стороны печени. Сердечную недостаточность сопровождает застой крови в сосудах печени, из-за чего возникает чувство тяжести и боли под правым ребром.
Патогенез сердечной недостаточности
Сердце, подобно насосу, нагнетает кровь в сосуды и перекачивает её из одной части тела в другую:
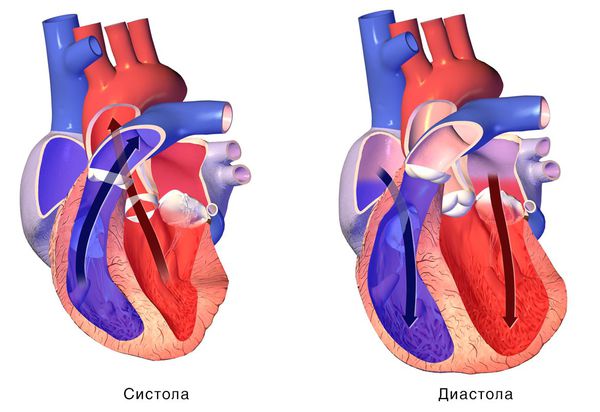
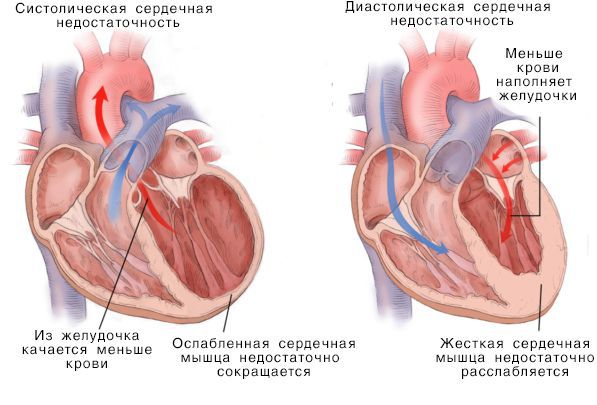
При сокращении сердечной мышцы, называемой систолой, кровь выталкивается из сердца. При расслаблении сердечной мышцы, или диастоле, она возвращается в сердце.
Если расслабляющая или сократительная способность сердца уменьшается, то развивается сердечная недостаточность. Это происходит, как правило, из-за слабости сердечной мышцы и/или потери её эластичности. В результате сердце качает недостаточно крови. Она может также накапливаться в тканях и вызывать застой.
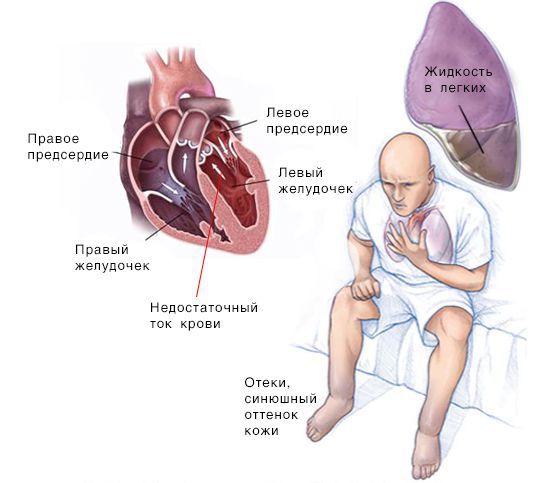
Скопление крови, поступающей в левую часть сердца, приводит к застою в лёгких и затруднению дыхания. Скопление крови, приходящей в правую половину сердца, вызывает застой жидкости в других частях тела, например в печени и ногах.
При сердечной недостаточности, как правило, поражены обе половины сердца. Но одна из них может страдать от заболевания сильнее, чем другая. В таких случаях выделяют правостороннюю и левостороннюю сердечную недостаточность.
Классификация и стадии развития сердечной недостаточности
Выделяют следующие формы сердечной недостаточности:
Недостаточность левого желудочка сердца
Левосторонняя сердечная недостаточность бывает левожелудочковой и левопредсердной. Для неё свойственно снижение выброса левого желудочка и/или застой крови на пути к левым отделам сердца, то есть в венах малого круга кровообращения.
Симптомы при левосторонней сердечной недостаточности (СН): слабость, головокружения, бледность кожи, одышка и быстрая утомляемость.
Недостаточность правого желудочка сердца
Симптомы при правосторонней СН: периферические отёки, цианоз и скопление жидкости в брюшной полости.
Изолированная сердечная недостаточность встречается редко и кратковременно. В последующем нарушение затрагивает все камеры сердца и развиваются типичные симптомы болезни.
Систолическая и дистолическая сердечная недостаточность
Нарушение насосной функции левого желудочка может быть вызвано систолической и диастолической дисфункцией. Систолическая дисфункция более распространена и связана со снижением сократимости миокарда — мышечной ткани сердца. В большинстве случаев причиной систолической хронической сердечной недостаточности становится ИБС, сочетаясь с артериальной гипертензией и сахарным диабетом.
Помимо привычных терминов “диастолическая сердечная недостаточность” и «систолическая сердечная недостаточность», используются названия “сердечная недостаточность с сохраненной фракцией выброса ЛЖ (СНСФВ)” и «сердечная недостаточность со сниженной фракцией выброса (СН СФВ)».
Острая и хроническая сердечная недостаточность
Симптомы при хронической и острой СН различаются лишь интенсивностью и сроками развития.
Стадии развития сердечной недостаточности
Современная классификация хронической сердечной недостаточности объединяет модифицированную классификацию Российской кардиологический школы по стадиям, которые могут только ухудшаться (В. Х. Василенко, М. Д. Стражеско, 1935 г.), и международную классификацию по функциональным классам, которые определяются способностью больного переносить физическую нагрузку (тест с 6-ти минутной ходьбой) и могут ухудшаться или улучшаться (Нью-Йоркская классификация кардиологов). [2]
Классификация ХСН Российского общества специалистов по сердечной недостаточности
| ФК | ФК ХСН (могут изменяться на фоне лечения) | НК | Стадии ХСН (не меняются на фоне лечения) |
|---|---|---|---|
| 1ФК | Ограничений физической активности нет; повышенная нагрузка сопровождается одышкой и/или медленным восстановлением | 1 ст | Скрытая сердечная недостаточность |
| 11ФК | Незначительное ограничение физической активности: утомляемость, одышка, сердцебиение | 11а ст | Умеренно выраженные нарушения гемодинамики в одном из кругов кровообращения |
| 111ФК | Заметное ограничение физической активности: по сравнению с привычными нагрузками сопровождается симптомами | 11б ст | Выраженные нарушения гемодинамики в обоих кругах кровообращения |
| 1У ФК | Симптомы СН присутствуют в покое и усиливаются при минимальной физической активности | 111 ст | Выраженные нарушения гемодинамики и необратимые структурные изменения в органах-мишенях. Финальная стадия поражения сердца и других органов |
Классификация сердечной недостаточности Нью-Йоркской кардиологической ассоциации
Класс I. Заболевание сердца не ограничивает физическую активность. Обычная нагрузка не вызывает усталость, сердцебиение и одышку.
Класс II. Болезнь незначительно ограничивает физическую активность. В покое симптомов нет. Обычная физическая нагрузка вызывает усталость, сердцебиение или одышку.
Класс III. Физическая активность значительно ограничена. В покое симптомов нет. Небольшая физическая активность вызывает усталость, сердцебиение или одышку.
Осложнения сердечной недостаточности
Осложнения хронической сердечной недостаточности:
Диагностика сердечной недостаточности
Лечение сердечной недостаточности
Этапы оказания помощи пациенту с острой сердечной недостаточностью
При сердечной недостаточности не стоит заниматься самолечением. Своевременное обращение к врачу поможет избежать негативных последствий.
Цели терапии
Правильно подобранная медикаментозная терапия способна улучшить качество жизни и значительно продлить её продолжительность у больных даже с тяжелыми формами хронической сердечной недостаточности (по данным литературы — до 10 лет). [4]
Стандарты диагностики и лечения сердечной недостаточности, которые утверждены Минздравом, предписывают определенные исследования и манипуляции для пациентов, обратившихся с симптомами, напоминающими сердечную недостаточность; там же есть список лекарственных средств, но без указания, кто и как должен это лечить. Терапевты в поликлиниках не имеют соответствующей подготовки и не могут грамотно оказывать помощь этим больным.
Нужна ли госпитализация при сердечной недостаточности
Причиной госпитализации является декомпенсация — выраженное нарастание отёков и одышки, тахикардия и нарушение сердечного ритма.
В России сегодня почти нет специализированных отделений, где принимали бы больных с этим заболеванием, проводили бы дифференциальную диагностику и подбирали лечение (в Западной Европе введена врачебная специальность «специалист по сердечной недостаточности»). Кто реально занимается индивидуальным подбором лекарственных препаратов для больного? Терапевт, который назначает преимущественно фуросемид (мочегонный препарат), выводящий калий, снижающий давление и ускоряющий наступление летального исхода?
Кардиологические отделения районных больниц, куда с огромным трудом можно госпитализировать тяжелого больного на очень короткий срок, где опять же назначат фуросемид и лишь выведут избыточно накопленную жидкость, а через 1-2 месяца опять наступит ухудшение (правило 4-х госпитализаций: время между каждой последующей госпитализацией сокращается, состояние ухудшается, после 4-й госпитализации больных не остается!) В то время как современные препараты в постепенно повышающихся дозах могут обеспечить гемодинамическую разгрузку сердца, улучшить состояние пациента, уменьшить потребность в госпитализациях, продлить жизнь больного.
При хронической сердечной недостаточности показано сохранять режим питания и нагрузок и непрерывно принимать лекарственные препараты. Одно-двухдневный пропуск может ухудшить состояние, симптомы могут вернуться, и станет неизбежной госпитализация. Хроническая сердечная недостаточность часто встречается у людей пожилого возраста и сочетается с энцефалопатией, и помощь близких может значительно повысить их приверженность к лечению. Нужно обучение правильному питанию, режиму дня, контролю за задержкой жидкости (за рубежом эти функции выполняет специально обученная медсестра, которая осуществляет патронаж больного).
Острая или тяжелая форма хронической сердечной недостаточности подразумевает постельный режим, полный психический и физический покой. В остальных случаях показаны умеренные нагрузки, которые не сказываются на самочувствии. Следует потреблять не более 500-600 мл жидкости в сутки, соли – 1-2 г. Назначается витаминизированное, легкоусвояемое диетическое питание, олигомерные питательные смеси.
Медикаментозное лечение
Если развивается приступ острой сердечной недостаточности левого желудочка (отёк легких), больной подлежит госпитализации, где ему оказывают неотложную помощь. Лечение заключается в введении диуретиков, нитроглицерина, препаратов, которые повышают сердечный выброс (добутамин, дофамин), проводятся ингаляции O2.
Если развивается асцит, показано проведение пункционного удаления жидкости из брюшной полости, при возникновении гидроторакса — плевральная пункция.
Поскольку сердечная недостаточность сопровождается выраженной гипоксией тканей, пациентам показана кислородная терапия. [10]
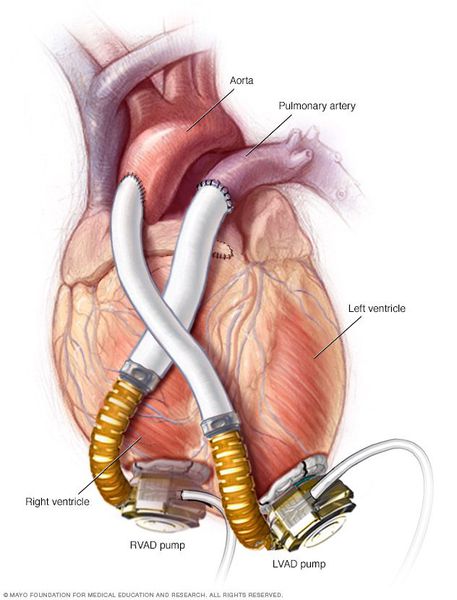
Хирургические и механические методы лечения
Питание и режим дня при сердечной недостаточности
Пациенту с сердечной недостаточностью следует уменьшить употребление жидкости до одного литра в сутки. Также следует исключить солёности, пряности и копчёности.
При заболевании нужно больше двигаться и выполнять посильные нагрузки: чаще ходить пешком и заниматься лёгкой гимнастикой.
Прогноз. Профилактика
До 1990-х годов 60 − 70 % пациентов с хронической сердечной недостаточностью умирали в течение пяти лет. Современная терапия позволила уменьшить смертность: сейчас в России при этой болезни она составляет 6 % в год, а среди пациентов с клинически выраженными формами — 12 % [16]
Отдалённый прогноз зависит от степени тяжести заболевания, образа жизни, эффективности подобранного лечения и приверженности ему, сопутствующих заболеваний и т. д.
Успешное лечение на ранних стадиях может полностью компенсировать состояние пациентов; при третьей стадии сердечной недостаточности прогноз самый печальный.
Чтобы сердечная недостаточность не прогрессировала, нужно соблюдать рекомендованный режим физической активности, регулярно и без пропусков принимать назначенные лекарства и регулярно наблюдаться у кардиолога.
Современные подходы к лечению больных гипертрофической кардиомиопатией
Полувековая история изучения проблемы гипертрофической кардиомиопатии (ГКМП) отражает значительную эволюцию знаний в области этиологии, патогенеза, диагностики, клинического течения, прогноза и вариантов лечения этого заболевания. За указанный период тол
Полувековая история изучения проблемы гипертрофической кардиомиопатии (ГКМП) отражает значительную эволюцию знаний в области этиологии, патогенеза, диагностики, клинического течения, прогноза и вариантов лечения этого заболевания. За указанный период только в англоязычных изданиях опубликованы более 1000 крупных научных работ. ГКМП — одна из основных и, вероятно, наиболее распространенных форм кардиомиопатий, заболеваний миокарда, сопровождающихся его дисфункцией (Report of the 1995 WHO/ISFC Task Force on the Definition and Classification of Cardiomyopathy) [1].
В 2003 г. создан Международный комитет (ACC/ESC), объединивший американских и европейских экспертов по ГКМП, и опубликовано сообщение, суммировавшее основные положения, включая стратегию лечебных мероприятий [2].
Определение заболевания носит описательный характер. Так, по современным представлениям, ГКМП является преимущественно генетически обусловленным заболеванием мышцы сердца, характеризующимся комплексом специфических морфофункциональных изменений и неуклонно прогрессирующим течением с высокой угрозой развития тяжелых, жизнеугрожающих аритмий и внезапной смерти (ВС). ГКМП характеризуется массивной гипертрофией миокарда левого и/или реже правого желудочка, чаще асимметричного характера за счет утолщения межжелудочковой перегородки (МЖП), нередко с развитием обструкции (систолического градиента давления) выходного тракта ЛЖ при отсутствии видимых причин (артериальная гипертония, пороки и специфические заболевания сердца). Основным методом диагностики остается эхокардиографическое исследование. В зависимости от наличия или отсутствия градиента систолического давления в полости ЛЖ, ГКМП разделяют на обструктивную и необструктивную, что имеет важное практическое значение при выборе тактики лечения. При этом различают 3 гемодинамических варианта обструктивной ГКМП: с субаортальной обструкцией в покое (так называемой базальной обструкцией); с лабильной обструкцией, характеризующейся значительными спонтанными колебаниями внутрижелудочкового градиента давления без видимой причины; с латентной обструкцией, которая вызывается только при нагрузке и провокационных фармакологических пробах (в частности, вдыханием амилнитрита, при приеме нитратов или внутривенном введении изопротеренола).
Типичными являются морфологические изменения: аномалия архитектоники сократительных элементов миокарда (гипертрофия и дезориентация мышечных волокон), развитие фибротических изменений мышцы сердца, патология мелких интрамиокардиальных сосудов [3, 4].
В настоящее время наблюдается повсеместный рост числа зарегистрированных случаев этой патологии как за счет внедрения в практику современных методов диагностики, так и, вероятно, в связи с истинным увеличением числа больных ГКМП [8, 9]. Согласно данным последних исследований, распространенность заболевания в общей популяции является более высокой, чем считалось ранее, и составляет 0,2% [10, 11]. ГКМП может диагностироваться в любом возрасте, от первых дней до последней декады жизни, однако преимущественно заболевание выявляется у лиц молодого трудоспособного возраста [12, 13]. Ежегодная смертность больных ГКМП колеблется в пределах от 1 до 6%: у взрослых больных составляет 1–3% [14, 15], а в детском и подростковом возрасте у лиц с высоким риском ВС — 4–6% [16, 17].
Общепризнанна концепция о преимущественно наследственной природе ГКМП [18, 19]. В литературе широкое распространение получил термин «семейная гипертрофическая кардиомиопатия». К настоящему времени установлено, что более половины всех случаев заболевания являются наследуемыми [20, 21], при этом основной тип наследования — аутосомно-доминантный. Оставшиеся приходятся на так называемую спорадическую форму; в этом случае у пациента нет родственников, болеющих ГКМП или имеющих гипертрофию миокарда. Считается, что большинство, если не все случаи спорадической ГКМП, также имеют генетическую причину, т. е. вызваны случайными мутациями.
ГКМП — это генетически гетерогенное заболевание, причиной которого являются более 200 описанных мутаций нескольких генов, кодирующих белки миофибриллярного аппарата [2, 22]. К настоящему времени известны 10 белковых компонентов сердечного саркомера, выполняющих контрактильную, структурную или регуляторную функции, дефекты которых наблюдаются при ГКМП. Причем в каждом гене множество мутаций могут становиться причиной заболевания (полигенное мультиаллельное заболевание).
Наличие той или иной ассоциированной с ГКМП мутации признается «золотым» стандартом диагностики заболевания. При этом описанные генетические дефекты характеризуются разной степенью пенетрантности, выраженностью морфологических и клинических проявлений. Тяжесть клинической картины зависит от присутствия и степени гипертрофии. Мутации, которые ассоциируются с высокой пенетрантностью и плохим прогнозом, выражаются большей гипертрофией левого желудочка и толщиной МЖП, чем те, которые характеризуются низкой пенетрантностью и имеют хороший прогноз. Так, было показано, что лишь отдельные мутации ассоциированы с плохим прогнозом и высокой частотой ВС. К ним относятся замены Arg 403 Gln, Arg 453 Cys, Arg 719 Trp, Arg 719 Gln, Arg 249 Gln в гене тяжелой цепи β-миозина, InsG 791 в гене миозин-связывающего белка С и Asp 175 Asn в гене α-тропомиозина [23, 24, 25, 26]. Для мутаций в гене тропонина Т характерна умеренная гипертрофия миокарда, однако прогноз достаточно неблагоприятен, а вероятность внезапной остановки сердца высока [27]. Другие генетические аномалии, как правило, сопровождаются доброкачественным течением и благоприятным прогнозом или занимают промежуточное положение по тяжести вызываемых ими проявлений.
Таким образом, ГКМП характеризуется крайней гетерогенностью вызывающих ее причин, морфологических, гемодинамических и клинических проявлений, разнообразием вариантов течения и прогноза, что существенно затрудняет выбор адекватных и наиболее эффективных лечебных подходов по контролю и коррекции имеющихся нарушений. При этом отчетливо выделяются 5 основных вариантов течения заболевания и исходов:
Вариабельность прогноза определяет необходимость детальной стратификации риска фатальных осложнений заболевания, поиск доступных прогностических предикторов и критериев оценки проводимого лечения.
По современным представлениям, лечебная стратегия определяется в процессе разделения больных на категории в зависимости от описанных выше вариантов течения и прогноза (рис.).
Все лица с ГКМП, включая носителей патологических мутаций без фенотипических проявлений болезни и пациентов с бессимптомным течением заболевания, нуждаются в динамическом наблюдении, в ходе которого оцениваются характер и выраженность морфологических и гемодинамических нарушений. Особое значение имеет выявление факторов, определяющих неблагоприятный прогноз и повышенный риск ВС (в частности, скрытых прогностически значимых аритмий).
К общим мероприятиям относятся ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска ВС. Для предупреждения инфекционного эндокардита в ситуациях, связанных с развитием бактериемии, при обструктивных формах ГКМП рекомендуется антибиотикопрофилактика, аналогичная таковой у больных с пороками сердца.
До настоящего времени окончательно не решен вопрос о необходимости проведения активной медикаментозной терапии у наиболее многочисленной группы больных с бессимптомной или малосимптомной формами ГКМП и низкой вероятностью ВС. Противники активной тактики обращают внимание на то, что при благоприятном течении заболевания продолжительность жизни и показатели смертности не отличаются от таковых в общей популяции [28, 29]. Некоторые же авторы указывают на то, что использование в этой группе пациентов β-адреноблокаторов и антагонистов кальция (верапамил) может приводить к сдерживанию гемодинамических нарушений и клинической симптоматики [30, 31]. При этом никто не оспаривает тот факт, что выжидательная тактика в случаях бессимптомного или малосимптомного течения ГКМП возможна лишь при отсутствии признаков внутрижелудочковой обструкции, обмороков и серьезных нарушений сердечного ритма, отягощенной наследственности и случаев ВС у близких родственников.
Следует признать, что лечение ГКМП, генетически обусловленного заболевания, обычно распознаваемого на поздней стадии, пока может быть в большей степени симптоматическим и паллиативным. Тем не менее к основным задачам лечебных мероприятий относятся не только профилактика и коррекция основных клинических проявлений заболевания с улучшением качества жизни пациентов, но и положительное влияние на прогноз, предупреждение случаев ВС и прогрессирования заболевания.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов (верапамил). Для лечения весьма распространенных при этом заболевании нарушений сердечного ритма используются также дизопирамид и амиодарон.
β-адреноблокаторы стали первой и остаются и по сей день наиболее эффективной группой лекарственных средств, применяемых в лечении ГКМП. Они оказывают хороший симптоматический эффект в отношении основных клинических проявлений: одышки и сердцебиения, болевого синдрома, включая стенокардию, не менее чем у половины больных ГКМП [32, 33, 34], что обусловлено, в основном, способностью этих препаратов уменьшать потребность миокарда в кислороде. Благодаря отрицательному инотропному действию и уменьшению активации симпатоадреналовой системы при физическом и эмоциональном напряжении, β-блокаторы предотвращают возникновение или повышение субаортального градиента давления у больных с латентной и лабильной обструкцией, существенно не влияя на величину этого градиента в покое. Убедительно показана способность β-блокаторов улучшать функциональный статус пациентов в условиях курсового и длительного применения [35]. Хотя препараты не оказывают прямого влияния на диастолическое расслабление миокарда, они могут улучшать наполнение ЛЖ косвенно — за счет уменьшения частоты сердечных сокращений и предупреждения ишемии сердечной мышцы [36]. В литературе имеются данные, подтверждающие способность β-блокаторов сдерживать и даже приводить к обратному развитию гипертрофии миокарда [37, 38]. Однако другие авторы подчеркивают, что вызываемое β-блокаторами симптоматическое улучшение не сопровождается регрессией гипертрофии ЛЖ и улучшением выживаемости больных [39]. Хотя эффект этих препаратов в отношении купирования и предупреждения желудочковых и суправентрикулярных аритмий и внезапной смерти не доказан, ряд специалистов все же считают целесообразным их профилактическое назначение больным ГКМП высокого риска, включая пациентов молодого возраста с отягощенным случаями внезапной смерти семейным анамнезом [40].
Предпочтение отдается β-блокаторам без внутренней симпатомиметической активности. Наибольший опыт накоплен по применению пропранолола (обзидан, анаприлин). Его назначают начиная с 20 мг 3-4 раза в день, с постепенным увеличением дозы под контролем пульса и артериального давления (АД) до максимально переносимой в большинстве случаев 120–240 мг/сут. Следует стремиться к применению возможно более высоких доз препарата, так как отсутствие эффекта терапии β-блокаторами, вероятно, связано с недостаточной дозировкой. При этом нельзя забывать о том, что повышение дозировок существенно увеличивает риск известных побочных эффектов.
В настоящее время широко изучается возможность эффективного применения нового поколения кардиоселективных β-блокаторов пролонгированного действия, в частности атенолола, конкора и др. При этом существует мнение о том, что кардиоселективные β-блокаторы у больных ГКМП не имеют преимуществ перед неселективными, так как в больших дозах, к достижению которых следует стремиться, селективность практически утрачивается. Следует отметить, что рекомендуемый к применению у больных ГКМП с тяжелыми суправентрикулярными и желудочковыми аритмиями соталол сочетает в себе свойства неселективных β-блокаторов и антиаритмических средств III класса (кордароноподобный эффект).
Применение блокаторов медленных кальциевых каналов при ГКМП основано на снижении уровня свободного кальция в кардиомиоцитах и нивелировании асинхронии их сокращения, улучшении расслабления миокарда и снижении его сократимости, подавлении процессов гипертрофии миокарда. Среди блокаторов кальциевых каналов препаратом выбора, благодаря наибольшей выраженности отрицательного инотропного действия и наиболее оптимальному профилю фармакологических свойств, является верапамил (изоптин, финоптин). Он обеспечивает симптоматический эффект у 65–80% больных, включая случаи рефрактерности к лечению β-блокаторами, что обусловлено способностью препарата уменьшать ишемию миокарда, в том числе безболевую, и улучшать его диастолическое расслабление и податливость ЛЖ [41, 42, 43]. Это свойство верапамила обеспечивает повышение толерантности больных к физической нагрузке и снижение субаортального градиента давления в покое при меньшей по сравнению с β-блокаторами способности к уменьшению внутрижелудочковой обструкции в случаях физического и эмоционального напряжения и провокации изопротеренолом. Одновременно верапамил снижает периферическое сосудистое сопротивление вследствие вазодилататорного действия [44]. И хотя этот эффект чаще всего нивелируется непосредственным положительным влиянием на диастолическую функцию ЛЖ, у отдельных больных с базальной внутрижелудочковой обструкцией в сочетании с повышенным конечно-диастолическим давлением ЛЖ и склонностью к системной артериальной гипотензии при уменьшении постнагрузки внутрижелудочковый градиент давления может резко возрастать. Это способно приводить к развитию отека легких, кардиогенного шока и даже внезапной смерти [45]. Подобные грозные осложнения фармакотерапии верапамилом описаны также у больных необструктивной ГКМП с высоким давлением в левом предсердии, у которых они обусловлены отрицательным инотропным действием препарата. Очевидно, как важно соблюдать осторожность при начале лечения верапамилом этой категории больных. Прием препарата следует начинать в условиях стационара с малых доз — 20–40 мг 3 раза в день с постепенным их повышением при хорошей переносимости до снижения частоты сердечных сокращений в покое до 50–60 уд/мин. Клинический эффект наступает обычно при приеме не менее 160–240 мг препарата в сутки; более удобны в условиях длительного применения пролонгированные формы (изоптин-ретард, верогалид-ретард). С учетом благоприятного влияния верапамила на диастолическую функцию и величину субаортального градиента давления в ЛЖ, а также доказанной способности увеличивать выживаемость больных ГКМП по сравнению с плацебо [46], целесообразно его профилактическое назначение у асимптоматичных больных ГКМП высокого риска.
Место дилтиазема в лечении ГКМП окончательно не определено. Имеются данные, что в средней дозе 180 мг/сут за 3 приема он оказывает столь же выраженное, как 240 мг верапамила, благотворное влияние на диастолическое наполнение ЛЖ и одинаковый симптоматический эффект, однако в меньшей степени улучшает физическую работоспособность больных [47].
В нашей клинике продолжается проспективное наблюдение (от 1 до 5 лет) более 100 больных ГКМП. Больные были рандомизированы на 3 сопоставимые по количеству, полу, возрасту и тяжести клинических проявлений группы. Пациентам произвольно назначались атенолол или изоптин-ретард; в третьей группе преобладали лица с тяжелыми желудочковыми нарушениями ритма, и им был рекомендован прием соталола. Оценка эффективности различных вариантов медикаментозного лечения проводилась в условиях длительного (не менее 1 года) применения препаратов. Суточные дозы при двухкратном режиме приема титровались индивидуально и составили в среднем 85, 187, 273 мг для атенолола, изоптина и соталола соответственно. Длительная терапия привела к улучшению клинического состояния соответственно у 77, 72 и 83% пациентов каждой группы, что выражалось в достоверном уменьшении основных симптомов, проявлений сердечной недостаточности (СН), увеличении мощности и времени выполненной нагрузки и улучшении показателей качества жизни (на 25, 32 и 34% соответственно). При этом выявлены достоверное (p
С. А. Габрусенко, кандидат медицинских наук
Ю. В. Сафрыгина
В. Г. Наумов, доктор медицинских наук, профессор
Ю. Н. Беленков, доктор медицинских наук, профессор
НИИ кардиологии им. А. Л. Мясникова РК НПК МЗ РФ, Москва