Гиперэхогенные тромботические массы что это
Гиперэхогенные тромботические массы что это
— Атероматозные бляшки.
Гипоэхогенные, выступающие внутрь просвета тромбоцитарные тромбы:
• Фиксированные или подвижные на ножке и иногда пластинчатые тромбы.
• Изредка тромбы имеют эхогенную верхушку, иногда в сочетании с расслоением интимы.
• Комбинированные бляшки: атеросклеротические бляшки с кальцинацией, некрозом и изъязвлениями (последнее состояние не диагностируется при УЗИ).
Склероз Менкеберга: диффузные отложения солей кальция в средней оболочке сосудов у пациентов с сахарным диабетом, имеющих симптомы облитерирующего атеросклероза ОАС (однако симптомы тяжелой окклюзии развиваются редко).
• Крайне высокое допплеровское давление заклинивания.
• Диффузная пятнистая эхогенная кальцинация стенок сосудов, иногда с акустической тенью.
Гипоэхогенные изменения просвета
Эмбол: гипоэхогенный дефект внутрисосудистого кровотока. Исследование в В-режиме имеет меньшее значение, чем ЦДЭ, которое может подтвердить отсутствие кровотока.
Склеивание тромбов в аневризмах аорты или артерий:
• Эксцентрически или концентрически расположенный слабоэхогенный материал на стенке сосуда.
• Часто отмечается расслоение.
• При допплеровском УЗИ иногда обнаруживается серповидный анэхогенный участок отсутствия кровотока.
Блуждающие тромбы, «эритроцитарная пыль»: пульсирующее, покачивающееся гипоэхогенное образование или скопления эритроцитов в медленном кровотоке.
Эхогенные изменения просвета
Лоскут интимы: например, при расслоении аорты.
• Гиперэхогенная мембрана в просвете сосуда, обычно с неравномерной толщиной.
• Внутрипросветный протез аорты: гладкая эхогенная оболочка внутри просвета сосуда
• Выступающие эхогенные бляшки.
Периваскулярные изменения сосудов
Метастазы, лимфаденопатия:
• Четко очерченные образования либо объемные гипоэхогенные периваскулярные структуры.
• Увеличение аортоспинального промежутка (>5 мм).
• Симптом бутерброда (сосуд располагается между конгломератами лимфатических узлов, что является возможным признаком высокозлокачественной лимфомы).
Ретроперитонеальный фиброз:
• Диффузные гипоэхогенные образования вокруг аорты.
• Обычно сопровождается обструктивными нарушениями мочевыводящих путей.
Парааортальный или параартериальный абсцесс: гипоэхогенное образование с неровными границами:
• Гипоэхогенное неровное полосовидное образование, окружающее протез.
• Периваскулярное образование в области протезированного анастомоза, часто имеющее признаки артериального кровотока (при ЦДЭ).
Инфекция трансплантата, несостоятельность швов: гипоэхогенное образование вокруг трансплантата.
УЗИ при посттромботическом синдроме
УЗИ вен в Красноярске у пациентов с тромбозом мы проводим в динамике, которая очень важна. По мере растворения тромба в просвете сосуда проходимость вены увеличивается, кровоток восстанавливается, что хорошо видно при цветном картировании. Это не всегда заканчивается полным восстановлением кровотока, чаще наблюдаются утолщение венозной стенки и уменьшение калибра вены после ее тромбоза, и эти изменения будут постоянными. В других случаях наблюдается сохранение полной окклюзии вены.
Продолжительность подострой фазы четко не регламентирована. Под подострой фазой подразумевают тромбоз от 2 недель до 6 месяцев после его начала, затем формируется посттромботический синдром. Переход острой фазы в подострую происходит постепенно, и эхографические характеристики свежего тромба в различной степени могут присутствовать и в подострой фазе. В течение подострой фазы тромб становится более эхогенным. Критерий его эхогенности тромба может быть полезным только в двух случаях: анэхогенный или крайне низкой эхогенности тромб расценивается как острый, он существует всего несколько дней. Высокоэхогенные тромботические массы, как правило, представлены фиброзной тканью, замещающей остаточные нелизированные тромботические массы. Все остальные случаи не могут соотноситься с реальным временем существования тромба.
У большинства пациентов, перенесших венозный тромбоз, в вене на УЗИ сохраняются патологические эхоструктуры. Это состояние корректно обозначается как «хронический посттромбофлебитический рубец», или «посттромботический синдром». Термин «хронический тромбоз» иногда используют спустя 6 месяцев от момента формирования тромба. За этот период нелизированная часть тромба прорастает фибробластами, при этом происходит трансформация тромботических масс в индифферентную фиброзную ткань. Полный лизис венозного тромба при своевременном лечении происходит только примерно в 20% случаев.
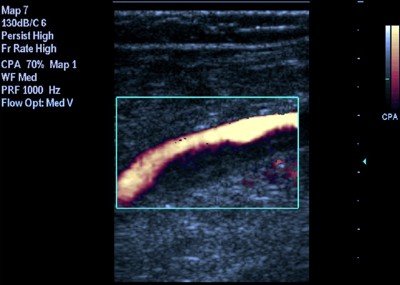
В фазу посттромботических изменений на УЗИ вен часто наблюдается диффузное утолщение венозной стенки. Диаметр утолщенной стенкой вены может быть уменьшен. Эхогенность утолщенной стенки может варьировать, однако в типичных случаях она ниже, чем эхогенность мышечной ткани. Во многих случаях тромботические массы визуализируются в виде выступающих в просвет бляшкоподобных структур, расположенных вдоль венозной стенки. Эти зоны могут быть гиперэхогенными (более эхогенными, чем ткань прилежащих мышц). В некоторых случаях наблюдается кальцификация в виде участка с высоким отражением и акустической тенью.
Другими эхографическими признаками посттромбофлебитического синдрома могут быть рубцовые спайки в виде сетчатой формации внутри просвета сосуда. Спайки формируются из нелизированного тромба, который был прикреплен только по одной стенке вены. Тромб постепенно трансформируется в фиброзный тяж, который прикрепляется в том же месте, откуда ранее отходил тромб.
Если не происходит реканализации тромба, то на УЗИ вен сохраняется значительное сужение или окклюзия сосуда, то в стадии хронических изменений вена превращается в фиброзный тяж значительно меньшего диаметра, чем исходная вена. Она может иметь крошечный просвет либо он вообще не определяется. В некоторых случаях вена вообще перестает визуализироваться.
Главным прогностическим фактором процесса реканализации вены при формировании посттромботической болезни является степень адгезии тромба к венозной стенке. В случаях концентрической адгезии венозного тромба, при ультразвуковом исследовании реканализация обычно происходит в центре сосуда. Если реканализации на фоне диффузной адгезии тромба не происходит, из вены формируется фиброзный тяж.
Вследствие венозного тромбоза практически всегда поражается клапанный аппарат вены. Повреждение клапана проявляется утолщением его створок, адгезией створок к стенке сосуда, ограничением подвижности створок, отсутствием смыкания створок в центре. Физиологическим последствием подобного повреждения становится рефлюкс и постоянный венозный стаз на фоне обусловленного клапанной недостаточностью избыточного венозного давления в подклапанном пространстве. Венозный рефлюкс регистрируется при цветном картировании, спектральной допплерографии. Рефлюкс приводит к развитию вторичной варикозной болезни, проявляющейся патологическим расширением и извитостью вен, хроническим отеком, утолщением и изменением цвета кожи, появлением трофических язв. Поэтому мы рекомендуем пациентам в Красноярске своевременно обратиться на УЗИ вен, а затем и к сосудистому хирургу, чтобы избежать серьезных осложнений.
Гиперэхогенные тромботические массы что это
Флеботромбозы нижних конечностей – одна из ведущих по клинической и научной значимости проблем практической флебологии [1]. Они широко распространены среди взрослого населения, а медикаментозное лечение недостаточно эффективно. При этом сохраняется высокий уровень нетрудоспособности и инвалидности [2, 3]. Отличает флеботромбозы стертость клинической картины в первые часы и дни заболевания, а первым симптомом становится легочная тромбоэмболия (ТЭЛА), являющаяся ведущей причиной как общей, так и хиругической летальности [1]. В связи с этим предельно важна своевременная и точная диагностика эмболоопасных венозных тромбозов с использованием информативных, доступных и неинвазивных способов [4–6]. Ультразвуковое доплеровское сканирование (УЗДС) стало основным методом диагностики указанных флеботромбозов, являющихся потенциальным источником развития легочной тромбоэмболии [1, 4, 7].
В литературе [7, 8] немного публикаций, в которых подробно освещаются ультразвуковые характеристики эмбологенности венозного тромба. Ведущими критериями эмбологенности тромба считаются степень его подвижности и длина и эхогенность флотирующей части, характеристика внешнего контура тромба (ровный, неровный, нечеткий), наличие циркулярного потока крови вокруг тромба в режиме цветового дуплексного картирования как при продольном, так и поперечном сканировании [8–12].
Профилактика ТЭЛА является неотъемлемым компонентом лечения больных с острым венозным тромбозом [13]. К сожалению, использование непрямых антикоагулянтов не способствует профилактике отрыва и миграции в легочные артерии сформированных тромбов [11]. Поэтому при выявлении протяженного флотирующего и эмболоопасного тромбоза показано хирургическое вмешательство, направленное на предотвращение миграции тромбоэмбола (тромбэктомия, пликация или эндоваскулярная имплантация кава-фильтра) [3–6, 14–17].
Вопрос о хирургической тактике при флотирующем тромбозе глубоких вен конечностей должен решаться индивидуально с учетом локализации проксимальной части тромба, её протяженности, флотации, наличия коморбидной и интеркуррентной патологии [9–11, 16–19].
При наличии тяжелой интеркуррентной патологии и противопоказаний к выполнению открытой операции у больных с эмболоопасными тромбозами магистральных вен показана установка кава-фильтра по абсолютным показаниям (противопоказания к антикоагулянтной терапии, эмболоопасные тромбозы при невозможности выполнения хирургической тромбэктомии, рецидивирующие ТЭЛА) [20, 21]. При этом важно учитывать факт фиксации флотирующих тромбов (длина тромба не более 2 см) и возможность консервативной тактики лечения [9–11, 18, 22–24].
Непредсказуемость течения венозных тромбозов в системе нижней полой вены доказывается дигностикой флотирующих тромбозов у пациентов без каких-либо клинических признаков венозной патологии, обнаружением эмболоопасных тромбозов у больных с хроническими заболеваниями вен, факты тромбоэмболий легочной артерии при окклюзирующих формах тромбозов глубоких вен [25, 26].
Цель исследования: улучшение сонографической диагностики и результатов ургентных вмешательств у больных с острыми флеботромбозами.
Материалы и методы исследования
Нами проанализированы результаты физикальной и сонографической диагностики флеботромбозов нижних конечностей у 334 пациентов, находившихся на стационарном лечении в государственном бюджетном учреждении здравоохранения Республики Мордовия «Республиканская клиническая больница № 4». Возраст пациентов составил 20–81 лет; 52,4 % составили женщины, 47,6 % – мужчины; 57,0 % из них были трудоспособного, а 19,4 % – молодого возраста (табл. 1).
Пол и возраст обследованных больных
Распределение флотирующих тромбов в системе глубоких вен нижних конечностей
Глубокие вены бедра
Подколенная вена и вены голени
Подкожные вены бедра
Самой большой оказалась группа пациентов от 61 года и старше (143 человека), среди мужчин преобладали лица в возрасте от 46 до 60 лет – 66 (52,3 %) человек, у женщин – в возрасте 61 года и старше – соответственно 89 (62,3 %) человек.
Флеботромбозы у мужчин в возрасте до 45 лет чаще встречались у лиц, злоупотребляющих внутривенным введением психоактивных веществ. В возрасте 60 лет и более число больных женского пола начинает преобладать над мужским, что объясняется преобладанием у женщин иных факторов риска: гинекологические заболевания (миома матки больших размеров, опухоли яичников), ИБС, ожирение, травмы, варикозное расширение вен и другие. Снижение заболеваемости в общей популяции у мужчин в возрасте 60 лет и более объясняется снижением их доли в соответствующих возрастных группах, высокой летальностью от ТЭЛА, развитием хронической венозной недостаточности и посттромбофлебитического синдрома.
Ультрасонографическая диагностика и эхоскопический мониторинг проводились на ультразвуковых аппаратах Vivid 7 (General Electric, США), Toshiba Aplio, Toshiba Xario (Япония), работающих в режиме реального времени с использованием конвексных датчиков 2–5, 4–6 МГц и линейных датчиков с частотой 5–12 МГц. Исследование начинали с проекции бедренной артерии (в паховой области) с оценки кровотока в поперечном и продольном сечении по отношению к продольной оси вены. При этом оценивали кровоток бедренной артерии. При сканировании оценивались диаметр вены, ее сжимаемость (путем компрессии вены датчиком до прекращения кровотока при сохранении кровотока в артерии), состояние просвета, сохранность клапанного аппарата, наличие изменений на стенках, состояние паравазальных тканей. Состояние гемодинамики вен оценивалось с использованием функциональных проб: дыхательной и кашлевой пробы или пробы с натуживанием. При этом оценивалось состояние вен бедра, подколенной вены, вен голени, а также большой и малой подкожных вен. Оценку гемодинамики нижней полой вены, а также подвздошных, большой подкожной, бедренных вен и вен голени в дистальном отделе проводили в положении пациента лежа на спине. Исследование же подколенных вен, вен верхней трети голени и малой подкожной вены проводилось в положении пациента лежа на животе с валиком, подложенным под область голеностопных суставов. Для исследования магистральных вен и при затруднениях в исследовании использовался конвексный, в остальном – линейные датчики.
Сканирование в поперечном сечении проводили для выявления подвижности головки тромба, о чем свидетельствовало полное соприкосновение венозных стенок при незначительной компрессии датчиком. В ходе обследования устанавливался характер флеботромбоза: пристеночный, окклюзионный или флотирующий.
В перечень лабораторных методов диагностики входили определение уровня Д-димера, коагулограмма, исследование маркеров тромбофилии. При подозрении на перенесенную ТЭЛА в комплекс обследования также входила компьютерная томография в режиме ангиопульмонографии и исследование брюшной полости и малого таза.
С целью хирургической профилактики ТЭЛА при острых флеботромбозах были использованы 3 способа операции: имплантация кава-фильтра, пликация сегмента вены и кроссэктомия и/или флебэктомия. В послеоперационном периоде ультразвуковая диагностика преследовала цель оценки состояния венозной гемодинамики, степени реканализации или усиления тромботического процесса в венозной системе, наличия или отсутствия фрагментации тромба, наличия флотации, тромбоза вен контралатеральной конечности, тромбоза зоны пликации или кава-фильтра и определялись линейная и объемная скорости кровотока и коллатеральный кровоток.
Cтатистический анализ производили с помощью программы Statistica. Оценка различий результатов между группами проведена по критериям Пирсона (проведена по критериям Пирсона) и Стьюдента (t). Статистически достоверными считались различия, уровень значимости которых был более 95 % (р
4.4. Дуплексное сканирование при тромбозе вен нижних конечностей.
Основные задачи ультразвуковой диагностики при подозрении на острый тромбоз глубоких вен включают:
Поскольку свежий тромб по эхоплотности не отличается от крови, ультразвуковыми признаками заболевания являются эктазия вены, отсутствие «дыхания» ее стенок, неполное их смыкание или отсутствие реакции вены на компрессию датчиком (Рис.19). Режим цветового кодирования потоков позволяет дифференцировать дефект заполнения сосуда при неокклюзивном тромбе или отсутствие заполнения при окклюзии просвета сосуда. Неокклюзивный тромб проявляется также наличием на поперечных эхограммах симптома сомкнутого или разомкнутого кольца вследствие «смывания» тромба кровью. Допплеровские спектрограммы демонстрируют снижение кровотока в свободной зоне и его отсутствие в области расположения тромба. Уже в раннем периоде выражен ускоренный коллатеральный кровоток по подкожным венам.
Рис. 19. Острый окклюзивный тромбоз общей бедренной вены.
Флотирующий тромб в условиях специализированной клиники наблюдается редко, что обусловлено поздним обращением больных в результате неоправданной «этапности» оказания медицинской помощи и низкого уровня диагностики в районных поликлиниках. Для флотирующего тромба характерно перемещение головки тромба в просвете вены (Рис.20), его «омывание» кодированным по цвету потоком, низкая скорость кровотока в зоне тромба и дистальнее его, отсутствие дыхательных волн.
В возрасте 5-7 дней в структуре тромба появляются изменения, свидетельствующие о начальных процессах организации: в результате выпадения фибрина эхогенность образования неравномерно повышается, более плотные участки располагаются в виде разводов на гипоэхогенном фоне. Характерные признаки окклюзивного тромба – «зияние» вены, наличие тромботических масс в ее просвете, отсутствие колебательных движений стенок, неспадаемость просвета при компрессии, отсутствие кровотока (Рис. 21).
Важным диагностическим тестом окклюзионного поражения является потеря компрессивности при надавливании датчиком. Компрессивность вены оценивается в продольном и поперечном сечении, сила сдавления датчиком контролируется по деформации просвета корреспондирующей артерии. Однако при оценке этого критерия необходимо учитывать клиническую картину и срок заболевания, так как при «свежих» тромбозах тест нужно использовать с осторожностью в связи с опасностью фрагментации тромба. Кроме того, «свежие» тромбы за счет своей незрелости и мягкой структуры могут давать почти полную сжимаемость просвета.






 в
в