Гетерозиготный полиморфизм что это
Гетерозиготный полиморфизм что это
Большинство оценок частоты мутаций использует обнаружение патологических мутаций с явным влиянием на фенотип. Тем не менее существует масса непатогенных мутаций, считающихся относительно нейтральными; а некоторые могут даже быть полезными. В ходе эволюции устойчивый приток новых изменений нуклеотидов гарантировал высокую степень генетического разнообразия и индивидуальности.
Это распространяется на все области генетики человека и медицинской генетики. Генетическое разнообразие может проявляться в виде изменений в окраске хромосом, изменения числа копий сегментов ДНК, нуклеотидных замен в ДНК, изменений в белках или же как болезнь.
ДНК последовательности каждого участка хромосомы в высшей степени сходны у большинства людей в мире. Фактически произвольно выбранный сегмент ДНК человека размером около 1000 пар оснований содержит, в среднем, только одну пару, отличающуюся на двух гомологичных хромосомах, унаследованных от родителей (если предположить, что родители не родственники).
Эта почти в 2,5 раза больше, чем оценка доли гетерозиготных нуклеотидов для кодирующих белок областей генома (примерно 1 на 2500 пар оснований). Различие неудивительное, поскольку интуитивно понятно, что регионы, кодирующие белок, находятся под более жестким давлением отбора, и таким образом встречаемость мутаций в таких регионах в эволюции должна быть более низкой.
Когда вариант встречается настолько часто, что его обнаруживают более чем в 1% хромосом в общей популяции, его называют генетическим полиморфизмом. Аллели с частотами менее чем 1% принято называть редкими вариантами. Хотя много патологических мутаций, приводящих к генетическим болезням — редкие варианты, нет простой корреляции между частотой аллеля и его влиянием на здоровье. Много редких вариантов не имеют патогенных эффектов, тогда как некоторые варианты, достаточно частые, чтобы считаться полиморфизмами, предрасполагают к тяжелым болезням.
Существует много типов полиморфизма. Некоторые полиморфизмы — следствие вариантов, вызванных делециями, дупликациями, утроениями и так далее, сотен миллионов пар оснований ДНК, и не связаны с каким-либо известным патологическим фенотипом; другие изменения аналогичного размера оказываются редкими вариантами, явно вызывающими тяжелые болезни. Полиморфизмами могут оказаться изменения в одном или нескольких основаниях ДНК, расположенных между генами или в интронах, не связанные с функционированием генов и обнаруживаемые только прямым анализом ДНК.
Изменения последовательности нуклеотидов могут располагаться в кодирующей последовательности самого гена и приводить к образованию различных вариантов белков, в свою очередь вызывающих четко очерченные фенотипы. Изменения в регуляторных областях также могут быть важными в определении фенотипа, влияя на транскрипцию или стабильность мРНК.
Полиморфизм — ключевой элемент в исследовании и практическом использовании генетики человека. Способность различать унаследованные формы генов или других сегментов генома обеспечивают инструментальные средства, необходимые для широкого спектра приложений. Как показано в этой и последующих главах, генетические маркеры — мощное научно-исследовательское инструментальное средство картирования генов на конкретном регионе хромосомы при анализе сцепления или аллельной ассоциации.
Они уже широко используются в медицине — от пренатальной диагностики наследственных болезней до обнаружения гетерозиготного носительства, а также в банках крови и тканей для типиро-вания перед переливаниями и пересадками органов (см. далее в этой главе).
Полиморфизм — основа для развивающихся мероприятий по обеспечению основанной на геномике персонализированной медицины, когда медицинские мероприятия индивидуально подбирают на основе анализа полиморфных вариантов, увеличивающих или уменьшающих риск частых болезней взрослого возраста (например, заболевания коронарных сосудов сердца, опухолей и сахарного диабета), возникновения осложнений после хирургических вмешательств или влияющих на эффективность и безопасность конкретного лекарственного препарата. Наконец, анализ полиморфизма стал мощным новым средством в судебных приложениях, например, определении отцовства, определении останков жертв преступления или для сопоставления ДНК подозреваемого и преступника.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гетерозиготный полиморфизм что это
Занимают третье место по частоте сердечно-сосудистых заболеваний и возникают при нарушении кровообращения (застоий крови), повреждении эндотелия сосудистоий стенки, повышенноий способности крови к образованию тромба (гиперкоагуляция и ингибирование фибринолиза), а также при сочетании этих причин.
Вероятность венозного тромбоза может многократно увеличиваться при наличии у больного наследственной или приобретенной тромбофилии.
Тромбофилия – хроническое состояние организма с тенденцией к спонтанному образованию тромбов в сосудах или к бесконтрольному распространению тромбов за пределы поврежденного участка.
Тромбофилия является потенциально опасным состоянием для людей любого возраста, поскольку может приводить к развитию тромбоза, инфаркта или инсульта в молодом возрасте, а также повышает риск осложнений и невынашивания беременности у женщин.
Механизм тромбообразования
Какая же роль образования тромбов?
Для чего они нужны?
В организме человека, при нормальном его функционировании, поддерживается постоянство внутренней среды, что называется гомеостазом.
Одним из факторов гомеостаза является и тромбообразование, что необходимо для сохранения крови в жидком состоянии и формирования гемостатической «пробки», которая закрывала бы поврежденный сосуд при патологическом процессе или травме, таким образом предотвращая потерю крови. Но следует учесть, что формирование гемостатической пробки не должно препятствовать кровоснабжению определенного органа.
Существует также и другая система, которая препятствует чрезмерному тромбообразованию и способствует рассасыванию тромбов. Совместное «правильное» функционирование этих систем поддерживают нормальные процессы гемостаза в организме человека.
Если же возникает сбой в системе гемостаза, то развиваются тромбофилии, которые могут вызвать тромбоз органов, закрывая просвет сосудов тромбом.Поэтому тромбофилия является потенциально опасным состоянием для людей любого возраста.
Факторы этого патологического состояния связаны, в первую очередь, с нарушением активности гемостатических белков (антикоагулянтов, прокоагулянтов), а также с разнообразными аномалиями в развитии сосудов.
Формы тромбофилии
Существует две формы тромбофилии: наследственная и приобретенная.
Наследственные формы тромбофилии могут быть обусловлены полиморфизмами в генах кодирующих аминокислотную последовательность белков:
F2 протромбина, F5 коагуляционного фактора 5 (фактора Лейдена) и некоторых других.
Мутации этих генов часто встречаются в сочетании друг с другом. Хотя под термином «тромбофилия» и подразумевают генетически обусловленное состояние, но выделяют и приобретенные состояния с повышенной склонностью к образованию тромбов.
К приобретенным факторам риска
формирования тромбов можно отнести:
Но основную группу составляют все-таки
наследственные факторы риска образования тромбов.
К наследственным тромбофилиям относятся
следующие состояния :
Диагностика наследственной тромбофилии
Диагностика наследственной тромбофилии включает в себя комплекс лабораторных тестов: исследование генетических полиморфизмов в генах гемостаза (F2, F5, F7, F13A1, FGB, PAI-1, ITGA2-a2, ITGB3-b) и в генах фолатного цикла (MTHFR, MTR, MTRR), оценка показателей коагулограммы (протромбин, МНО, АЧТВ, фибриноген, тромбиновое время), определение уровня антитромбина III, протеинов C и S, гомоцистеина и волчаночного антикоагулянта.
Полиморфизм бывает двух видов: гомозиготный и гетерозиготный.
Первый очень «серьезный» вариант, ведь в таком случае человек имеет два доминантных или рецессивных гена, которые отвечают за проявление тех или иных признаков.
Второй вариант полиморфизма менее «серьезный», но указывает на носительство «неблагоприятного», в развитии заболевания, признака. И не стоит думать, что это все мутации, ведь такой вариант в строении гена может представлять и естественную вариацию. Поэтому определив вариацию генного полиморфизма, можно повлиять на эффективность лечения и профилактику возможных тромботических осложнений.
Показания к анализу на
полиморфизм генов
Важные в развитии генетической
тромбофилии полиморфизмы:
F2 c.*97G>A (p.20210 G>A; rs1799963)
F2 или протромбин в системе свертываемости крови входит в перечень одного из главных ее компонентов.
Ген F2 кодирует аминокислотную последовательность белка протромбина. В процессе расщепления протромбина образуется тромбин, который необходим для формирования кровяного сгустка. Полиморфизм F2 p.20210 G>A приводит к увеличению экспрессии гена F2, в результате чего уровень протромбина становится в несколько раз выше нормы. Мутация имеет аутосомно-доминантный тип наследования, соответственно тромбофилией страдает даже гетерозиготный носитель измененного гена (G>A). Носители А варианта полиморфизма обладают большим риском летального случая в периоде после операции, а также во время лечения новообразований и других болезней, без учета генетической склонности человека к тромбозу.
Гетерозиготными носителями, по данным статистики, являются около 3% людей европеоидной расы.
Клинически данный полиморфизм проявляется необъяснимым бесплодием, гестозами во время беременности и состоянием преэклампсии, преждевременной отслойкой плаценты, невынашиванием беременности, фетоплацентарной недостаточностью, задержкой внутриутробного развития плода или даже его гибелью; венозными и артериальными тромбозами и тромбоэмболией, нестабильной стенокардией, инфарктом миокарда.
F5 с.1691G>A (p.Arg506Gln; rs6025)
Функция этого фактора заключается в активации перехода протромбина в тромбин. При полиморфизме данного гена в 1691 позиции (Лейденовская мутация) заменяется нуклеотидное основание гуанина на аденин, что приводит к замене аргинина на глутамин в положении 506 и повышенной устойчивости активной формы проакцелерина. Таким образом, активная форма фактора Лейдена вызывает гиперкоагуляцию крови и приводит к рецидивирующим венозными тромбозами и тромбоэмболиям. Распространенность мутации этого гена среди европеоидной расы составляет до 6%.
Клинически полиморфизм F5 c.1691G>A (p.Arg506Gln) проявляется тромбоэмболиями, инфарктом миокарда, инсультами. Также представляет угрозу при беременности, усложняя ее течение, и может спровоцировать не только выкидыш на ранних сроках, но и повлиять на развитие плода, вызвая его отставание.
Пациенты, являющиеся одновременно носителями полиморфизма c.*97G>A гена протромбина и «мутации Лейдена» в гене F5, в большей степени подвержены риску развития тромбозов и тромбоэмболий и нуждаются в тщательном наблюдении и лечении.
PAI-1 (SERPINE1) c.–675 5G>4G (rs1799889)
Ген ингибитора активатора плазминогена (PAI-1) кодирует белок-антагонист тканевого и урокиназного активатора плазминогена и является важным компонентом противосвертывающей системы.
Мутации в данном гене приводят к снижению активности противосвертывающей системы, повышая риск кровотечений.
Распространенность полиморфизма среди людей европеоидной расы составляет от 5 до 8%.
Последние исследования показали, что три вышеперечисленных полиморфизмы имеют наибольший эффект на систему свертывания крови и подлежат глубокому изучению.
F7 c.10976 G>A (p.Arg353Gln; rs6046)
При активации фактора VII происходит его взаимодействие с III фактором, активизируя при этом IX и X факторы системы гемостаза. Таким образом, коагуляционный фактор VII принимает непосредственное участие в образовании кровяного сгустка. При наличии варианта p.353Gln понижается экспрессия гена VII фактора, что обладает протективным свойством в процессе развития инфаркта миокарда и тромбозов.
Распространенность такого варианта среди лиц европейской популяции составляет от 10 до 20 %.
F13 с.103G>T (p.I63Т; rs5985)
Фактор свертываемости крови 13 (F13) представляет собой фермент, отвечающий за последнюю стадию в процессе коагуляции крови. Этот фактор является плазменным гликопротеином, который циркулирует в крови. Кроме основной функции во время свертывания крови, данный фактор еще и стабилизирует клеточную поверхность мембран.
Распространенность в европейской популяции составляет около 20%.
Распространенность мутации данного гена среди европейской популяции составляет от 5 до 10%.
ITGA2 с.807C>T (p.Phe224Phe; rs1126643)
Ген ITGA2 отвечает за кодирование аминокислотной последовательности а2-субъединицы специализированных тромбоцитарных рецепторов (интегринов), благодаря которым тромбоцит взаимодействует с белками тканей во время повреждения сосудистой стенки. Благодаря своим рецепторам, тромбоциты могут образовать в области повреждения монослой, что является важным условием в активации следующих компонентов в цепной реакции свертывания крови, из-за которой организм предохраняется от обильных кровопотерь.
Частота встречаемости данного полиморфизма составляет от 5 до 7%.
При наличии нуклеотидной замены цитозина (С) на тимин (Т) в позиции 807 данного гена, изменяются свойства рецепторов тромбоцитов, увеличивается скорость их склеивания, что приводит к повышению риска возникновения тромбофилии.
ITGB3 с.1565T>C (p.Leu33Pro; rs5918)
ITGB3 – это тромбоцитарный рецептор фибриногена. Его также называют гликобелком-3а (GPIIIa), он участвует в процессах сигнализации и межклеточной адгезии. Именно этот белок обеспечивает взаимосвязь между тромбоцитом и фибриногеном, который содержится в плазме крови, вследствие чего происходит быстрая агрегация (склеивание) тромбоцитов, и закупорка поверхности поврежденного эпителия. Распространенность – от 8 до 15%.
Полиморфизм в ITGB3 вызывает повышенную склонность тромбоцитов к склеиванию, а это, в свою очередь, повышает риск возникновения заболеваний сердечно-сосудистой системы. Часто у людей, при таком полиморфизме, отмечается снижение эффективности действия аспирина, как тромболитического средства.
Распространенность мутации ITGB3: 1565 T>C (Leu33Pro) в европейской популяции – от 8 до 15%.
Важно также отметить, что данная нуклеотидная замена усугубляет влияние других полиморфизмов (к примеру, мутации Лейден).
Таким образом, диагностика тромбофилий крайне важна и помогает правильно назначить терапию, провести профилактику венозных тромбоэмболических осложнений, а также определиться с тактикой ведения беременности.
Заказать анализ генетических полиморфизмов, ассоциированных с риском тромбообразования можно можно в Медико-генетическом центре «Геномед».
Стоит отметить, что вероятность развития осложнений при беременности увеличивается в сочетании с полиморфизмами в генах фолатного цикла (MTHFR, MTR, MTRR), в связи с чем лучше всего их рассматривать в комплексе
Стоимость 6 900 рублей
Срок выполнения 10 дней
Заказать исследования
Заболевания, ассоциированные
с повышенным тромбообразованием
Нарушения в свертываемости крови являются одной из причин осложнений во время беременности. Имея в основе разные факторы, она сгущается и двигается по сосудам, замедляя скорость. А это в свою очередь, может вызвать образование тромбов, которые закупоривают сосуды и приводят к тяжелым последствиям.
Такие нарушения в свертываемости крови приводят к тому, что у женщины не приживается в матке плодное яйцо, происходят нарушения в плаценте, либо регулярные выкидыши на ранних сроках.
И причиной этому является антифосфолипидный синдром – это клинический иммунный симптоматический комплекс, характеризующийся тромбозами венозного и артериального характера, последствиями которого является потеря плода с неясным генезом.
Этот синдром может развиваться и имея в основе генетическую предрасположенность.
В организме человека произошло мутирование определенных генов, которые отвечают за свертывание крови. А потом эти нарушения из поколения в поколение передаются по наследству.
Чаще всего это обнаруживается при определенных ситуациях – беременность, операция, травма или прием гормонов. То есть при тех обстоятельствах, когда свертываемость крови увеличивается. Это хорошая почва на которой проявляется неблагоприятная наследственность.
Антифосфолипидный синдром при беременности провоцирует появление тромбозов в несколько раз.
Соответственно, повышается вероятность невынашивания плода. Однако это не означает, что женщинам с проблемой свертывания крови нельзя помочь. Современная медицина имеет возможность провести тщательную диагностику таких нарушений. По ее результатам можно провести отбор женщин в потенциальную группу риска. А затем приложить максимум усилий, чтобы свести на нет проявления антифосфолипидного синдрома и беременность сделать максимально безопасной, исключить возможность осложнений.
Будущей маме придется произвести корректировку образа жизни, питания и начать прием назначенных препаратов.
Прием таких лекарств необходим на протяжении всего срока беременности, особенно тем, у кого были случаи невынашивания беременности. Обязательной диагностике особенно должны подлежать женщины, если у них рождались мертвые младенцы или они вскоре умирали.
Если есть осложнения, которые связаны с антифосфолипидным синдромом, и беременность планируется в ближайшее время, в таких случаях за месяц до ее наступления необходимо начать прием противотромботических препаратов, назначенных врачом. И не прекращать лечение в течение всего периода положения беременности. Тогда шансы на благополучный исход очень велики, ведь правильное и своевременное лечение дает эффективность почти 100%!
Термин «Тромбоз» используется для обозначения появления сгустков в сосудистой системе. Чаще всего встречается тромбоз вен.
Тромбоз – серьезное заболевание, которое может привести к сердечной недостаточности (коронарный тромбоз), инсульту или гангрене, если он поразит кровеносные сосуды конечностей.
Острый тромбоз требует срочного врачебного вмешательства. Вызовите «скорую помощь» или вашего домашнего врача. Положите пациента поудобнее, обеспечьте ему тепло. Не давайте пациенту никакой еды и питья. Не разрешайте ему двигаться до тех пор, пока не придет помощь.
Никаких средств альтернативной медицины применять нельзя, пока не получено заключение врача. Длительное наблюдение за состоянием и профилактика возможного в будущем тромбоза зависит от правильного питания, физических упражнений, снижения потребления алкоголя и табака. Излишний вес также является фактором риска.
Новая генетика (геномика) в профилактике осложнений беременности
Особенностью многих вариантных генов является то, что они могут долгое время никак себя не проявлять. Патологические симптомы могут возникнуть при дополнительных условиях (особенности питания, беременность, прием лекарств, образ жизни и т. д.). Выяснение этих дополнительных условий помогает эффективно предотвращать развитие заболеваний и их осложнений у носителей вариантных генов.
Тромбофилия как фактор риска осложнений беременности
Тромбофилией называется склонность к развитию тромбов (кровяных сгустков). Тромбофилия может быть угрожающим жизни состоянием, если тромб запирает кровоток. Тромбофилия может быть наследственным нарушением, но может быть связана и с внешними причинами, такими как хирургические операции, ожирение, беременность, использование гормональных контрацептивов, антифосфолипидный синдром, повышение уровня гомоцистеина или долгий период неподвижности. Врачи подозревают наличие тромбофилии у пациентов, имевших тромбозы в прошлом, или у родственников которых были случаи тромбозов, инсультов, инфарктов в молодом возрасте (до 40 — 50 лет). Однако у многих людей с тромбофилией нет никаких симптомов, или эти симптомы проходят незамеченными, поскольку тенденция к тромбофилии недостаточно сильно выражена. Исследования последних лет показали, что наличие тромбофилии сопряжено с повышенным риском развития осложнений беременности (привычное невынашивание, плацентарная недостаточность, задержка роста плода, поздний токсикоз (гестоз)). К числу генных маркеров наследственных тромбофилий относятся мутация метилентетрагидрофолатредуктазы, лейденская мутация и мутация гена протромбина G20210A.
Исследования последних лет показали, что у пациенток с привычным невынашиванием беременности часто обнаруживаются один или несколько генетических маркеров тромбофилии. Например, в одном из исследований было обнаружено наличие лейденской мутации у 19% пациенток с невынашиванием беременности, тогда как в контрольной группе лейденская мутация была обнаружена только у 4% женщин.
Мутация метилентетрагидрофолат-редуктазы
фермента с нарушениями обмена гомоцистеина. Примерно в те же годы было показано, что повышение уровня гомоцистеина является независимым фактором риска развития сосудистых осложнений. Начались попытки выяснения генетической природы дефицита MTHFR. Клонирование гена MTHFR в 1993 г. стало основой для определения мутаций, связанных с различными степенями дефицита данного фермента.
Фолатный цикл
Фермент 5,10-метилентетрагидрофолат-редуктаза относится к группе флавопротеинов и состоит из двух одинаковых субъединиц с молекулярной массой около 70 кДа. MTHFR является ключевым ферментом фолатного цикла. Фолат и фолиевая кислота (синтетический витамин, отсутсвующий в естественных продуктах) являются двумя формами семейства веществ, связанных с птероилглютаминовой кислотой (ПтеГлу). Эта кислота является сложной молекулой, состоящей из птероидной кислоты и одного (моноглютаматы) или нескольких (до 9, полиглютаматы) остатков глютаминовой кислоты (см. рис. 1). Пища, особенно свежая зелень, печень, дрожжи и некоторые фрукты в основном содержат восстановленные полиглютаматы, которые должны быть гидролизованы с помощью фермента птероилполиглютамат-гидролазы до моноглютамата, чтобы они могли быть абсорбированы в проксимальном отделе тонкого кишечника. После всасывания фолат-моноглютамат быстро восстанавливается до тетрагидрофолата, поскольку только восстановленные формы фолата обладают биологической активностью. После метилирования фолаты поступают в кровь в виде 5-метилтетрагидрофолата. Кроме пищи, постоянное поступление 5-метилтетрагидрофолата обеспечивается кишечно-печеночным циклом: птерил-моноглютамат всасывается из кишечника и поступает в печень, где он восстанавливается и метилируется до 5-метилтетрагидрофолата. Образовавшийся 5-метилтетрагидрофолат выделяется с желчью в кишечник, где он затем всасывается и разносится с кровью по всему организму.
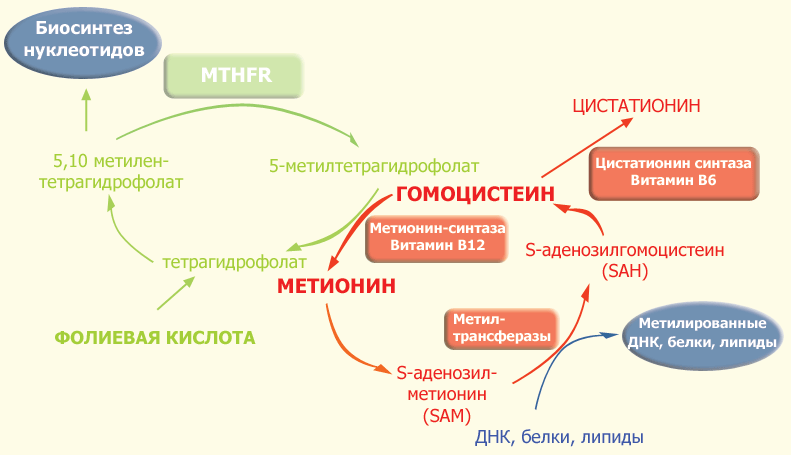 |
| Рис. 1. Фолатный цикл и цикл метионина. |
В ткани поступление 5-метилтетрагидрофолата внутрь клетки происходит с помощью эндоцитоза при участии специфических фолатных рецепторов. Описаны три изоформы фолатных рецепторов. Внутри клетки 5-метилтетрагидрофолат служит донором метильных групп и основным источником тетрагидрофолата. Последний выступает в качестве акцептора большого числа моноуглеродных групп, превращаясь в разные виды фолатов, служащих в свою очередь специфическими коферментами в целом ряде внутриклеточных реакций. К ним относятся 5-формилтетрагидрофолат (фолиниевая кислота, лейковорин), 10-формилтетрагидрофолат и 5,10-метилентетрагидрофолат.
Одной из реакций, требующих наличия 5,10-метилентетрагидрофолата и 5-метилтетрагидрофолата, является синтез метионина из гомоцистеина (путь реметилирования в обмене гомоцистеина). В этой реакции MTHFR играет ключевую роль, восстанавливая 5,10-метилентетрагидрофолат до 5-метилтетрагидрофолата, являясь таким образом катализатором единственной внутри клетки реакции образования 5-метилтетрагидрофолата. Хотя в сыворотке и других тканевых жидкостях обнаруживаются разные формы фолатов, главной формой фолата в плазме является 5-метилтетрагидрофолат, несущий на себе метильную группу, необходимую для превращения гомоцистеина в метионин. В этой реации метильная группа вначале переносится на коб(I)аламин (форма витамина B12), превращая его в метилкобаламин, который затем отдает метильную группу гомоцистеину, образуя метионин с помощью фермента метионин-синтазы. Однако в некоторых случаях коб(I)аламин может окисляться в коб(II)аламин, что приводит к подавлению метионин-синтазы. Для поддержания активности фермента необходимо восстановительное метилирование с помощью фермента метионин-синтаза-редуктазы.
Поскольку кобаламин (витамин B12) служит акцептором метильной группы 5-метилтетрагидрофолата, дефицит этого витамина приводит к «ловушке для фолата». Это тупиковый путь метаболизма, поскольку метилтетрагидрофолат не может при этом восстанавливаться до тетрагидрофолата и возвращаться в фолатный пул. Неспособность регенирировать метионин приводит к истощению запаса метионина и выбросу в кровь избытка гомоцистеина.
