Гепатопетальный кровоток что это такое
Особенности портального кровотока при хронических гепатитах и циррозах печени
Опубликовано в журнале:
Визуализация в клинике »» N18, Июнь 2001 PORTAL BLOOD FLOW IN PATIENTS WITH CHRONIC HEPATITIS AND LIVER CIRRHOSIS
Б.H. Левитан, Б.А. Гринберг
Levitan В.N., Grinberg B.A.
Астраханская медицинская академия, г. Астрахань
strakhan Medical Academy, Astrakhan
У 43 больных хроническим гепатитом (ХГ) и 71 больного циррозом печени (ЦП) проведены импульсная допплерография и цветовое допплеровское картирование (дуплексный допплер) сосудов портальной системы на ультразвуковом сканере «Logic 500» (США). Обнаружены значительные нарушения допплерографических показателей венозного и артериального кровотока, выраженные в наибольшей степени у больных ЦП. Анализ характера изменений показателей допплерографии позволил выделить пять типов портального кровотока при ЦП: 1) нормокинетический (13% больных) без существенных изменений портального кровотока; 2) гиперкинетический с преимущественным увеличением параметров линейной скорости кровотока в воротной вене (ВВ) при незначительном нарастании ее диаметра (12%); 3) гиперкинетический с преимущественным увеличением диаметра ВВ (20% больных). Конгестивный индекс был увеличен. Объемный кровоток в ВВ возрастал, главным образом, за счет ее расширения. Линейная скорость кровотока по ВВ при этом была незначительно сниженной или оставалась неизмененной; 4) гипокинетический (40% больных), при котором значительно снижалась линейная скорость кровотока в ВВ без увеличения ее диаметра, что приводило к уменьшению объемного кровотока в ВВ; 5) псевдонормокинетический (15% больных), при котором объемный кровоток в ВВ оставался в нормальных пределах, а конгестивный индекс был значительно повышен; существенно снижалась линейная скорость кровотока в ВВ при увеличении ее диаметра. Полученные данные открывают дополнительные возможности диагностики и лечения больных ХГ и ЦП.
Forty-three patients with chronic hepatitis (СП) and 71 patients with liver cirrhosis (LC) were provided pulse Doppler and Color Doppler Imaging (duplex Doppler) of the portal vessels using an ultrasound «Logic 500» scanner (USA). Noticeable disorders in the Doppler parameters of the venous and arterial blood flow were discovered. They were pronounced in LC patients to the largest extent. Analysis of the character of changes in the Doppler parameters made it possible to distinguish five types of the portal blood flow in LC: 1) normokinetic (13% of patients) without appreciable changes in the portal blood flow; 2) hyperkinetic with a predominant increase in the parameters of the linear blood flow velocity in the portal vein (PV) at a negligible enlargement of its diameter (12% of patients); 3) hyperkinetic with a predominant enlargement of PV diameter (20% of patients). The congestive index was increased. The volume blood flow in the PV rose mainly because of its enlargement. The linear velocity of PV blood flow was lowered insignificantly or remained unchanged; 4) hypokinetic (40% of patients) marked by an appreciable decrease in the linear velocity of PV blood flow without PV diameter enlargement, which led to the reduction of the volume blood flow in the PV; 5) pseudonormokinetic (15% of patients): in this case the volume blood flow in the PV remained within normal whereas the congestive index was substantially higher; the linear velocity of the blood flow in the PV dropped substantially at its diameter enlargement. The data obtained have contributed much to the diagnosis and treatment of patients suffering from CH and LC. («Визуализация в клинике», 2001, 18: 16-20)
Ключевые слова: хронический гепатит, цирроз печени, портальный кровоток, допплерография.
Key words: chronic hepetitis, liver cirrhosis, portal blood flow, Doppler.
Хронические диффузные заболевания печени (ХДЗП) занимают одно из ведущих мест среди заболеваний желудочно-кишечного тракта, что связано с их широким распространением, тяжестью течения и часто неблагоприятным исходом [1, 7]. В последние годы среди неинвазивных методов диагностики ХДЗП и портальной гипертензии важное место отводится ультразвуковым исследованиям [2-5, 8, 9]. Данные мировой литературы свидетельствуют, что дуплексное сканирование сосудов портальной системы в сочетании с цветовым допплеровским картированием является золотым стандартом для выявления нарушений портального кровотока при заболеваниях печени [10].
Однако до настоящего времени в литературе сохраняются противоречивые данные о параметрах кровотока в сосудах портальной системы при ХДЗП. Не выделены основные типы портальной гемодинамики при циррозах печени.
Целью работы явились изучение допплерографических особенностей портального кровотока у больных хроническим гепатитом (ХГ) и циррозом печени (ЦП), выделение и характеристика основных типов портального кровотока у больных ЦП.
Материал и методы
Комплексное ультразвуковое исследование выполнялось строго натощак на ультразвуковом сканере «Logic-500» (США) конвексным датчиком частотой 3,5 МГц по методике Г.И. Кунцевич и соавт. [4] и включало ультразвуковое исследование в реальном масштабе времени в В-режиме, импульсную допплерографию и цветовое допплеровское картирование сосудов брюшной полости.
При исследовании оценивали ультразвуковые свойства печени и селезенки (контуры, структура, размеры). При импульсной допплерографии и цветовом допплеровском картировании сосудов брюшной полости изучались воротная и селезеночная вены, общая печеночная и селезеночная артерии. В каждом сосуде измеряли диаметр (D), определяли максимальную систолическую скорость кровотока (Vmах), конечно-диастолическую скорость кровотока (Vmin), максимальную линейную скорость кровотока, усредненную по времени (ТАМХ); рассчитывали объемную скорость кровотока (Q).
Для воротной вены рассчитывали конгестивный индекс (СI) по формуле:
Для интегральной оценки соотношения кровотока в воротной и селезеночной венах нами предложен воротно-селезеночный венозный индекс (ВСВИ), который рассчитывали по формуле:
Для оценки кровотока в артериальных сосудаx рассчитывали пульсационный индекс (РI) и индекс периферического сопротивления (RI). Для интегральной оценки соотношения артериального и венозного кровотока в печени рассчитывали индекс артериальной перфузии (ИАП) по формуле:
Для оценки соотношения параметров кровотока в воротной вене и общей печеночной артерии нами предложен печеночный сосудистый индекс (ПСИ), который рассчитывали по формуле:
Результаты и их обсуждение
Данные о параметрах кровотока в венах и артериях портальной системы приведены в табл. 1 и 2.
Как следует из табл. 1, у первой группы больных зарегистрировано достоверное увеличение диаметpa воротной и селезеночной вен, СI, а также снижение параметров линейной скорости кровотока в воротной вене (Vmах, Vmin, ТАМХ) по сравнению со второй (больные ХГ) и контролем. Показатели объемной скорости кровотока (Q) в воротной вене во всех трех группах достоверно не различались. В то же время Q в селезеночной вене у больных первой и второй групп была достоверно выше, чем в контроле. ВСВИ был достоверно ниже в первой группе больных по сравнению с больными второй группы и контролем.
У больных второй группы, по сравнению с контролем, выявлено снижение Vmах в воротной вене, a также увеличение СI, диаметра селезеночной вены и Q в селезеночной вене. Таким образом, уже у больных ХГ развивались изменения портальной гемодинамики: некоторое снижение линейной скорости кровотока в воротной вене, незначительное увеличение диаметра селезеночной вены и объемной скорости кровотока в ней.
У больных ЦП происходила значительная перестройка гемодинамики в венах воротной системы, выражавшаяся в увеличении диаметра воротной и селезеночной вен, а также в снижении показателей линейной скорости кровотока в воротной вене. При этом объемная скорость кровотока в ней сохранялась в нормальных пределах. В то же время у этой категории больных происходило увеличение объемного кровотока в селезеночной вене, т. е. перераспределение кровотока в венах воротной системы в направлении селезенки.
Таблица 1. Параметры кровотока в венах воротной системы у больных ХДЗП
Доплер сосудов печени (лекция на Диагностере)
Кровоснабжение печени организовано через артерии, отводящие и приводящие вены. При доплерографии печеночную артерию, печеночные и воротные вены можно отличить по неповторимой форме спектра (подробнее смотри Доплер сосудов начинающим).
Доплер печеночной артерии
В печеночной артерии и воротной вене гепатопетальный кровоток (К печени). Печеночная артерия несет 20-30% объема крови, а воротная вена — 70-80%. После приема пищи кровоток в воротной вене нарастает, а артериальная фракция сокращается. При портальной гипертензии растет сопротивление в системе воротной вены, тогда печеночная артерия компенсаторно увеличивается.
Нажимайте на картинки, чтобы увеличить.
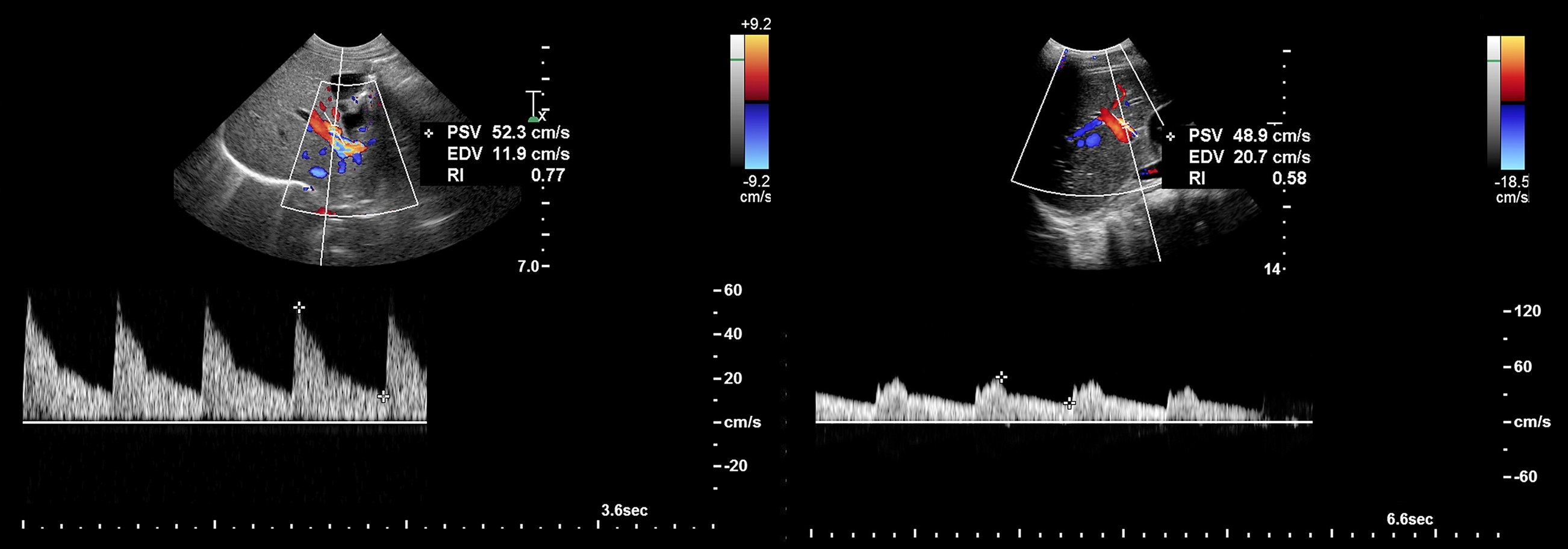
Рисунок. На УЗИ разные сегменты печеночной артерии у здоровых детей. В печеночной артерии кровоток К датчику — красный цвет при ЦДК и спектр выше базовой линии. Спектр с высоким диастолическим потоком и низким сопротивлением: общая печеночная артерия у новорожденного (1) — RI 0,77; левая печеночная артерия у мальчика 13-ти лет (2) — RI 0,58.
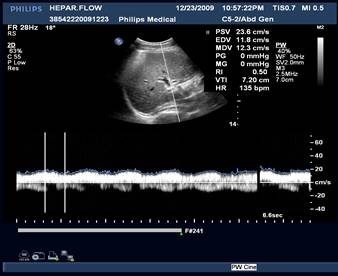
Рисунок. Печеночная артерия в норме имеет низкое сопротивление — RI 0,55-0,8 (2). RI>0,8 (1) вызывает настороженность. RI В воротных венах индекс пульсации PI=V2/V1, в отличие от артериального PI=(V1-V2)/Vmean. В норме PI>0,5.
Гепатопетальный кровоток что это такое
Неалкогольная жировая болезнь печени (НАЖБП) представляет собой заболевание, сопровождающееся последовательными патологическими изменениями в печени на фоне, прежде всего, инсулинорезистентности, и формированием фиброзных изменений в печеночной ткани, которые распространяются вглубь печеночных долек, переходят на перипортальные зоны, приводя к повышению давления внутри воротной вены, формированию портальной гипертензии и других нарушений портального и печеночного кровотока. Сочетание НАЖБП с гипертонической болезнью (ГБ), несомненно, оказывает взаимно потенцирующее действие как на течение НАЖБП и скорость развития фиброзных изменений в паренхиме печени, так и на прогрессирование артериальной гипертензии (АГ) и повреждения органов-мишеней [3].
Известно, что при ГБ развиваются тяжелые структурно-функциональные нарушения со стороны сосудистой системы. Ремоделирование сосудистой стенки при ГБ является компенсаторно-приспособительной реакцией в условиях длительного повышения артериального давления (АД) и заключается в гипертрофии ее мышечной стенки, накоплении эластических волокон с последующей дегенерацией и гиалинозом. Все это приводит к повышению ригидности и относительному уменьшению просвета сосуда [1].
Наряду с поражениями крупных сосудов, при ГБ развиваются микроциркуляторные нарушения, которые рассматриваются в качестве ключевого механизма повышения общего периферического сосудистого сопротивления. При этом наряду с гипертрофией сосудистой стенки происходят обеднение капиллярного русла, локальный спазм артериол, застой в венулах и снижение интенсивности кровотока в обменных сосудах [8].
Поражение органов-мишеней при ГБ (миокарда, почек, головного мозга и др.) хорошо изучено и описано в литературе [6]. В то же время большой научный и практический интерес представляет изучение особенностей портального кровотока и внутрипеченочной гемодинамики при ГБ, поскольку нарушения микроциркуляции в печеночной паренхиме в условиях ГБ, безусловно, будут отрицательно влиять на функцию печени, а наличие стеатоза (стеатогепатита) как проявления НАЖБП, в свою очередь, будет отрицательным образом сказываться на течении ГБ.
В нескольких исследованиях, опубликованных в последние годы, был зафиксирован высокий риск развития ишемической болезни сердца (ИБС) у больных НАЖБП. В частности, в проведенных испытаниях были проанализированы клинические исходы у больных НАЖБП, перенесших коронарную ангиографию; конечная точка объединяла кардиоваскулярную смертность, нефатальный инфаркт миокарда и потребность в проведении коронарного вмешательства. В исследовании приняли участие 612 пациентов, из них у 356 (58,2 %) больных выявили ультразвуковые признаки НАЖБП, у 318 (52,0 %) участников отметили повышение уровня АЛТ, у 465 (76,0 %) пациентов диагностировали ИБС. Оказалось, что ИБС наблюдалась у 84,6 % больных НАЖБП и у 64,1 % пациентов, не имевших сопутствующей патологии печени (р 0,05.
При качественном анализе спектрограмм кровотока по воротной вене во всех изучаемых группах пациентов был зарегистрирован нормальный, направленный в сторону печени, гепатопетальный, непрерывный, ламинарный поток крови с незначительными колебаниями, связанными с актом дыхания (см. рис. 1).
Рисунок 1. Допплерографический спектр кровотока в воротной вене (гепатопетальный) в норме и у обследованного контингента
В первой группе пациентов (НАЖБП) все абсолютные и индексированные показатели кровотока в воротной и печеночных венах и артериях, отражающие внутрипеченочную гемодинамику, не отличались от нормативных. Во второй группе (НАЖБП+ГБ) зарегистрировано достоверное повышение числового значения PI опа (нормативные значения 1,5±0,09), который составил в среднем по второй группе 1,55±0,02 против 1,54±0,07 в первой группе наблюдения (р 0,05) и достоверно снижавшегося до 12,15±3,3 см/с в третьей группе (р 0,05) за счет незначительного снижения значения V vol вв с 967,3±45,7 до 960,0±23,0 мл/мин в группах 1 и 2 соответственно (р>0,05) на фоне незначительного повышения кровотока в селезеночной вене (V vol св) с 375,1±38,9 до 393,0±44,8 мл/мин в группах 1 и 2 соответственно (р>0,05). СПИ у больных 3 группы (НАЖБП+ГБ+ИБС) достоверно отличался от показателей пациентов группы 1 и 2 (р 0,05). У больных 3 группы d вв был достоверно больше, чем у пациентов с изолированной НАЖБП, и составил 1,12±0,3 см (р
Что покажет расшифровка УЗИ брюшной полости
Для начала давайте посмотрим, что показывает данное ультразвуковое исследование.
За передней стенкой живота находится большое пространство – брюшная полость. В ней расположено довольно много органов, которые и покажет ультразвук полости живота. Это:
Брюшная полость выстлана двумя слоями тонкой оболочки – брюшины. Именно ее воспаление называется перитонитом и является опасным для жизни состоянием. Органы по-разному покрыты брюшиной: некоторые в нее обернуты, некоторые даже не касаются, но находятся внутри очерченных ею границ. Условно полость разделяется на собственно брюшную полость и забрюшинное пространство. К последнему относится нижняя часть списка органов, начиная с почек.
Все эти органы – и брюшной полости, и пространства за брюшиной — смотрят на УЗ-исследовании брюшной полости. Это исследование способно выявить наличие повреждения структуры, воспаление, патологические образования, увеличение или уменьшение органа, нарушение его кровоснабжения. То, как справляется больной или здоровый орган со своими функциональными обязанностями, ультразвук не видит.
Что дает УЗИ. Исследование помогает найти причину болезни в таких случаях:
Патология, определяемая на УЗИ
Что диагностирует УЗИ полости живота. С помощью данного исследования могут быть выявлены такие болезни:
1. Со стороны желчного пузыря:
2. Со стороны печени:
3. Со стороны почек и мочевыделительной системы:
4. Со стороны селезенки ультразвук брюшной полости выявляет:
5. Со стороны поджелудочной железы:
6. УЗИ выявляет свободную жидкость в брюшной полости
7. Со стороны брюшной части аорты или ее ветвей может быть видна аневризма и ее расслоение, сужение сосудов
8. Со стороны забрюшинных лимфоузлов видно их увеличение, однородность структуры
Как понять результаты исследования
Для этого рассмотрим бланк (протокол) УЗИ. В нем указаны моменты, которые касаются каждого органа по-отдельности.
Расшифровка УЗИ брюшной полости в отношении этого органа включает:
| Параметр | Что написано в бланке | Нормальные показатели УЗИ у взрослых |
|---|---|---|
| Размеры всего органа | Норма, уменьшена, увеличена (подчеркнуть нужное) | Норма |
| правая | Указаны цифры в см по каждому пункту | До 12,5 |
| левая | До 7 | |
| хвостатая | 30-35 | |
| Косо-вертикальный размер (КВР) правой доли | Цифры в мм | До 150 мм |
| Контуры | Подчеркнуто, ровные они или нет | Ровные |
| Капсула | Подчеркнуто, дифференцируется она или нет, утолщена или нет | Дифференцируется, не утолщена |
| Толщина левой доли | Цифра в мм | 50-60 |
| Толщина правой доли | 120-125 | |
| Эхоструктура паренхимы | Подчеркнуто, норма, повышена или снижена | Норма |
| Очаговые образования | Есть или нет | Не должно быть |
| Воротная вена | Указан размер в мм | До 14 мм |
| Сосудистый рисунок | Обеднен, обычный или усилен | Обычный |
| Нижняя полая вена | Размер в мм | Анэхогенная, диаметром 20 мм |
| Вены печеночные первого порядка | Размер в мм | До 1 мм |
На видео специалист рассказывает об ошибках, возникающих при ультразвуковом исследовании органов брюшной полости.
Норма УЗИ по результатам осмотра этого органа:
Признаки патологии желчного пузыря
Расшифровка УЗИ желчных протоков
В норме на УЗИ желчные протоки имеют такие характеристики:
Нормы поджелудочной железы на УЗИ
Снижение эхоплотности железы говорит об остром панкреатите, увеличение ее – о хроническом панкреатите или раке. Также о хроническом воспалении говорит и расширение вирсунгова протока. В «пользу» рака же свидетельствует сегментарное увеличение размеров и неровность контура железы, вдавление на поверхности печени, а также смещение или сдавливание нижней полой вены или аорты.
Расшифровка УЗИ селезенки
УЗИ полых органов (желудка, тонкой, толстой и прямой кишок)
Здесь указывается только то, есть ли симптом «пораженного органа» (его не должно быть) и имеется ли депонирование жидкости в просвете кишки (этого также не должно быть).
Если проводилось УЗИ еще и почек, то описание этого органа также входит в заключение исследования. Результаты обследования почек по УЗИ в норме:
Лимфатические структуры при ультразвуковой визуализации
УЗИ забрюшинных лимфоузлов в норме предполагает такое заключение «Лимфоузлы не визуализируются». То есть, если они имеют нормальные размеры, их ультразвук «не видит». Увеличение этих органов иммунитета говорит или об инфекционном заболевании, имеющемся в брюшной полости, или о злокачественном образовании. В последнем случае они могут увеличиваться из-за того, что в них «обитают» клетки рака кроветворной системы, а также при метастазах любой расположенной рядом опухоли органа.
В заключении УЗИ сонолог (врач ультразвуковой диагностики) указывает наличие патологии: он описывает, на что похожи эхо-признаки. Если в направлении врач указывает, что нужно провести осмотр на предмет какого-то заболевания, но его УЗИ не визуализировало (например, калькулезный холецистит), тогда может быть фраза «Эхо-признаков заболевания не выявлено». Окончательный диагноз ставит только врач, направляющий на обследование.
Кому нужно пройти допплерометрию брюшнополостных сосудов
Это обследование, которое еще называется УЗДГ (то есть ультразвуковая допплерография) брюшнополостных сосудов, выполняется зачастую вместе с УЗИ. Пациентом по ощущениям не дифференцируется и не является более вредным, чем УЗИ. Оно позволяет оценить анатомию и характеристики кровообращения в таких сосудах, как:
УЗИ сосудов брюшной полости позволяет вовремя выявить ранние нарушения в сосудах, выявить и оценить степень повышения давления в воротной вене (при циррозе, «застойной» печени), оценить результат имплантации кава-фильтра.
УЗИ брюшного отдела аорты и ее ветвей помогает в диагностике:
В исследование сосудов во время УЗИ на современной аппаратуре почти всегда входит и дуплексное ангиосканирование. Это – «золотой стандарт» в оценке кровообращения в венозных сосудах. Он позволяет выявить патологические забросы крови, препятствия кровотоку, оценить их локализацию, протяженность и степень выраженности.
При данном виде исследования сонолог получает цветное двухмерное изображение брюшнополостных сосудов, где красный цвет означает движение крови к датчику, а синий – наоборот, от датчика. По интенсивности красного и синего цветов врач делает выводы о скорости кровотока на любом участке сосудистой системы.
Дополнительные данные об исследовании
Отзывы об УЗИ, в основном, положительные: исследование безболезненно, безвредно, очень информативно. Отрицательный момент заключается в том, что перед процедурой нужно тщательно подготовиться, чтобы газы в кишечнике («явления метеоризма») не помешали правильной диагностике.
Сколько стоит провести данное исследование. Полное обследование всех органов (включая почки и мочевыводящую систему) с дуплексным ангиосканированием оценивается клиниками в среднем в 2000- 2500 рублей. Осмотр отдельных органов с оценкой в них кровотока обходится около 800-1000 рублей.
Таким образом, расшифровка УЗИ брюшной полости должна проводиться специалистом с учетом не только цифр «нормы», но и на основании клинических проявлений. Указанные выше значения помогут вам немного разобраться с выявленной у вас патологией, но окончательную оценку должен давать специалист терапевт или гастроэнтеролог.
А еще здесь искали: узи брюшной полости расшифровка норма, не видят жидкость на узи, бланк для УЗИ органов ЖКТ, селезеночная вена норма у взрослых
Гепатопетальный кровоток что это такое
ГБОУ ВПО «Ростовский государственный медицинский университет Минздрава России», Ростов-на-Дону
ГБОУ ВПО «Ростовский государственный медицинский университет Минздрава России», Ростов-на-Дону
Отдаленное наблюдение пациентки после спленоренального венозного шунтирования по поводу внутрипеченочной портальной гипертензии
Журнал: Флебология. 2014;8(4): 59-65
Сапронова Н. Г., Кательницкий И. И. Отдаленное наблюдение пациентки после спленоренального венозного шунтирования по поводу внутрипеченочной портальной гипертензии. Флебология. 2014;8(4):59-65.
Sapronova N G, Katel’nitsky I I. The long-term follow up of the patient after splenorenal venous bypass surgery for the treatment of intrahepatic portal hypertension. Flebologiya. 2014;8(4):59-65.
ГБОУ ВПО «Ростовский государственный медицинский университет Минздрава России», Ростов-на-Дону
Цирроз печени в 70% случаев служит причиной внутрипеченочной портальной гипертензии. Наиболее грозным и самым частым осложнением гипертензии в портальной системе является кровотечение из варикозно-расширенных вен пищевода и желудка. Многие из паллиативных операций продлевают жизнь пациентам с портальной гипертензией, не препятствуют выполнению пересадки печени и помогают им дождаться трансплантации. В статье представлено описание наблюдения пациентки с вирусассоциированным циррозом печени после спленоренального венозного шунтирования в течение 7 лет после операции с хорошим результатом.
ГБОУ ВПО «Ростовский государственный медицинский университет Минздрава России», Ростов-на-Дону
ГБОУ ВПО «Ростовский государственный медицинский университет Минздрава России», Ростов-на-Дону
Несмотря на успехи в диагностике и лечении заболеваний, осложненных портальной гипертензией, большое число экспериментальных и клинических работ, многие тактические вопросы лечения и профилактики вызывают дискуссию и до сих пор не решены. В основе этиологии и патогенеза синдрома портальной гипертензии лежит многокомпонентное нарушение гемоциркуляции как на органном, так и на системном уровне [1].
Цирроз печени в 70% наблюдений служит причиной внутрипеченочной портальной гипертензии. В России цирроз печени ежегодно является причиной смерти около 50 000 человек, коэффициент смертности при этом превышает среднемировой в 3 раза. Всемирная организация здравоохранения (ВОЗ) связывает эту неблагоприятную тенденцию с увеличением заболеваемости вирусными гепатитами [2].
Наиболее грозным и самым частым осложнением гипертензии в портальной системе является кровотечение из варикозно-расширенных вен пищевода и желудка [3]. Именно пищеводно-желудочные кровотечения являются основной причиной смерти больных циррозом печени. Смертность от первого кровотечения из варикозно-расширенных вен пищевода составляет 50—60%, а при декомпенсированной функции печени достигает 76—80%.
Многие из паллиативных операций продлевают жизнь пациентам с портальной гипертензией, не препятствуют выполнению пересадки печени и помогают им дождаться трансплантации [5].
В настоящее время для лечения и профилактики пищеводно-желудочных кровотечений при портальной гипертензии применяется несколько оперативных вмешательств: портокавальные анастомозы, эндоваскулярные вмешательства (трансъюгулярное внутрипеченочное портосистемное шунтирование, эмболизация варикозно-расширенных вен пищевода, эмболизация селезеночной артерии), спленэктомия, эндоскопические вмешательства [5]. Отдаленные результаты показывают, что портокавальное шунтирование является наиболее адекватным и патогенетически обоснованным методом хирургического лечения повышенного давления в воротной вене.
Клиника хирургических болезней Ростовско-го государственного медицинского университета располагает опытом лечения 341 пациента с портальной гипертензией за последние 15 лет, из них 207 выполнены операции декомпрессии портальной системы. У всех пациентов портальная гипертензия развилась на фоне цирроза печени разной этиологии. 79 пациентам декомпрессия была достигнута за счет выполнения спленоренального венозного шунтирования после спленэктомии. Оценка отдаленных результатов оперативного вмешательства у больных с внутрипеченочной портальной гипертензией является наиболее надежным и объективным методом определения эффективности лечения, качества его выполнения. В таблице представлены критерии оценки эффективности вмешательств в отдаленном периоде. В настоящей работе мы представляем вниманию читателей случай длительного успешного функционирования спленоренального венозного анастомоза.

Больная Л., 22 года, поступила в клинику хирургических болезней 02.02.06 с диагнозом: вирусассоциированный по вирусу гепатита С цирроз печени, портальная гипертензия, гепатоспленомегалия, поверхностный гастродуоденит, дуоденогастральный рефлюкс, варикозное расширение вен пищевода и кардиального отдела желудка III степени, гиперспленизм, хроническая печеночно-клеточная недостаточность класс, А (4 балла по Child—Turcotte—Pugh). Из анамнеза известно, что при обследовании в 2004 г. были выявлены положительные маркеры вирусного гепатита С, по данным ультразвукового исследования установили увеличение печени и селезенки. Наблюдалась в гепатологическом центре, где в январе 2006 г. при эзофагогастродуоденоскопии (ЭФГДС) были выявлены расширенные вены пищевода и кардиального отдела желудка III степени. Направлена на оперативное лечение в Ростовский государственный университет. При обследовании в хирургической клинике установлено следующее:
Общий анализ крови (06.02.06): Hb 108 г/л; эр. 3,64·10 12 /л, показатель гематокрита 28,6%, тр. 100·10 9 /л, л.3,0·10 9 /л; СОЭ 6 мм/ч; лейкоцитарная формула: мц. 0%, ю. 0, п. 4%, с. 48, э. 2%, б. 2%, лимф. 36%, мон. 8%.
Общий анализ мочи (06.02.06): количество 160 мл; цвет светло-желтый; прозрачная; неполная; удельный вес 1016; реакция кислая; лейкоциты 4—6 в поле зрения; эпителий мочевыводящих путей плоский 5—7 в поле зрения; слизь — небольшое количество.
Биохимический анализ крови (06.02.06): общий белок 72 г/л; альбумины 65 г/л; α-глобулины 13%; β-глобулины 7%; γ-глобулины 15%; коэффициент альбумины/глобулины 1,8; глюкоза 3,92 ммоль/л; общий билирубин 19 мкмоль/л; прямой билирубин 4,6 ммоль/л; аспартатаминотрансфераза 32 Е/л; аланинаминотрансфераза 41 Е/л; креатинин 65 мкмоль/л.
Коагулограмма (06.02.06): активированное время рекальцификации 60 с; антипротромбиновое время 39 с; протромбиновый индекс 89%; фибриноген 2,44 г/л; тромбиновое время 14,5 с; толерантность к гепарину 9 мин 30 с; XII-А-калликреинзависимый фибринолиз 4 мин; МНО 1,24.
Ультразвуковое исследование от 07.02.06: селезеночная вена в проекции поджелудочной железы 14 мм в диаметре, кровоток монофазный 18 см/с, в воротах селезенки 15 мм в диаметре, кровоток монофазный 20 см/с. Воротная вена в воротах печени 19 мм в диаметре, кровоток гепатопетальный 14 см/с, печеночные вены сужены, кровоток монофазный, внутрипеченочные протоки не расширены, холедох 4 мм. Селезенка 170×100 мм, эхоструктура печени умеренно диффузно неоднородная, свободная жидкость в брюшной полости не визуализируется. Заключение: ультразвуковые признаки диффузных изменений паренхимы печени, спленомегалия, косвенные признаки портальной гипертензии.
ЭФГДС от 07.02.06. Заключение: поверхностный гастродуоденит, дуоденогастральный рефлюкс, варикозное расширение вен пищевода и кардиального отдела желудка III степени.
13.02.06 пациентке была выполнена операция: спленэктомия, спленоренальное венозное шунтирование (СРВШ), биопсия печени, дренирование брюшной полости.
Результат морфогистологического исследования от 14.02.06.
Материал: селезенка. Макроселезенка 160×110×50 мм, на разрезе пульпа серо-красная, дает скудный соскоб. Заключение: в ткани селезенки эктазия просвета, склероз стенок селезеночных вен, эктазия и склероз стенок синусоид. Атрофия лимфоидной ткани, полнокровие, кровоизлияния, гемосидероз красной пульпы.
Материал: участок селезеночной вены. В стенке эктазированной вены очаговый склероз интимы, гипертрофия гладкомышечных клеток среднего слоя.
Послеоперационный период протекал без осложнений, дренажи удалены на 2-е сутки после операции. В анализах после операции прослеживались следующие изменения: снижение содержания гемоглобина до 95 г/л, увеличение числа тромбоцитов от 137·10 9 /л на 3-и сутки после операции до 525·10 9 /л к 13-м суткам после операции (рис. 1).

На 12-е сутки после операции больной было выполнено ультразвуковое исследование, показавшее, что спленоренальный анастомоз диаметром 9 мм функционирует с максимальной линейной скоростью кровотока (ЛСК) 29 см/с. Диаметр воротной вены 12 мм. При ЭФГДС определялись варикозно-расширенные вены пищевода II степени.

На протяжении всего времени после СРВШ пациентка находилась под нашим динамическим наблюдением. Через 7 лет после операции при осмотре пациентки не выявлено признаков асцита, при ЭФГДС выявлено варикозное расширение вен пищевода I степени. В течение всего периода наблюдения у пациентки не было признаков варикозного пищеводно-желудочного кровотечения. При проведении психомоторных тестов признаки печеночной недостаточности не выявлены. Пациентка продолжает работать переводчиком иностранного языка в крупной коммерческой организации, не изменив профессии после операции.
Приводим результаты обследования больной Л., 29 лет, через 7 лет после операции СРВШ (рис. 3).

Общий анализ крови (20.10.13): Hb 128 г/л, эр. 3,9·10 12 /л, показатель гематокрита 28,6%, тр. 213·10 9 /л, л. 4,2·10 9 /л; СОЭ 4 мм/ч; лейкоцитарная формула: мц. 0%, ю. 0%, п. 4%, с. 49%, э. 1%, б. 1%. лимф. 38%, мон. 7%.
Общий анализ мочи (20.10.13): количество 80 мл; цвет светло-желтый; прозрачная, неполная; удельный вес 1014; реакция кислая; лейкоциты 2—3 в поле зрения; эпителий мочевыводящих путей плоский 4—5 в поле зрения; слизь — небольшое количество.
Коагулограмма (20.10.13): протромбиновое время 0,94 МНО; активированное частичное тромбопластиновое время 30,3 с; фибриноген 2,8 г/л; тромбиновое время 18,4 с; антитромбин III 95%; фибринолиз 240 мин; плазминоген 83%; растворимые фибрин-мономерные комплексы 3,0 мг/100 м; D-димер 354 нг/мл. Заключение: показатели гемостаза в референтных пределах.
СФГДС от 20.10.13: пищевод: слизистая розовая, блестящая, на уровне средней и нижней трети на всех стенках имеются варикозно-расширенные вены, выступающие в просвет до 0,2—0,3 см, перистальтика сохранена. Слизистая нижней трети пищевода осмотрена в режиме NBI — переходная зона не расширена, Z-линия четкая, слизистая без признаков метаплазии. Желудок: форма правильная, слизистая умеренно диффузно гиперемированная, блестящая, умеренно атрофична, в антральном отделе единичные «полные» в неактивной фазе по 0,2 см точечные геморрагические эрозии. Двенадцатиперстная кишка: луковица правильной формы, слизистая умеренно гиперемированная, блестящая, большой дуоденальный сосочек до 0,3 см, не изменен. Заключение: поверхностный гастродуоденит с эрозиями в антральном отделе. Дуоденогастральный рефлюкс, варикозное расширение вен пищевода I степени (рис. 4).

Непрямая эластометрия от 15.10.13: показатель непрямой эластометрии печени на аппарате Фиброскан равен 8,2 кПа, что с точностью до 93,2% соответствует стадии фиброза F2 по шкале Metavir.
Ультразвуковое сканирование воротной вены от 20.10.13: нижняя полая вена 17 мм, ЛСК 38 см/с, кровоток фазный; печеночные вены 6—7 мм, ЛСК 30 см/с, кровоток фазный; диаметр воротной вены 11 мм, ЛСК 12 см/с, кровоток гепатопетальный. Правая ветвь воротной вены 5 мм, ЛСК 9 см/с, левая ветвь воротной вены 5 мм, ЛСК 9 см/с. Селезеночная вена не визуализируется, верхняя брыжеечная вена 9 мм, ЛСК 13 см/с, кровоток гепатопетальный. Заключение: состояние после спленэктомии, визуализируемые вены кавальной и портальной систем проходимы, диаметр вен в допустимых пределах. Кровоток в венах портальной системы гепатопетальный. Расширение портосистемных анастомозов в области ворот печени.
Компьютерная томография органов брюшной полости от 15.09.13: по сравнению с исследованием от 2007 г. отмечается некоторое уменьшение размеров печени в фронтальном направлении с сохранением вертикального размера. Отмечается повышение степени неоднородности печеночной паренхимы. В VIII сегменте печени визуализируется образование округлой формы 24×20 мм равномерное в артериальную фазу и гиподенсивное в венозную фазу. В других отделах печени также определяются аналогичные образования меньшего размера (вероятнее всего, очаги регенерации). Свободная жидкость не обнаружена, вокруг головки поджелудочной железы сохраняются прежнего калибра извитые венозные сосуды, анастомозирующие с ветвями брыжеечной вены, расширена яичниковая вена. Заключение: картина нарастания структурных изменений паренхимы печени, признаки портальной гипертензии (рис. 5).

После клинического всестороннего обследования пациентке был поставлен диагноз: вирусассоциированный по вирусу гепатита С цирроз печени F2 по шкале Metavir в стадии интеграции, портальная гипертензия, поверхностный гастродуоденит с эрозиями в антральном отделе, дуоденогастральный рефлюкс, варикозное расширение вен пищевода I степени, хроническая печеночно-клеточная недостаточность класс, А (4 балла по Child—Turcotte—Pugh).
По результатам обследования пациентки выраженных изменений в анализах крови и мочи не выявлено. Таким образом, данный клинический пример указывает на возможности СРВШ, которое дает хорошие клинические результаты (отсутствие рецидивов кровотечения, регрессирование варикозного расширения вен пищевода, отсутствие асцита, отсутствие прогрессирования печеночной недостаточности).
Необходимые пояснения. У пациентки получено письменное разрешение на публикацию данных.
Конфликт интересов: авторы сообщают об отсутствии конфликта интересов.