Генетическая модификация это что
ГМО-люди – будущее биотехнологий уже здесь

Интересно, чем закончатся наши исследования
Кажется, прошлая тема про ГМО-лосося весьма неплохо зашла Хабрачитателям. Пока мы готовим материал по модификации растений, я предлагаю посмотреть не менее интересную тему — генная модификация Homo Sapiens. Это очень спорная и холиварная тема, игнорировать которую бесполезно.
Сразу дам несколько тезисов, которые могут показаться спорными, но которые так или иначе надо решать в научном сообществе:
Что такое генотерапия
Давайте для начала определимся с терминологией. Генотерапия — это вмешательство в геном человека с целью лечения тех или иных заболеваний. Причем, вмешательство идет только в соматические клетки. Это те клетки, которые не участвуют в размножении. Нам явно не надо какие-то мутации и багфиксы закреплять в новых поколениях. Пока, по крайней мере.
Реальные эксперименты на животных начались примерно в 1980-х годах, но тогда это были только робкие шаги. Всякого рода красоты вроде ДНК-принтеров, экспрессирующихся векторов для эукариотов у нас не было.
Куда мы реально можем вмешаться?
Плазмиды
Для начала можно не трогать ядро клетки, которое содержит основную генетическую информацию. Можно воспользоваться плазмидами. 
1) Хромосомная ДНК бактерии 2) Плазмиды
Плазмиды — это почти исключительно бактериальная штука. Иногда встречаются у примитивных грибов и некоторых растений. По сути, это ДНК, но свернутая в кольцо и плавающая отдельно в цитоплазме. То есть такой отдельный механизм для хранения генетического материала. Для бактерий они очень важны для передачи положительных мутаций, например, чтобы «рассказать соседям» о вариантах защиты от антибиотика. Фишка плазмид при использовании у людей в том, что они разваливаются сами по себе через какое-то время после введения в клетку. А еще они не затрагивают основной генетический аппарат клетки. То есть основную прошивку не затронет.
Патчим kernel
Далее, у нас есть возможность непосредственно отредактировать фрагмент кода в ядре. Это более инвазивная процедура и она уже сопряжена с рисками неточной вставки или вырезания кусочка ДНК. Но это практически единственный вариант радикально починить какой-то тяжелый генетический дефект, так как соматические клетки будут делиться и передавать пропатченную версию ДНК своим потомкам.
Митохондрии
Митохондрии — это что-то вроде атомных реакторов в клетке. Потребляют жирные кислоты и глюкозу, а на выходе штампуют макроэрги — вещества с высокой энергией связи. Например, АТФ. Это универсальное «топливо» для всех активных реакций, например для работы осмотических мембранных насосов против градиента концентрации.
У них есть особенность — свой собственный генетический аппарат. Собственно, они на полуавтономных симбионтов похожи именно поэтому. Их генетический аппарат имеет смысл править при врожденных мутациях в митохондриальной ДНК. Обычно это тоже очень тяжелые врожденные синдромы.
Вирусный вектор — это как шприц
Первый ключевой момент — разработка инструментария доставки — вирусных векторов. Первый такой вирус для млекопитающих был разработан в 1984 году. В качестве молекулярного шприца использовали мышиный ретровирус. Он сам по себе являлся весьма неприятным инструментом, так как с высокой вероятностью провоцировал онкологические заболевания. Собственно, его второе название murine leukemia virus (MLVs). В дальнейшем разработки перешли на более безопасные варианты.
Что вообще такое вирусный вектор? Это такой специально модифицированный вирус, который срабатывает только один раз. Как шприц. Для этого он должен отвечать нескольким критериям:
Безопасность
Вирусный вектор не должен иметь возможность самопроизвольно размножаться. Для этого у них есть встроенный kill-switch. Их геном изначально так поврежден, что автономно размножаться они не могут. В лабораторной среде они размножаются на культуре клеток только в присутствии незаменимых компонентов и дополнительных вспомогательных вирусов, которые производят часть нужных для сборки белков. То есть в культуральном флаконе лаборатории размножается, а в организме срабатывает один раз, выходит из клетки в полусобранном виде и умирает.
Низкая цитотоксичность
Многие вирусы очень жестоко обращаются с клетками носителя. После фазы инкубации клетка дохнет от истощения и из ее бренных останков во все стороны разлетаются новые вирионы. При этом есть и вирусы, которые особо не влияют на нормальную физиологию клеток, на которых паразитируют. Например, аденовирусы.
Стабильность
Вирусы должны быть генетически стабильны. Например, грипп не подойдет. Он вообще не имеет внятных механизмов «контроля четности» и ему все равно, что хеш после копирования не сошелся. Это его эволюционная стратегия. Те же коронавирусы, напротив имеют механизмы контроля и репарации, что дает большую стабильность генетического материала. Хотя их не используют как вектор по другим причинам. Таким образом, задача состоит в том, чтобы вирус в процессе своего размножения в биореакторах сохранил тот самый payload — полезную нагрузку без изменений.
Специфичность типа клеток
Вирус должен доставить свою нагрузку не абы куда, а точно в конкретный тип клеток. Это значит, что если нам надо вылечить заболевание, связанное с дефектными эритроцитами, то вирус должен очень точно поражать именно мультипотентные стволовые клетки-предшественники клеток крови. И при этом не зацепить, например, мышечную ткань.
Что уже реально делают в плане генотерапии
Первая генетическая коррекция человека была проведена в 1990 году.Четырёхлетняя Ашанти ДеСильва получила лечение от тяжелого генетического дефекта сложного комбинированного иммунодефицита, связанного с недостатком фермента ADA. Надо отметить, что редактировали не геном стволовых клеток, которые производят Т-лимфоциты, а уже взрослые Т-клетки из ее же собственной донорской крови. То есть она нуждалась в повторении этих процедур в дальнейшем. Далее была серия успешных экспериментальных протоколов для лечения SCID (Severe combined immunodeficiency) по схожей методике.
В 1999 году произошел инцидент, который ощутимо затормозил исследования в этой области. Джесси Гелсинджер, страдал от генетического заболевания печени, из-за которого она была неспособна обезвреживать аммиак. Через 4 суток после введения аденовирусного вектора со здоровой копией гена он умер в результате гипериммунного ответа и полиорганной недостаточности. В дальнейшем FDA пришли к выводу о многочисленных нарушениях в протоколе исследования.
В 2006 появились первые сообщения об удачных протоколах индивидуальной генотерапии для лечения онкологии. Т-киллеры программируются на конкретный вид опухоли и затем выпускаются в организм пациента.
В 2011 году признали терапию ВИЧ у пациента Геро Хюттера в 2008 году. Метод не особо применим для широкой аудитории, так как требует полного удаления своего костного мозга, а затем имплантация скорректированных клеток с двойной дельта-32 мутацией, которая отключает рецептор CCR5.
К 2013 году в мире было разрешено всего пять генных препаратов. Три от онкологии, глибера для лечения наследственного дефицита липопротеинлипазы и неоваскулген. Последний, кстати, разработали полностью у нас.
Неоваскулген
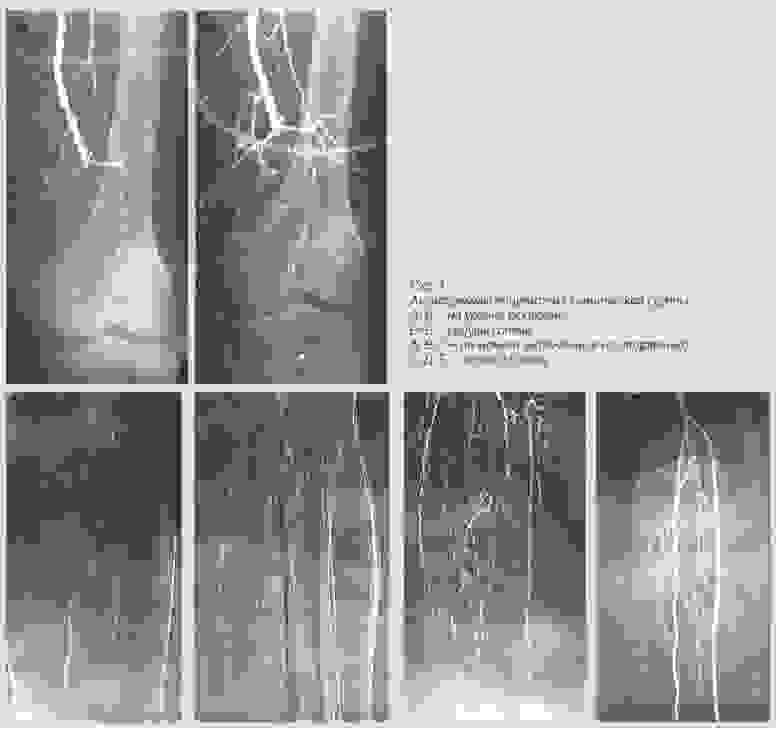
Результаты лечения Неоваскулгеном.
Этот препарат относится к плазмидным, то есть он не редактирует свой геном клетки, а только доставляет в нее плазмиды, которые работают ограниченное время.
Препарат представляет собой кольцевую ДНК (плазмиду), несущую человеческий ген VEGF 165, кодирующий синтез фактора роста эндотелия сосудов (VEGF — Vascular Endothelial Growth Factor). Стимулируя образование и рост коллатеральных сосудов, Неоваскулген призван оказать длительный лечебный эффект и улучшить качество жизни пациентов. Развитие микроциркуляторного русла в ишемизированной ткани нижней конечности способствует насыщению тканей кислородом, заживлению язв, увеличивает дистанцию безболевой ходьбы.
Механизм действия интересный. Клетки в месте инъекции начинают синтезировать VEGF — это фактор роста сосудов. В результате, в этом участке начинает нарастать новая разветвленная капиллярная сеть. Это критично для пациентов с хронической ишемией нижних конечностей из-за диабета и атеросклероза, например. До этого препарата ампутаций было больше. Сейчас его протестировали еще и для использования в стоматологии для приживления имплантов.
Генопрепарат смешивают с костным материалом и ушивают. В итоге сосуды быстро прорастают и формируется нужная ткань без отторжения. На кроликах уже точно моделировали при трансплантации фрагментов черепа. Люди на очереди, насколько мне известно.
Zolgensma
Спинальная мышечная атрофия — заболевание очень мрачное, по клинике отчасти похожее на боковой амиотрофический склероз, которым страдал Хокинг, но имеет другие причины. В результате развития заболевания прогрессирует паралич, который заканчивается смертью из-за невозможности дышать.
Zolgensma — это первый лекарственный препарат для генной терапии спинальной мышечной атрофии. Выпускается компанией AveXis (Novartis). Рабочая копия гена SMN вводится с помощью аденоассоциированного вируса (AAV) серотипа 9, AAV9, который способен преодолевать гематоэнцефалический барьер и проникать в клетки пациента. Одна проблема — стоит совершенно чудовищных денег. Одна инъекция стоит больше 2,1 миллиона долларов (около 152 миллионов рублей). Но результаты тоже потрясающие. У людей восстанавливается моторная функция и в дальнейшем заболевание не прогрессирует. По идее, такие дорогостоящие манипуляции должно оплачивать государство. Для отдельных людей стоимость лечения редких заболеваний просто неподъемная.
Что дальше?
Вот тут вопрос очень сложный. Мы действительно накапливаем дефектные гены в популяции. Раньше ребенок с пороком сердца бы просто умер — сейчас его спасут и он даст потомство с этим дефектом. Раньше много беременностей не сохранялось — сейчас беременных вытягивают с минимальным процентом выкидышей и завершают успешными родами. По сути, мы ломаем механизмы естественной выбраковки популяции. Это правильно и гуманно, но что-то надо делать с накапливающимися мутациями генофонда.
Либо мы придем к зеленым карточкам и разрешениям на размножение, либо научимся надежно и безопасно исправлять генетические аномалии. Было бы круто выкинуть близорукость, системную дисплазию соединительной ткани и кучу других врожденных дефектов. А еще наконец починить этот дурацкий сломанный ген, отвечающий за синтез витамина С из глюкозы, как у всех нормальных млекопитающих.
Вот только дальше нас ждет неизвестное будущее. Больше всего настораживает потенциальное расслоение общества, когда самые богатые слои населения будут модифицировать своих детей на отсутствие сахарного диабета, атеросклероза, а заодно еще и задавить немного миостатин, чтобы выглядели атлетичными без особых усилий. Круто же. Но пугает.
Что такое генная инженерия и зачем вмешиваться в природу организмов
Содержание:
Генная инженерия — это современное направление биотехнологии, объединяющее знания, приемы и методики из целого блока смежных наук — генетики, биологии, химии, вирусологии и так далее — чтобы получить новые наследственные свойства организмов.
Перестройка генотипов происходит путем внесения изменений в ДНК (макромолекулу, обеспечивающую хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов) и РНК (одну из трех основных макромолекул, содержащихся в клетках всех живых организмов).
Если внести в растение, микроорганизм, организм животного или даже человека новые гены, можно наделить его новой желательной характеристикой, которой до этого он никогда не обладал. С этой целью сегодня генная инженерия используется во многих сферах. Например, на ее основе сформировалась отдельная отрасль фармацевтической промышленности, представляющая собой одну из современных ветвей биотехнологии.
История развития
Истоки
Основы классической генетики были заложены в середине XIX века благодаря экспериментам чешского-австрийского биолога Грегора Менделя. Открытые им на примере растений принципы передачи наследственных признаков от родительских организмов к их потомкам в 1865 году, к сожалению, не получили должного внимания у современников, и только в 1900 году Хуго де Фриз и другие европейские ученые независимо друг от друга «переоткрыли» законы наследственности.
Параллельно с этим шел процесс формирования знаний о ДНК. Так, в 1869 году швейцарский биолог Фридрих Мишер открыл факт существования макромолекулы, а в 1910 году американский биолог Томас Хант Морган обнаружил на основе характера наследования мутаций у дрозофил, что гены расположены линейно на хромосомах и образуют группы сцепления. В 1953 году было сделано важнейшее открытие — американец Джон Уотсон и британец Фрэнсис Крик установили молекулярную структуру ДНК.
На подъеме
К концу 1960-х годов генетика активно развивалась, а ее важными объектами стали вирусы и плазмиды. Были разработаны методы выделения высокоочищенных препаратов неповрежденных молекул ДНК, плазмид и вирусов, а в 1970-х годах был открыт ряд ферментов, катализирующих реакции превращения ДНК.
Генная инженерия как отдельное направление исследовательской работы зародилась в США в 1972 году, когда в Стэнфордском университете ученые Пол Берг, Стэнли Норман Коэн, Герберт Бойер и их научная группа внедрили новый ген в бактерию кишечной палочки (E. coli), то есть создали первую рекомбинантную ДНК.
Техника ПЦР была впервые разработана в 1980-х годах американским биохимиком Кэри Маллисом. Будущий лауреат Нобелевской премии по химии (1993 года), обнаружил в специфический фермент — ДНК-полимеразу, который участвует в репликации ДНК. Этот фермент буквально считывает отрезки цепи нуклеотидов молекулы и использует их в качестве шаблона для последующего копирования генетической информации.
Новая эра
В 1996 году методом пересадки ядра соматической клетки в цитоплазму яйцеклетки на свет появилось первое клонированное млекопитающее — овца Долли. Это событие стало революционным в истории развития генной инженерии, потому что впервые стало возможным серьезно говорить о создании клонов и выращивании живых организмов на основе молекул.
Технологии генной инженерии
Генная инженерия за короткий срок оказала огромное влияние на развитие различных молекулярно-генетических методов и позволила существенно продвинуться на пути познания генетического аппарата.
Так, появилась технология CRISPR — инструмент редактирования генома. В 2014 году MIT Technology Review назвал его «самым большим биотехнологическим открытием века». Он основан на защитной системе бактерий, которые производят специальные ферменты, позволяющие им защищаться от вирусов.
«Каждый раз, когда бактерия убивает вирус, она разрезает остатки его генома, будь то ДНК или РНК, и сохраняет их внутри последовательности CRISPR, как в архив. Как только вирус атакует снова, бактерия использует информацию из «архива» и быстро производит защитные белки Cas9, в которых заключены фрагменты генома вируса. Если вдруг эти фрагменты совпадают с генетическим материалом нынешнего атакующего вируса, Cas9 как ножницами разрезает захватчика, и бактерия снова в безопасности», — поясняет Алевтина Федина, медицинский директор Checkme.
Уникальное открытие состоялось в 2011 году, когда биологи Дженнифер Дудна и Эммануэль Шарпантье обнаружили, что белок Cas9 можно обмануть. Если дать ему искусственную РНК, синтезированную в лаборатории, то он, найдя в «архиве» соответствие, нападет на нее. Таким образом, с помощью этого белка можно резать геном в нужном месте — и не просто резать, а еще и заменять другими генами.
Теоретически, технология CRISPR может позволить редактировать любую генетическую мутацию и излечивать заболевание, которое она вызывает. Но практические разработки CRISPR в качестве терапии еще только в начальной стадии, и многое еще непонятно.
Есть и другие методы генной инженерии, например, ZFN и TALEN.
Где и как применяется генная инженерия
Медицина
Уже сейчас активно применяется инсулин человека (хумулин), полученный посредством рекомбинантных ДНК. Клонированные гены человеческого инсулина были введены в бактериальную клетку, где начался синтез гормона, который природные микробные штаммы никогда не синтезировали. С 1982 года компании США, Японии, Великобритании и других стран производят генно-инженерный инсулин.
Кроме того, несколько сотен новых диагностических препаратов уже введены в медицинскую практику. Среди лекарств, находящихся в стадии клинического изучения, препараты, потенциально лечащие артрозы, сердечно-сосудистые заболевания, онкологию и СПИД. Среди нескольких сотен генно-инженерных компаний 60% заняты именно разработкой и производством лекарственных и диагностических средств.
«В медицине среди достижений генной инженерии сегодня можно выделить терапию рака, а также другие фармакологические новинки — исследования стволовых клеток, новые антибиотики, прицельно бьющие по бактериям, лечение сахарного диабета. Правда, пока все это на стадии исследований, но результаты многообещающие», — говорит Алевтина Федина.
Сельское хозяйство
В сельском хозяйстве одна из важнейших задач генной инженерии — получение растений и животных, устойчивых к вирусам. В настоящее время уже есть виды, способные противостоять воздействию более десятка различных вирусных инфекций.
Еще одна задача связана с защитой растений от насекомых-вредителей. Путем генетической модификации растений можно уменьшить интенсивность обработки полей пестицидами. Например, трансгенные растения картофеля и томатов стали устойчивы к колорадскому жуку, растения хлопчатника — к разным насекомым, в том числе и к хлопковой совке.
Использование генной инженерии позволило сократить применение инсектицидов (препаратов для уничтожения насекомых) на 40–60%.
Благодаря генной инженерии зерновые культуры стали более устойчивы к климатическим условиям, кроме того появилась возможность увеличить количество витаминов и полезных веществ в продукте. Например, можно обогатить рис витамином «А» и выращивать его в тех регионах, где люди имеют массовую нехватку этого элемента.
С помощью генной инженерии пытаются решить и экологические проблемы. Так, уже созданы особые сорта растений с функцией очистки почвы. Они поглощают цинк, никель, кобальт и иные опасные вещества из загрязненных промышленными отходами почв.
Скотоводство
В Кемеровской области работа генетиков позволила получить устойчивое к вирусу лейкоза племенное поголовье высокопродуктивных животных. Для проведения эксперимента кузбасские ученые отобрали здоровых коров черно-пестрой породы массой до 500 кг. Животным трансплантировали модифицированные эмбрионы, устойчивые к вирусу лейкоза. В середине сентября 2020 года родилось 19 телят с измененными генами.
«В месячном возрасте была проведена оценка, которая показала, что телята отличаются от своих сверстников только устойчивостью к вирусу. Пять особей отобрали для дальнейшей селекционной работы. Это позволит закрепить наследственные признаки устойчивости к вирусу лейкоза у последующих поколений», — пояснила руководитель проекта, доктор биологических наук, профессор кафедры зоотехнии Кузбасской ГСХА Татьяна Зубова.
По словам Зубовой, лейкоз крупного рогатого скота — вирусная хронически неизлечимая болезнь, при которой возникают поражение кроветворной системы и новообразования. Данное заболевание наносит значительный ущерб генофонду пород и мясной промышленности в целом, потому что мясо зараженных животных запрещено употреблять в пищу. Единственным доступным методом борьбы с лейкозом ранее было только уничтожение зараженного скота.
Этот успех позволяет говорить о том, что в дальнейшем будет возможно редактировать гены крупного рогатого скота и от других болезней.
С прицелом на человека
В 2009 году группа ученых под руководством молодого исследователя Джея Нейтца из Вашингтонского университета сумели с помощью генной терапии вернуть обезьянам способность различать оттенки зеленого и красного, которой они были лишены от рождения.
В область сетчатки глаза двух подопытных обезьян был введен безвредный вирус, несущий недостающий ген фоточувствительного рецептора. Вскоре после процедуры обе обезьяны начали различать оттенки красного и зеленого на сером фоне. Два года наблюдения не выявили у них каких-либо нарушений, поэтому ученые не исключают, что данную методику уже вскоре можно будет применять у людей, страдающих дальтонизмом.
Ученые шагнули еще дальше и уже пробуют выращивать в теле животных органы для трансплантации людям. Для минимизации риска отторжения тканей животным вводят специальные гены. Этими опытами занимается научная лаборатория Рослинского института в Великобритании, которая представила миру овцу Долли.
В 2019 году британские ученые вывели кур, яйца которых содержат два вида человеческих белков, способных противодействовать артриту и некоторым видам онкологических заболеваний. В яйцах содержится человеческий белок под названием IFNalpha2a, обладающий мощными противовирусными и противораковыми свойствами, а также человеческий и свиной вариант белка под названием макрофаг-CSF, который планируют использовать для создания препарата, стимулирующего самостоятельное заживление поврежденных тканей.
Изменение ДНК человека
Первые клинические испытания методов генной терапии были предприняты 22 мая 1989 года с целью генетического маркирования опухоль-инфильтрующих лимфоцитов в случае прогрессирующей меланомы.
14 сентября 1990 года в Бетесде (США) четырехлетней девочке, страдающей наследственным иммунодефицитом, обусловленным мутацией в гене аденозиндезаминазы (АDA), были пересажены ее собственные лимфоциты.
Работающая копия гена ADA была введена в клетки крови с помощью модифицированного вируса, в результате чего клетки получили возможность самостоятельно производить необходимый белок. Через шесть месяцев количество белых клеток в организме девочки поднялось до нормального уровня.
После этого область генной терапии получила толчок к дальнейшему развитию. С 1990-х годов сотни лабораторий ведут исследования по использованию генной терапии для лечения различных заболеваний. Уже сегодня с помощью генной терапии можно лечить диабет, анемию и некоторые виды онкологии.
Генная терапия
Генная терапия — введение, удаление или изменение генетического материала, в частности ДНК или РНК, в клетке пациента для лечения определенного заболевания.
Существует три основных стратегии использования генной терапии:
Наиболее часто применяемый метод включает вставку «терапевтического» гена для замены «ненормального» или «вызывающего болезнь».
В 2015 году впервые была проведена процедура изменения ДНК человека с целью продления молодости клеток, когда американке Элизабет Пэрриш 44 лет ввели в организм препарат, влияющий на ДНК, а в 2018 году китайский ученый Хэ Цзянькуй заявил, что с его помощью у двух детей-близнецов якобы изменены гены для выработки у них иммунитета к вирусу ВИЧ, носителем которого являлся их отец.
Все это, с одной стороны, выглядит грандиозно и обнадеживает, но с другой, — вызывает опасения, ведь генетические манипуляции, теоретически, возможно использовать не только в благих и мирных целях.
После эксперимента с ДНК близнецов в Китае, ЮНЕСКО выступила с инициативой о запрете изменения генов у новорожденных до того момента, пока достоверно не будет доказана безопасность таких манипуляций.
Этическая сторона вопроса
В 1997 году ЮНЕСКО выпустила Всеобщую декларацию о геноме человека и его правах, рекомендовав мораторий на генетическое вмешательство в зародышевую линию человека, а в декабре 2015 года на международном саммите по геномному редактированию человека изменение гаметоцитов и эмбрионов для генерации наследственных изменений у людей было объявлено безответственным.
Российское сообщество генетиков в большинстве своем считает, что такие эксперименты на данный момент преждевременны и требуют более глубокого исследования и обсуждений.
«Вопрос клонирования уже давно стоит на горизонте. Этично ли выращивать клонов, чтобы потом забирать их органы для трансплантации человеку… Большой вопрос. Само собой, это абсолютно нормально, что нет единой точки зрения, ведь смысл подобных дискуссий как раз в том, чтобы найти правильные формулировки и отрегулировать потенциально спасительное, но при этом очень опасное знание», — говорит Алевтина Федина.
Страх неизвестности
Вариантов развития событий в области генной инженерии существует множество, и далеко не все они изучены и, в принципе, известны. Поэтому они должны быть последовательно зафиксированы и регламентированы.
Естественно, больше всего опасений вызывают плохие сценарии развития событий. Как правило, все начинается с помощи людям и изобретения новых лекарств. Но потом человек может прийти к желанию сделать своего ребенка светловолосым и зеленоглазым или создать армию универсальных солдат, не боящихся боли и не ведающих страха.
Олег Долгицкий, социальный философ, отмечает, что современное общество настолько неоднородно в культурном и экономическом плане, что любые методы, способные существенно изменить геном, могут создать условия не только для классового, но и видового расслоения, где представители «первого мира» смогут существенно продлевать свою жизнь и не бояться никаких болезней, в отличие от менее богатых людей. Это является серьезнейшей почвой для конфликтов и столкновений.
Эксперты убеждены, что генная инженерия — это будущее медицины. Возможность избавить младенца от пожизненного гнета заболевания, излечить людей от рака, найти лекарство против ВИЧ — за всем этим будет стоять генная инженерия. При этом желание человека изменить, например, цвет глаз или предотвратить наследственное заболевание, несмотря на все риски, будет только расти. И похоже, что остановить этот процесс уже не представляется возможным.