Гемосидерин что это такое
Гемосидероз
Гемосидероз (капиллярит, геморрагический пигментный дерматоз) – болезнь из разряда пигментных дистрофий, связанная с нарушением процессов обмена и избыточным накоплением гемосидерина в тканях и сосудах. Поражаются кожные покровы и внутренние органы. Отложения гемоглобиногенного пигмента могут быть распространенными либо местными. Установление природы заболевания затруднительно. Лечением занимаются дерматологи, пульмонологи, гематологи, иммунологи и другие специалисты.
Генерализованный гемосидероз
Общий или распространенный капиллярит характеризуется накоплением железосодержащего пигмента в структурах костного мозга, в клетках селезенки и печени. Ткани и органы приобретают буро-красный цвет. Пигментные изменения обусловлены системными процессами, следствием которых является эндоваскулярный (внутрисосудистый) гемолиз клеток крови.
Локальный гемосидероз
Местный капиллярит развивается из-за внесосудистого гемолиза эритроцитов. Гемосидерин накапливается в очаге кровоизлияний с образованием гематом в пределах кожи, легкого, печени, почек. Если депонирование железосодержащего пигмента влечет нарушение работы органа, развивается гемохроматоз.
Отдельные формы заболевания:
О причинах развития гемосидероза
Гемосидероз кожи может быть первичным и вторичным, развивающимся из-за повреждений и кожных инфекций.
Причинами первичного капиллярита кожи могут быть следующие факторы:
Вторичный гемосидероз дермы может быть обусловлен:
К факторам риска, способным спровоцировать развитие недуга, относят:
Генерализованный гемосидероз развивается на фоне предшествующих заболеваний. Чаще всего основными причинами являются системные заболевания крови, аутоиммунные болезни, тяжелые интоксикации и воздействие инфекционных агентов. Увеличенное депонирование гемосидерина может быть обусловлено:
Почему железосодержащий пигмент накапливается в легких – не вполне понятно. Часто причины кроются в генетической предрасположенности, во врожденной аномалии легочных капилляров, в имеющихся сердечных заболеваниях.
Характерные симптомы
Клинические проявления зависят от того, где накапливается гемоглобиногенный пигмент.
Гемосидероз легких
Идиопатический (первичный) гемосидероз легких проявляется следующими признаками:
Бурая пурпура легких, как правило, встречается в детском и в молодом возрасте, является серьезным заболеванием. При затяжном течении болезни очень часто развиваются рецидивирующие инфаркт-пневмонии и другие патологии.
Гемосидероз кожи
Характерны следующие симптомы:
Хронический гемосидероз дермы обычно диагностируют у мужчин старше 30 лет. Заболевание протекает без поражения внутренних органов.
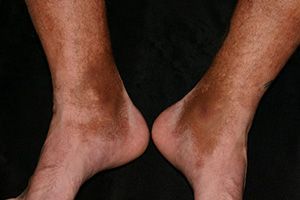
Пурпурозно-пигментный дерматоз печени проявляется увеличением органа, его болезненностью, желтушностью покровов, наличием пигментной сыпи на руках, в области подмышек, на лице. При поражении почек появляется отечность в ногах, диспепсия, изменения вкуса, боли в пояснице и пр.
Наши врачи
Диагностика
Врач-дерматолог осматривает пациента, исследует характер высыпаний, наличие характерных признаков. Обязательно проводятся лабораторные исследования – биохимия крови с определением уровня железа, общие анализы мочи, ПЦР-тесты. Анализируется содержание мокроты и мочи с проведением десфералового теста. Для уточнения диагноза пораженные сегменты направляют на биопсию. Гистологические исследования кожных покровов, костного мозга, легких, лимфатических тканей, печени, почек помогают обнаружить отложения пигмента. С целью диагностики может проводиться бронхоскопия с исследованием промывных вод, делается рентген грудной клетки, МРТ, компьютерная томография.
Лечебная тактика гемосидероза
Лечение назначается врачом-дерматологом и зависит от клинических проявлений и тяжести заболевания.
В тяжелых случаях врачи проводят спленэктомию, пациентам удаляют селезенку, чтобы добиться стойкой ремиссии. Прибегают к гемотрансфузии, PUVA-терапии, назначают препараты, способствующие выведению железа из организма.
Осложнения
Если пациент с капилляритом не получает должного лечения, то формируются опасные осложнения, способные привести к инвалидизации и летальному исходу. Особенно трудно поддается лечению запущенные формы гемосидероза легких, когда патологический процесс затрагивает альвеолы.
Гемосидероз кожи отличается благоприятным течением. При запущенных формах заболевания появляются косметические дефекты, которые требуют должной коррекции.
Профилактика
Рекомендации общие, так как механизм развития болезни изучен не до конца и не всегда удается установить причины гемосидероза.
Идиопатический гемосидероз легких. Причины, симптомы и лечение
1. Общие сведения
В длинном перечне диагнозов, обозначающих рассматриваемое здесь тяжелое заболевание, не хватает еще одного, – самого краткого и, возможно, самого точного: «железное легкое». Гемосидерин – продукт распада гемоглобина и денатурации белка ферритина.
Заметим, что греческое «сидерос» означает то же самое, что латинское «феррум», то есть железо. Ферритин – сложный белковый комплекс, который служит «кладовой» железа в организме. Гемосидерин – пигмент, который в больших объемах придает депонирующим его тканям характерный ржаво-бурый оттенок, поскольку содержит оксид железа.
Термин «гемосидероз», согласно канонам образования слов в медицине, должен означать явный, патологический избыток гемосидерина; в данном случае речь идет о его накоплении в легочной паренхиматозной ткани.
Такое состояние впервые описал выдающийся немецкий ученый-энциклопедист Рудольф Вирхов в 1864 году, и ему же принадлежит определение «бурая индурация легких». С тех пор прошло более полутора веков, однако у исследователей по сей день остается множество вопросов в связи с этим заболеванием. Найти ответы, да и просто установить правильный диагноз в данном случае очень трудно: гемосидероз легких встречается примерно один раз на миллион человек, – что чрезвычайно затрудняет и разработку диагностических критериев, и исследования патогенеза, – и лишь в последние годы его стали доказательно диагностировать прижизненно (ранее установить точный диагноз удавалось, в основном, при патологоанатомическом исследовании).
Гемосидероз встречается у лиц обоих полов и в любом возрасте. Однако накопленная к настоящему времени статистика выявляет, по некоторым источникам, двукратное преобладание мужчин среди заболевающих. Сообщается также о том, что заболевание манифестирует преимущественно в детском и юношеском возрасте.
2. Причины
Непосредственной причиной является проникновение и накопление эритроцитов в легочной паренхиме (с последующим высвобождением гемосидерина), – вследствие частых капиллярных кровотечений. Однако причина несостоятельности сосудистых стенок и повышенной их проницаемости, что приводит к избирательному депонированию именно оксида железа, остается неизвестной. Наиболее разработанными и аргументированными, на сегодняшний день, являются гипотезы о врожденной наследственной аномалии (что подтверждается, в частности, известными случаями семейного гемосидероза) и/или об аутоиммунно-аллергической природе заболевания (в пользу чего говорят случаи гемосидероза в сочетании с аллергической чувствительностью, а также терапевтическая эффективность гормональных средств). Кроме того, ряд авторов считают доказанной этиопатогенетическую роль инфекций, в первую очередь вирусных и, возможно, протозойных (малярийный плазмодий).
3. Симптомы
Течение идиопатического гемосидероза легких, как правило, волнообразное, хроническое, с чередованием ремиссий и обострений, выраженных в той или иной степени. Типичны симптомы гипохромной анемии и дыхательной недостаточности, кровохарканье, в наиболее тяжелых случаях – массивные легочные геморрагии. В периоды обострений отмечается кашель, затрудненное дыхание, тахикардия, общая слабость, иногда повышенная температура тела, боли в груди или абдоминальной области. Продолжительность ремиссий и кризовых обострений широко варьирует (от нескольких часов до нескольких недель). Заболевание постепенно прогрессирует, в отсутствие адекватной терапии состояние больного утяжеляется, и результатом нарастающей сердечно-легочной недостаточности, присоединяющегося пневмоторакса, закупорки бронхов свернувшейся кровью, инфаркта легких, – становится летальный исход.
Как указано выше, гемосидероз легких является очень сложным в диагностике заболеванием.
Необходимо самое тщательное изучение анамнеза, клиники, динамики, наследственности, иммунно-аллергического статуса, ряда биохимических показателей, рентгенографических данных, результатов функциональных дыхательных проб. Следует также дифференцировать идиопатический сидероз с множеством клинически сходных заболеваний.
4. Лечение
В последнее время стандартом терапевтического сопровождения больных гемосидерозом легких стали кортикостероидные гормональные средства. Многие авторы полагают более эффективным сочетание гормональной терапии с удалением селезенки. Симптоматически назначают также препараты, применяемые при лечении железодефицитных анемий; с той же целью по показаниям производят переливания препаратов крови.
Несмотря на то, что результаты такого комплексного подхода оцениваются в литературе как «обнадеживающие», прогноз остается неблагоприятным. Лишь при достоверно и правильно установленном диагнозе, интенсивном адекватном лечении и наблюдении продолжительность жизни больных превышает 10 лет; в среднем же, этот показатель пока остается на уровне 3-5 лет.
Перегрузка железом
Общая информация
Краткое описание
НАЦИОНАЛЬНОЕ ГЕМАТОЛОГИЧЕСКОЕ ОБЩЕСТВО
Рекомендации утверждены на IV Конгрессе гематологов России (апрель 2018г)
ПЕРЕГРУЗКА ЖЕЛЕЗОМ: ДИАГНОСТИКА И ЛЕЧЕНИЕ
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Наследственный гемохроматоз (НГ) – полисистемное заболевание, в основе которого лежат генетически обусловленные нарушения метаболизма железа, приводящие к его избыточному накоплению в организме и токсическому повреждению органов и тканей [4,10].
IV тип – генетическую основу составляют мутации гена SLC40A1, кодирующего синтез транспортного белка ферропортина [4,13].
Этиология и патогенез
Эпидемиология
Клиническая картина
Cимптомы, течение
Диагностика
Рекомендуется проводить осмотр, включающий измерение роста и массы тела, оценку состояния кожных покровов и костно-суставной системы; выявление гепатоспленомегалии, признаков дисфункции сердца, легких, печени, органов эндокринной системы.
Лечение
В Российской Федерации в настоящее время зарегистрирован 1 лекарственный препарат – хелатор железа: деферозирокс (Эксиджад). Деферазирокс является пероральным хелатором железа, период полувыведения которого составляет 8-16 часов, что позволяет принимать данный препарат 1 раз в день. Клинические исследования показали, что деферазирокс способен контролировать токсичный пул лабильного железа плазмы и удалять отложения железа из ткани печени и сердца.
Информация
Источники и литература
Информация
Рекомендации обсуждены на заседании Проблемной комиссии по гематологии (март 2018г).
Синдром перегрузки железом при хронических заболеваниях печени: фокус на неалкогольную жировую болезнь печени
Статья посвящена вопросам терапии синдрома перегрузки железом (СПЖ) при хронических заболеваниях печени (ХЗП). Рассмотрены роль железа и его метаболизм в организме человека, механизмы и диагностика СПЖ у пациента с ХЗП, особенности клинических проявлений
The article is dedicated to the issues of therapy of iron overload syndrome (IOS) in chronic hepatic diseases (CHD). Role of iron and its metabolism in human organism were considered, as well as the mechanisms and diagnostics of IOS in a patient with CHD, features of clinical manifestations of iron metabolism disorders and methods of IOS treatment.
На сегодняшний день синдром перегрузки железом (СПЖ) при хронических заболеваниях печени (ХЗП) недостаточно полно освещен в литературе и малоизвестен практикующему врачу. При этом СПЖ у данной категории больных часто является более тяжелым нарушением, нежели дефицит железа, и может приводить к необратимым последствиям [2, 5, 16].
В последние годы регистрируется высокая распространенность первичного СПЖ — наследственного гемохроматоза (НГ) в популяции (до 1:250 среди жителей Северной Европы, манифестные формы — 2:1000), а также обнаружены новые мутации в генах, регулирующих обмен железа [8, 18, 23]. Тогда как далеко не все клиницисты осведомлены, что вторичный СПЖ, возникающий при развитии ХЗП, в том числе при такой частой на сегодняшний день патологии, как неалкогольная жировая болезнь печени (НЖБП), наблюдается почти у каждого третьего пациента (в 20–30% случаев). Нередко при этом, по данным некоторых авторов, у 36,7% больных ХЗП обнаруживаются мутантные гены в гетерозиготном состоянии (C282/N, H63D/N), которые сами по себе не приводят к развитию НГ, однако при возникновении патологии печени способствуют манифестации СПЖ [18, 28].
Результаты исследований свидетельствуют, что раннее обнаружение и лечение СПЖ у пациентов с ХЗП позволяет предотвратить прогрессирование заболевания печени до цирротической стадии и значительно уменьшает риск гепатоцеллюлярной карциномы (ГЦК) [2, 4, 26, 31].
В этой связи необходимы новые подходы к диагностике, оценке клинической картины, лечению данного состояния и практическому специалисту актуально получение ответов на следующие вопросы:
Роль железа и его метаболизм в организме человека
В литературе последних лет появились новые данные о метаболизме железа (Fe) в организме человека, в связи с открытием белков-регуляторов, участвующих в обмене этого микроэлемента [1, 17, 20].
Известно, что железо является важнейшим элементом, участвующим в метаболизме организмов, живущих в среде, богатой кислородом. Обладая выраженными окислительно-восстановительными свойствами, оно необходимо для транспорта кислорода гемоглобином, синтеза дезоксирибонуклеиновой кислоты (ДНК), работы митохондриальных ферментов. Как металл с переменной валентностью, железо в составе негемовых энзимов (каталазы, пероксидазы, цитохрома) нейтрализует активные формы кислорода. Однако увеличение пула Fe III может являться катализатором образования свободных радикалов и инициатором оксидативного стресса. С целью компенсации, в организме предусмотрены естественные антиоксиданты — хелаторы Fe III, к которым относятся мочевая кислота (МК), церулоплазмин, супероксиддисмутаза, ферритин, трансферрин.
У человека в норме содержится около 3–4 г железа (40–50 мг Fe/кг). Суточная потребность в этом элементе в пище составляет около 10 мг для мужчин и 20 мг для женщин детородного возраста. При этом всасывается лишь 1–2 мг и почти столько же теряется со слущиваемым эпителием желудочно-кишечного тракта, эпидермисом, потом и мочой. Основная масса необходимого железа ежедневно поступает в циркуляцию из клеток ретикулоэндотелиальной системы (РЭС) (селезенка, печень, костный мозг).
Всасывание железа осуществляется эпителиальными клетками двенадцатиперстной кишки и начальных отделов тощей кишки и находится под строгим контролем белков-регуляторов обмена железа.
Известно, что гемовое железо (Fe II), находящееся в составе гемоглобина и миоглобина (в мясных продуктах), усваивается человеком на 20–30% независимо от желудочной секреции и состава пищи. Гемовое железо легко эндоцитируется энтероцитом после сливания с транспортером гемового железа (НСР1). Негемовое железо (Fe III), содержащееся в растительной пище, усваивается человеком на 1–7% и во многом зависит от сопутствующих пищевых факторов (табл. 1).
Всасывание негемового железа — сложный энергозависимый транспортный процесс. Оно происходит после восстановления Fe III до Fe II при помощи соляной кислоты желудочного сока и дуоденального цитохрома — ферроредуктазы (Dcyt b). Затем Fe II переносится в энтероцит специальным транспортером двухвалентных ионов (ДMT1).
Часть железа, которая не используется клеткой, депонируется в виде ферритина и гемосидерина в печени, селезенке, костном мозге, мышечной ткани. Ферритин — внутриклеточный комплекс, содержащий белок-апоферритин, связывающий до 4 тысяч атомов железа. Существует 5 изоформ ферритина: щелочные изоформы печени и селезенки отвечают за депонирование железа, а кислые изоформы миокарда, плаценты, опухолевых клеток являются посредниками в процессах синтеза и участвуют в регуляции Т-клеточного иммунного ответа. Поэтому ферритин является еще и белком острого воспаления и опухолевого роста. Гемосидерин — нерастворимая часть ферритина, форма депонирования избыточного железа.
Поступление железа (Fe II) в кровь из энтероцита, а также из клеток печени, макрофагов селезенки, костного мозга осуществляется единственным белком-переносчиком — ферропортином. В 2001 г. был открыт важнейший регулятор обмена железа и функции ферропортина — гепсидин. Этот белок, состоящий из 25 аминокислот, синтезируется печенью, а также, по некоторым данным, клетками жировой ткани при ожирении [24].
Ранее он был известен как белок острой фазы, обладающий антибактериальными свойствами, благодаря способности уменьшать поступление железа к микроорганизмам, блокировать их размножение, разрушать бактериальные мембраны. Основными стимуляторами синтеза гепсидина при воспалении являются провоспалительные цитокины — ИЛ-6 и ФНО-а. На сегодняшний день известно, что именно гепсидин, уровень которого повышается при воспалении, а также опухолевом процессе, играет основную роль в развитии анемии хронического воспаления [35]. Гепсидин регулирует сывороточную концентрацию железа, путем «выключения» работы ферропортина (в этом случае железо накапливается в энтероцитах, макрофагах, гепатоцитах). При повышении железа в крови — увеличивается синтез гепсидина. В результате блокируются процессы всасывания (угнетается работа ДMT1), рециркуляции и высвобождения железа из депо.
Транспорт железа от энтероцитов и органов-депо к костному мозгу и другим тканям осуществляет трансферрин, синтезируемый печенью. Этот белок способен переносить только Fe III. Поэтому на поверхности мембран клеток происходит окисление Fe II в Fe III при помощи ферментов-ферроксидаз — гефестина и церулоплазмина. Трансферрин является отрицательным белком острой фазы.
Железо (Fе III), связанное с трансферрином, поступает внутрь клетки посредством специальных трансферриновых рецепторов 1-го и 2-го типа (TfR). Под действием внутриклеточных ферроредуктаз Fe III вновь восстанавливается в Fe II. Синтез трансферриновых рецепторов в клетке зависит от ее потребностей в железе и строго регулируется системой внутриклеточных белков (IRP1, IRP2, IRE). Образование комплекса трансферрина с TfR и их эндоцитоз внутрь клетки контролируется белком HFE, при мутации гена которого развивается НГ.
Механизмы развития СПЖ
По имеющимся на сегодняшний день данным, организм человека не имеет средств контроля за экскрецией железа. Интестинальная абсорбция — основной этап, который тщательно регулируется. Поэтому любые ситуации, связанные с избыточным поступлением железа в кровь (при парентеральном введении препаратов железа, переливании крови, гемолизе) или всасыванием (наследственные и приобретенные механизмы), могут приводить к СПЖ.
Таким образом, развитие СПЖ обуславливается как наследственными причинами, так и приобретенными факторами (табл. 2).
Среди основных этиологических факторов можно выделить «триаду»:
1) гемолиз эритроцитов (сидероахрестические анемии, талассемия, недостаточность глюкозо-6-фосфатдегидрогеназы, микросфероцитоз, дефицит витамина В12);
2) избыточное экзогенное поступление железа (диета, многократные гемотрансфузии, длительное бесконтрольное применение парентеральных препаратов железа, хронический гемодиализ);
3) заболевания печени (хронический вирусный гепатит С, реже В, алкогольная болезнь печени, НЖБП, кожная порфирия).
При СПЖ железо оказывает негативное влияние на организм. Перенасыщение трансферрина железом сопровождается включением дополнительного транcпорта железа, связанного с альбумином. Данный комплекс легко проникает в клетки, не предназначенные для депонирования железа (миокард, гонады, поджелудочная железа и др.), и вызывает токсические эффекты. При избыточном накоплении железа в органах-депо, а также тканях, не являющихся таковыми, происходит усиление образования коллагена и прямое повреждение ДНК. При переходе Fe III в Fe II образуются токсичные свободные радикалы, активирующие процессы перекисного окисления. При выраженном СПЖ в организме работа собственных антиоксидантных систем защиты становится неэффективной.
Тем не менее патогенез СПЖ у больных с ХЗП остается не до конца ясным. Возможными механизмами могут являться:
Признаки СПЖ
СПЖ выявляется при оценке совокупности признаков:
1. Клинические признаки
В зависимости от причины СПЖ весьма вариабельны. Могут наблюдаться проявления стеатоза или цирроза печени, меланодермия, гипогонадизм, дисфункция надпочечников, гипотиреоз, артропатия, сахарный диабет 2-го типа, гиперурикемия [5, 13, 18, 29].
2. Лабораторные маркеры СПЖ
Показатели клинического анализа крови при СПЖ не являются специфичными, гемоглобин, эритроциты, цветовой показатель могут быть даже снижены (например, при гемолитической анемии, талассемии). При НГ, а также СПЖ, связанном с ХЗП, нередко обнаруживается повышение уровня гемоглобина.
Согласно мнению специалистов, лабораторными маркерами СПЖ являются [26]:
Рекомендации Европейского общества по изучению заболеваний печени (European association for the study of the liver, EASL) по лабораторной диагностике СПЖ, 2010 [26]:
Как правило, при воспалении повышение ферритина сочетается с нормальными показателями НТЖ. В ряде случаев требуется учитывать, что повышение НТЖ может быть «ложным» при печеночно-клеточной недостаточности и снижении синтеза трансферрина, а также при синдроме мальабсорбции белков. Однако, по мнению специалистов, НТЖ — самый информативный показатель статуса железа и может использоваться для скрининга патогенетически значимых нарушений обмена железом у больных с ХЗП [18].
3. Генетическое тестирование
Применяется для исключения первичного СПЖ. На сегодняшний день доступными методами диагностики НГ являются:
Рекомендации EASL по генетическому тестированию, 2010 [26]:
4. Морфологическое исследование
Для подтверждения СПЖ в случаях, когда его маркеры сомнительны, а также в целях дифференциальной диагностики заболеваний печени показано проведение биопсии печени с окраской берлинской лазурью на железо (гемосидерин) по Перлсу и определением количественного содержания железа в препарате (печеночный индекс железа (ПИЖ) — Fе в печени/возраст). При НГ данный показатель более 1,9.
Рекомендации EASL по проведению гепатобиопсии при СПЖ, 2010 [26]:
5. МРТ печени и сердца в режиме Т2
Может использоваться как метод дополнительного измерения содержания железа в печени, а также миокарде, как альтернатива биопсии [11].
6. Десфераловая проба
Проводится в сомнительных случаях СПЖ и при необходимости проведения дифференциального диагноза между первичным и вторичным СПЖ. После внутримышечго введения 0,5 г Десферала производится последующий анализ суточной экскреции железа. В норме этот показатель составляет менее 1 мг/сут (менее 18 мкмоль/л), при СПЖ — 18–27 мкмоль/л, при НГ — более 27 мкмоль/л [4, 11].
Механизмы развития и клинические проявления СПЖ при НЖБП
На сегодняшний день установлено, что СПЖ обнаруживается примерно у 1/3 больных НЖБП: у 30% пациентов с жировым гепатозом (ЖГ), у 34% больных с неалкогольным стеатогепатитом (НАСГ) [4, 6, 15].
Впервые СПЖ у пациентов с НЖБП был описан в 1997 г. R. Moirand и Y. Deugnier, которые предложили термин «дисметаболический синдром перегрузки железом» (ДСПЖ, Dysmetabolic iron overload syndrome (DIOS)) [25]. В 1999 г. M. Mendler и соавт. доказали наличие СПЖ у пациентов с ИР и метаболическим синдромом (Insulin resistance hepatic iron overload syndrom (IR-HIO)) [32]. Был описан «железный фенотип» синдрома ИР. В 2008 г. A. Riva и соавт. предложили критерии синдрома DIOS/IR-HIO [34].
Важно знать, что СПЖ у данной категории пациентов является фактором риска, предрасполагающим к развитию и прогрессированию ИР, СД и сердечно-сосудистых заболеваний. Так, установлено, что высокий ферритин более 400 мкг/л у мужчин и более 300 мкг/л у женщин с ожирением является маркером ИР [34]. Гиперферритинемия, при исключении воспалительного процесса, требует тщательного контроля за уровнем гликемии у больных НЖБП, так как увеличивает риск СД в 4,6 раза [16]. Повышенный уровень ферритина может быть также предиктором стеатоза печени и предшествовать его развитию, что свидетельствует о том, что причиной гиперферритинемии является не НЖБП, а гиперферритинемия, связанная с ожирением и ИР, что приводит к НЖБП [14, 15].
В основе развития СПЖ при НЖБП лежит ИР, гипергликемия и висцеральное ожирение.
При ИР и гиперинсулинемии происходит повышенная транслокация трансферриновых рецепторов на мембранах гепатоцитов, энтероцитов, приводящая к увеличению поступления железа в клетку и стимулированию синтеза ферритина [27]. В свою очередь, при перегрузке железом гепатоцитов нарушается поглощение и деградация инсулина печенью, что усугубляет гиперинсулинемию. Избыток железа (Fe III), катализируя образование свободных радикалов, нарушает процесс проведения инсулинового сигнала и соединение инсулина с инсулиновым рецептором. Стимулируется синтез глюкозы в печени. При стойкой гипергликемии возникает гликирование трансферрина, приводящее к нарушению связывания Fe III и его транспорта к органам-потребителям.
Абдоминальная жировая ткань, обладающая собственной гормональной активностью, при липолизе выделяет провоспалительные цитокины (ФНО, ИЛ-6, ИЛ-8, ИЛ-10), что приводит к инфильтрации жировой ткани макрофагами, которые активно накапливают железо. Это индуцирует окислительный стресс и воспалительную реакцию. Таким образом, формируется порочный круг. Повышенная продукция вышеперечисленных цитокинов стимулирует синтез гепсидина, причем не только в гепатоцитах, но и в клетках жировой ткани [24]. Гепсидин блокирует работу ферропортина, в результате чего тормозятся процессы абсорбции пищевого железа, высвобождения железа из клеток, соответственно, стимулируется синтез ферритина. При этом, в результате повышенного синтеза гепсидина, у некоторых пациентов, чаще подростков и фертильных женщин, а также лиц с морбидным ожирением (индекс массы тела более 40), может даже развиваться анемия хронического воспаления, с недостаточностью железа, вследствие уменьшения его всасывания в тонкой кишке и перераспределения в клетки РЭС, а не на нужды синтеза гемоглобина [6, 7, 14].
Этот «железодефицитный» фенотип ожирения характеризуется как признаками относительного железодефицита, так и ДСПЖ. В данном случае оценка такого параметра крови, как количество растворимых трансферриновых рецепторов, может помочь в диагностике истинного дефицита железа, так как не зависит от активности воспалительного процесса, влияющего на содержание ферритина. Дополнительным предиктором наличия «функционального» дефицита железа служит также уровень С-реактивного белка.
Преимущественное накопление железа в гепатоцитах и клетках Купфера в перисинусоидальном пространстве запускает процессы проапоптоза, некроза, коллагенообразования и является триггерным механизмом прогрессирования ЖГ в НАСГ, с последующим развитием ФП, ЦП и ГЦК.
Дополнительным фактором, усугубляющим СПЖ у пациентов с НЖБП, по мнению некоторых авторов, может быть нарушение экскреции МК почками (например, при диабетической нефропатии) [5]. МК, являясь естественным хелатором негемового железа (Fe III), в условиях гиперферремии усиленно продуцируется в ксантинооксидазной реакции. Первоначально повышение уровня МК в крови и/или ее экскреции с мочой свидетельствует о включении компенсаторной реакции организма, Так, при НТЖ ниже 30%, повышение МК и ее экскреции способствует адекватному выведению с мочой избытка железа и поддержанию его физиологического уровня. При НТЖ 30–45% наблюдается более выраженное повышение МК, при недостаточно эффективной экскреции. При НТЖ более 45% уровень урикемии не соответствует механизму антиоксидантной защиты [5].
Критерии постановки диагноза ДСПЖ:
1) наличие двух и более компонентов метаболического синдрома (ожирение, дислипидемия, артериальная гипертензия, гипергликемия или нарушение толерантности к глюкозе);
2) гиперферритинемия при нормальном или незначительно повышенном НТЖ;
3) наличие стеатоза печени;
4) легкое или умеренное повышение содержания железа в печени (по данным МРТ или гепатобиопсии, ПИЖ менее 1,9 (рис. 1)).
Дополнительными маркерами СПЖ при НЖБП могут служить также повышение уровня гепсидина (определение данного показателя в настоящее время малодоступно), МК в крови и/или ее суточной экскреции с мочой.
Лечение СПЖ при ХЗП
Согласно мнению большинства специалистов, показаниями для лечения СПЖ у больных ХЗП являются:
1) клинически манифестный НГ;
2) повышение ферритина более 200 мкг/л у женщин и более 300 мкг/л у мужчин и женщин в постменопаузе или более 500 мкг/л у мужчин моложе 40 лет и у женщин до наступления менопаузы (при исключении острого воспаления, опухолевого процесса, алкогольного эксцесса);
3) НТЖ более 45%;
4) при НЖБП целесообразно рассматривать дополнительное показание: НТЖ 30–45% в сочетании с гиперурикемией и/или повышенной суточной экскрецией мочевой кислоты и гипергликемией [5].
Способы лечения СПЖ при ХЗП включают: этиотропную терапию, строгий отказ от алкоголя, соблюдение диеты с ограничением содержания железа до 8–10 мг/сут, лечебные кровопускания (флеботомии), с эксфузией до 300–400 мл крови 1 раз в неделю, до достижения целевого уровня ферритина ≤ 50 мкг/л и НТЖ ≤ 30%, использование антиоксидантов.
Согласно клиническим рекомендациям Европейских обществ по изучению заболеваний печени, ожирения и диабета (EASL, Европейского общества изучения диабета (European association for the study of diabetes, EASD), Европейского общества изучения ожирения (European Association for the Study of Obesity, EASO)), проведение флеботомии с целью уменьшения запасов железа почти до уровня железодефицита улучшает статус больных НЖБП по шкале NAS без прогрессирования фиброза, однако необходимы дополнительные данные. Как свидетельствуют специалисты, флеботомии при НЖБП уменьшают ИР, выраженность воспалительных изменений в печени, замедляют темпы прогрессирования фиброза печени и риски развития ГЦК [12].
При противопоказаниях к флеботомии (прежде всего, в случае НГ с повышением уровня ферритина более 1000 мкг/л, сочетающимся с анемией средней и тяжелой степени, выраженной гипотонией, гипоальбуминемией, СН) используются хелаторы железа (деферазирокс (Эксиджад), менее предпочтителен дефероксамин (Десферал)). Однако высокая стоимость препаратов и возможные побочные эффекты (диспептические расстройства, нарушение функции почек, печени, зрения, слуха и др.) ограничивают их применение.
В терапию СПЖ всем больным целесообразно включать антиоксиданты. Для этого могут применяться препараты янтарной кислоты, урсодезоксихолевая кислота (Урдокса), глицирризиновая кислота, липоевая кислота, адеметионин [5, 9].
Так, например, установлено, что антиоксидантный эффект янтарной кислоты связан с повышением активности глутатионпероксидазы и каталазы, важнейших ферментов, участвующих в разрушении активных форм кислорода, перекисей. Препарат также способствует увеличению уровня восстановленного глутатиона и подавлению активности ксантиноксидазы, что приводит к снижению продукции высокоактивных форм кислорода [9].
Глицирризиновая кислота как антиоксидант способна ингибировать образование супероксидного радикала и перекиси водорода [10].
Антиоксидантное действие урсодезоксихолевой кислоты связано с изменением метаболизма простагландинов и жирных кислот, а также снижением оксидативной активации клеток Купфера гидрофобными желчными кислотами. Несомненным достоинством данного препарата у пациентов с ХЗП и СПЖ является опосредованное антифибротическое действие, обусловленное снижением содержания активаторов фиброгенеза и угнетением активности звездчатых клеток [22, 30]. В исследовании J. Holoman и соавт. [38] продемонстрировано, что на фоне применения УДХК снижалась сывороточная концентрация N-терминального пептида коллагена III типа и матриксных металлопротеиназ и одновременно повышался уровень их тканевых ингибиторов, что клинически выражается в замедлении развития фиброза.
ФГБОУ ВО СПбГМУ им. И. П. Павлова МЗ РФ, Санкт-Петербург
Синдром перегрузки железом при хронических заболеваниях печени: фокус на неалкогольную жировую болезнь печени/ С. Н. Мехтиев, О. А. Мехтиева
Для цитирования: Лечащий врач №12/2017; Номера страниц в выпуске: 60-67
Теги: гемохроматоз, метаболизм, наследственность, метаболизм железа




.gif)
.gif)