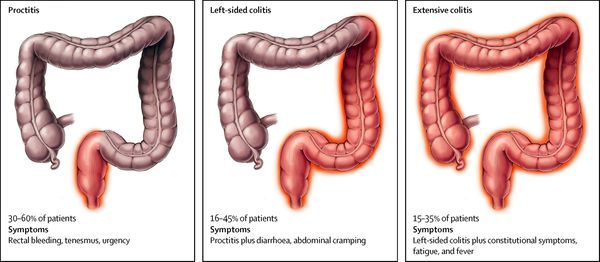
Геморрагический колит что это
Антибиотикоассоциированный колит, тяжелого течения. Разбор клинического случая
Авторы клинического разбора:
Ивашкин Владимир Трофимович – академик РАМН, профессор, заведующий кафедрой проведевтики внутренних болезней и директор клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии Первого МГМУ им И.М. Сеченова.
В клинику обратился пожилой мужчина 62 лет с жалобами на жидкий стул до 8 раз в сутки, повышение температуры тела до 38-39С, боль в околопупочной области спастического характера, общую слабость и похудание на 7 кг в течение месяца.
При объективном осмотре состояние средней тяжести, 38С, кожа и видимые слизистые бледные, язык сухой, живот увеличен в объеме за счет метеоризма, при пальпации умеренно болезненный по ходу толстой кишки.
Требовалось установить предварительный диагноз. Отрицательные результаты исследования кала на дизгруппу ставили под сомнение наличие кишечной инфекции, дебют воспалительных заболеваний кишечника у мужчины в 62 года представлялся маловероятным. Имеющиеся факторы риска антибиотикоассоциированного колита – прием антибиотиков, пожилой возраст, наличие сопутствующей патологии (ишемическая болезнь сердца, гипертоническая болезнь) свидетельствовали с высокой вероятностью о наличии антибиотикассоциированного колита, тяжелого течения (псевдомембранозный?).
Было начато обследование. В анализах крови обращали на себя внимание нормохромная железодефицитная анемия, лейкоцитоз со сдвигом лейкоцитарной формулы влево вплоть до миелоцитов, тромбоцитоз и ускорение СОЭ. Также выявлена гипонатриемия, гипоальбуминемия, снижение уровня железа, резкое повышение уровня С-реактивного белка, реакция кала на скрытую кровь с бензидином – положительная. При исследовании кала методом ИФА обнаружены токсины А и В C.difficile. Для исключения дилатации толстой кишки был сделан обзорный снимок брюшной полости в положении лежа – ширина петель в пределах нормы. При ультразвуковом исследовании брюшной полости обращало на себя внимание утолщение стенок толстой кишки до 10 мм. Утолщение стенок толстой кишки, сужение просвета кишки отмечалось и при компьютерной томографии органов брюшной полости.
При сигмоскопии: аппарат введен в сигмовидную кишку, на осмотренных участках слизистая умеренно гиперемирована, с множественными белесоватыми включениями. Слизистая прямой кишки гиперемирована, отёчна. Заключение: антибиотикоассоциированный колит (псевдомембранозный). (Рис. 2).
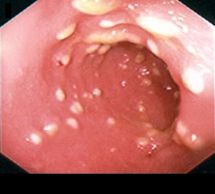
Рис. 2. Сигмоскопия
Морфологическая картина соответствовала псевдомембранозному колиту: выявлялся некроз эпителия, фибриновый выпот с нейтрофилами, типичные изъязвления слизистой напоминающие извержения вулкана, формирование псевдомембран (Рис.3).
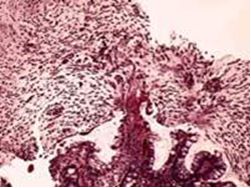
Рис. 3. Морфологическая картина псевдомембранозного колита
Таким образом, был установлен следующий клинический диагноз: Антибиотикоассоциированный колит, тяжелого течения (псевдомембранозный). Синдром нарушенного всасывания: железодефицитная анемия. Гипоальбуминемия.
Лечение больного включало регидратационную терапию, парентеральное питание, с дальнейшим переводом на энтеральное питание, метронидазолом 500 мг в/в каждые 6 ч, ванкомицином 250 мг 4 раза в сутки. Пробиотические препараты не назначались. На фоне лечения состояние больного улучшилось, нормализовалась температура тела, постепенно уменьшилась частота стула и общая слабость, больной прибавил в весе и был выписан в удовлетворительном состоянии.
Через 2 недели после выписки из стационара больному была назначена антибиотикотерапия после экстракции зуба, которая была прервана на 2-е сутки в связи с возникновением диареи. Больной обратился в нашу клинику. Был заподозрен рецидив C.difficile-ассоциированного колита, что было подтверждено обнаружением токсинов C.difficile в кале. Назначена терапия ванкомицином в начальной дозе 500 мг 2 раза в сутки с последующим постепенным снижением дозы в комбинации с пробиотическим препаратом Флорасан А по 1 капсуле 3 раза в день на 14 дней. Состояние больного быстро улучшилось, в течение 1 года наблюдения рецидивов диареи не отмечалось.
Пробиотические препараты (Флорасан А) оказывают отчетливый эффект в лечении антибиотикоассоциированного колита, что делает актуальным включение пробиотиков в схемы лечения. Важными элементами профилактики антибиотикоассоциированных поражений кишечника служат дифференцированное назначение антибиотиков под строгим и обязательным контролем врача, а также обязательное назначение пробиотиков одновременно с началом антибактериальной терапии.
Геморрагический колит
, MD, MPH, University of North Carolina School of Medicine
Геморрагический колит может быть вызван токсинами, вырабатываемыми кишечной палочкой.
Микроорганизмы, вызывающие расстройство, обычно попадают в организм из зараженной говядины, воды или непастеризованного молока.
Частые симптомы — колики и диарея, иногда с кровью.
Диагноз основывается на оценке врача и результатах анализов кала.
Профилактические меры включают тщательное приготовление мяса и тщательное мытье рук.
Лечение предусматривает потребление большого количества жидкости.
Геморрагический колит может поражать людей всех возрастов, но наиболее распространен среди детей и пожилых людей. Существует много штаммов Escherichia coli ( E. coli), вызывающих геморрагический колит. В Северной Америке наиболее распространенный штамм E. coli Инфекция E. coli O157:H7 Escherichia coli (E. coli) — это группа грамотрицательных бактерий, которые обитают в кишечнике здоровых людей. Однако некоторые штаммы могут вызывать инфекцию в пищеварительном тракте, мочевыводящих. Прочитайте дополнительные сведения ― O157:H7. Эти бактерии в естественных условиях встречаются в кишечнике примерно у 1 % здорового крупного рогатого скота. Вспышки заболевания могут быть вызваны употреблением в пищу недостаточно обработанного говяжьего фарша, непастеризованного молока или сока. Употребление пищи или воды, загрязненных коровьим навозом или сырым говяжьим фаршем, также может способствовать распространению инфекции. Заболевание может передаваться от человека к человеку, особенно от детей в подгузниках другим людям. Недостаточно хлорированная вода в аквапарках может быть источником инфекции.
Токсины E. coli повреждают слизистую оболочку толстой кишки. Если токсины попадают в кровоток, они могут также поражать другие органы, такие как почки.
Симптомы геморрагического колита
Сильные кишечные колики начинаются внезапно вместе с водянистой диареей, которая может приобрести кровавую форму в течение 24 часов. Диарея обычно продолжается от 1 до 8 дней. Температура обычно не повышается или повышается незначительно, но иногда температура может превысить 39 °C.
Примерно у 5–10 % пациентов с геморрагическим колитом развивается тяжелое осложнение, называемое гемолитико-уремическим синдромом Гемолитико-уремический синдром (ГУС) Гемолитико-уремический синдром (ГУС) — это серьезное заболевание, возникающее обычно в детском возрасте и проявляющееся в образовании небольших сгустков крови по всему телу, которые блокируют. Прочитайте дополнительные сведения ). Симптомы включают низкое количество эритроцитов (анемию, характеризующуюся утомляемостью, слабостью и бледным цветом кожи), вызванное разрушением эритроцитов (гемолитическая анемия), низкое количество тромбоцитов (тромбоцитопения Общие сведения о тромбоцитопении Тромбоцитопения — это низкий уровень тромбоцитов в крови, который приводит к повышению риска кровотечения. Тромбоцитопения возникает в том случае, если костный мозг производит слишком мало тромбоцитов. Прочитайте дополнительные сведения 
Диагностика геморрагического колита
Врач обычно подозревает геморрагический колит, когда у пациента диарея с кровью. Чтобы поставить диагноз геморрагического колита, врач отправляет образец кала на анализ на наличие штаммов E. coli или токсинов, которые они вырабатывают.
Другие исследования, такие, как сигмоидоскопия, могут проводиться в случаях, когда врач подозревает, что диарея с кровью может быть обусловлена другими заболеваниями.
Профилактика геморрагического колита
Тщательное приготовление мяса
Внедрение более эффективных процедур переработки мяса в Соединенных Штатах помогло снизить показатель загрязнения мяса E. coli. Несмотря на эти меры, говяжий фарш все равно может быть заражен. Таким образом, говяжий фарш следует готовить до внутренней температуры 71 °C, или до того, как он перестанет давать соки. Следует пить только пастеризованное молоко и употреблять пастеризованные молочные продукты.
Следует правильно утилизировать кал инфицированных людей, хорошо соблюдать гигиенические процедуры и мыть руки с мылом, чтобы ограничить распространение инфекции. У детей не должно больше быть диареи и должно быть два отрицательных результата анализа кала, прежде чем им разрешат вернуться в детский сад.
Следует сообщать о вспышках кровавого поноса в органы здравоохранения, поскольку вмешательство может предотвратить инфицирование других людей. Сообщить можно, связавшись с местным Департаментом здравоохранения, воспользовавшись информацией на их веб-сайте или в телефонной книге.
Лечение геморрагического колита
Иногда вводить жидкости внутривенно
Наиболее важным аспектом лечения геморрагического колита является потребление достаточного количества жидкостей. Однако иногда организм теряет так много жидкости, что врач должен восстановить недостаток жидкости через вену (внутривенно). Антибиотики не назначают, так как они фактически увеличивают риск развития гемолитико-уремического синдрома. Это расстройство в конечном итоге проходит само по себе.
Людям, у которых развиваются осложнения, с большей вероятностью требуется интенсивный уход в больнице и может потребоваться почечный диализ Диализ Диализ — это процесс искусственного выведения продуктов жизнедеятельности и избыточной жидкости из организма. Этот процесс необходим тогда, когда почки не в состоянии выполнять свою функцию. Прочитайте дополнительные сведения 
Знаете ли Вы, что.
Антибиотики не назначают при геморрагическом колите, который считают вызванным E. coli, поскольку они не облегчают симптомы, не предотвращают распространение инфекции и фактически увеличивают риск развития гемолитико-уремического синдрома.
Что такое колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Куракин А. А., проктолога со стажем в 10 лет.
Определение болезни. Причины заболевания
Колит (лат. colitis, от греч. kolon (толстый кишечник) и itis (воспаление) — собирательное понятие, включающее большую группу заболеваний с одним общим признаком: воспалением толстого кишечника.
Основные признаки колита: частый жидкий стул с кровью, боль в животе и высокая температура.
Колиты встречаются в практике гастроэнтерологов, инфекционистов, терапевтов, колопроктологов, хирургов и других специалистов.
Этиология колита
Основные формы колитов можно описать только по отдельности, в зависимости от этиологического фактора. Размеры статьи не позволяют коснуться всех видов колита. Рассмотрим только основные из них.
Инфекционный колит — это заболевание кишечника, возникающее из-за активизации условно-патогенных микроорганизмов в кишечнике или попадания новых болезнетворных микробов из внешней среды. [1]
Инфекционный колит имеет очень широкое распространение: нет человека, ни разу не переносившего данное заболевание. Количество заболевших увеличивается в жаркий период, когда создаются благоприятные условия для распространения инфекции. Поэтому чаще болеют люди в регионах с жарким климатом (Африка, Юго-Восточная и Средняя Азия). Заболевание чаще встречается в детском возрасте, особенно у детей, посещающих учебные заведения (детские сады, школы и т. д.). Гастроэнтерологи и проктологи могут встречать в практике больных с данной патологией, но она не является профильной. Лечат заболевание обычно инфекционисты.
Причины инфекционного колита:
Формы инфекционного колита:
Воспалительные явления могут иметь стадийный характер, а могут сразу иметь картину запущенного воспаления. Его выраженность напрямую зависит от характера инфекции. Некротическое и флегмонозно-гангренозное воспаление встречается при клостридиальной инфекции. Катарально-геморрагическое — при дизентерии. Катаральное воспаление встречается чаще при вирусных заболеваниях. [2]
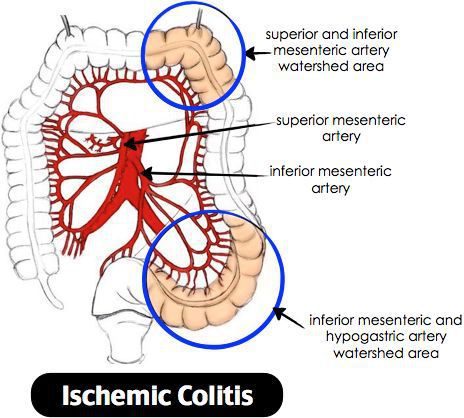
Ишемический колит — воспаление стенки толстого кишечника, возникающее из-за нарушения процессов кровобращения. Существует хроническое и острое нарушение кровообращения. [3]
Причиной нарушения кровообращения является полное прекращение или критическое снижение притока крови к толстой кишке, вследствие чего возникает воспаление. При тяжёлом течении может приводить к некрозу стенки кишечника. Причиной закупорки сосудов могут быть тромбы, но чаще всего к сужению просвета сосуда приводят атеросклеротические бляшки. Поэтому болезнь чаще проявляется у лиц пожилого возраста. Около 79% больных ишемическим колитом старше 48 лет. [4] Частота встречаемости не имеет связи с половой принадлежностью и регионом. Впервые открыт в 1966 году. Ишемический колит является профильным заболеванием для колопроктологов, но им также занимаются общие хирурги и гастроэнтерологи. [5]
Причины ишемического колита:
Закупорка просвета сосуда приводит к ишемии стенки кишки, а как следствие — к некрозу и далее перфорации. [6]
Объём поражения зависит от размера питающей артерии, длительности закупорки. Если закупорка сосуда происходит постепенно (при образовании атеросклеротических бляшек в сосудах), то говорят о хроническом нарушении кровообращения, что в свою очередь приводит к стриктурам.
При критических состояниях и снижении давления крови (например, анафилактический шок, ДВС-синдром и т.д.), происходит централизация кровообращения, при этом резко снижается приток крови к кишечнику, что приводит к ишемии и некрозу.
При атеросклерозе чаще страдает сигмовидная и поперечная ободочная кишка. Воспаление начинается со слизистой оболочки, затем переходит на все слои. [7]
По характеру поражения выделяют:
Лучевой колит — образуется в результате ионизирующего воздействия на стенку толстого кишечника.
Симптомы колита
Симптомы острого и хронического колита: боль в животе, кровь в кале, диарея, высокая температура, слабость, слизь и кровь в стуле, спазмы.
Симптомы язвенного колита: к перечисленным выше признакам добавляются боли в анусе и анемия.
Боли при колите кишечника:
Инфекционный колит
Клиника инфекционного колита напрямую зависит от возбудителя.
Для любого инфекционного колита независимо от этиологии характерно:
Для первичной оценки этиологии инфекционного колита оценивают характер дефекации, объём и особенности каловых масс.
Ишемический колит
Симптоматика очень вариабельна, характерно быстрое прогрессирование.
Лучевой колит
Обычно колит формируется у лиц, перенёсших курс лучевой терапии по поводу новообразований, локализующихся в области малого таза или брюшной полости. [12]
Патогенез колита
Толстый кишечник очень восприимчив к ионизирующему излучению. [10] Лучевой колит возникает при воздействии малых доз облучения: происходит атрофия слизистой оболочки (сразу после облучения).
Классификация и стадии развития колита
По течению:
По этиологии:
По локализации:
| Вид колита | Локализация |
|---|---|
| проктит | воспаление прямой кишки |
| панколит | тотальное поражение кишечника |
| тифлит | воспаление слепой кишки |
| трансверзит | воспаление поперечной ободочной кишки |
| сигмоидит | воспаление сигмовидной кишки |
| диффузный колит кишечника | охватывает два и более отдела кишечника |
Поражение кишечной стенки подразделяют на три вида:
Осложнения колита
Диагностика колита
Инфекционный колит:
Ишемический колит:
Лучевой колит:
Лечение колита
Инфекционный колит:
Ишемический колит:
Показаниями для срочного хирургического лечения служат:
Терапия лучевого колита схожа с терапией язвенного колита и болезни Крона:
Может быть полезно вести дневник питания, чтобы отслеживать, что вы едите, а также свои чувства. Если вы обнаружите, что некоторые продукты вызывают обострение ваших симптомов, вы можете попробовать их устранить.
Диетотерапия
Убедительных доказательств того, что неправильное питание приводит к воспалению кишечника, нет. Но оно может усугубить симптомы болезни, особенно при обострении. Поэтому полезно вести дневник питания и отслеживать свои реакции на определённые продукты.
Прогноз. Профилактика
На сегодняшний день хорошо известны причины возникновения инфекционного колита, разработаны современные методики лечения. Поэтому при неосложненном течении и вовремя начатой терапии удается достигнуть полного выздоровления. Менее благоприятный прогноз у лиц с явлениями иммунодефицита и ослабленной иммунной системой (например, у людей пожилого возраста). Прогноз благоприятный.
Основными методами профилактики являются:
При транзиторной форме ишемического колита прогноз благоприятный. При гангренозной форме — зависит от вовремя поставленного диагноза и проведенного лечения.
Так как ишемический колит является осложнением других болезней, то для его профилактики необходимо:
Лучевой колит приводит к постоянным, необратимым изменениям кишечной стенки, поэтому прогноз неблагоприятный.
При радиационном колите могут появляться язвы и стриктуры на слизистой оболочке толстого кишечника, что может привести к кишечной непроходимости. В таком случае необходимо хирургическое лечение, от своевременности которого зависит прогноз. При правильном и вовремя проведенном лечении прогноз благоприятный. Специальных методов профилактики лучевого колита не существует.
Неинфекционный гастроэнтерит и колит неуточненный (K52.9)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Примечание 1
В данную подрубрику включены следующие клинические понятия:
— неинфекционная диарея;
— неинфекционный энтерит;
— неинфекционный сигмоидит;
— неинфекционный еюнит;
— неинфекционный илеит.
Примечание 2. Перечень терминов, описывающих колит, применительно к данной подрубрике:
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
По патогенезу:
— первичный колит (изолированное поражение);
— вторичный колит (осложнение других заболеваний).
Этиология и патогенез
Острый колит
Этиология:
1. Инфекционные колиты:
— дизентерийный;
— брюшнотифозный;
— колибациллярный;
— стафилококковый;
— грибковый;
— протозойный;
— септический;
— туберкулезный;
— сифилитический.
2. Токсический колит:
— уремический;
— сулемовый;
— медикаментозный.
3. Токсико-аллергический колит: алиментарный.
Хронический колит
Представляет собой первично или вторично возникающее хроническое воспаление толстой кишки.
Патологическая анатомия
Биопсия при хроническом колите выявляет изменения, схожие с таковыми при хроническом энтерите. Отличием является тот факт, что при колите более отчетливо выражены воспалительные явления, которые сочетаются с дисрегенераторными изменениями и ведут к атрофии и склерозу слизистой оболочки.
1. Хронический колит без атрофии слизистой оболочки. Слизистая оболочка отечная, тусклая, зернистая, имеет серо-красную или красную окраску, нередко отмечаются множественные кровоизлияния и эрозии. Наблюдаются уплощение и десквамация призматического эпителия, увеличение числа бокаловидных клеток в криптах. Крипты укорочены, имеют расширенный просвет, иногда напоминают кисты (пастозный колит).
Собственная пластинка слизистой оболочки, в которой встречаются кровоизлияния, инфильтрирована лимфоцитами, плазматическими клетками, эозинофилами; клеточный инфильтрат зачастую проникает в ее мышечный слой. Клеточная инфильтрация может быть умеренной очаговой или резко выраженной диффузной с формированием отдельных абсцессов в криптах и очагов изъязвления.
2. Хронический атрофический колит. Характерно уплощение призматического эпителия, уменьшение числа крипт, гиперплазия гладкомышечных элементов. В слизистой оболочке наблюдается преобладание гистиолимфоцитарной инфильтрации и разрастания соединительной ткани. В ряде случаев встречаются эпителизирующиеся и рубцующиеся язвы.
Так называемый «коллагеновый колит» выделяют как одну из форм хронического колита. Характеризуется накоплением вокруг крипт слизистой оболочки коллагена, аморфного белка и иммуноглобулинов. В качестве причин развития коллагенового колита предполагают нарушение синтеза коллагена или аутоиммунизацию.
Эпидемиология
Признак распространенности: Распространено
Соотношение полов(м/ж): 1
Точные данные отсутствуют, но общее мнение специалистов указывает на рост заболеваемости и распространенности неинфекционного колита. Возможно это связано с улучшением качества диагностики, изменением питания, общим увеличением продолжительности жизни, накоплением мутаций.
Гемолитико-уремический синдром как осложнение острой кишечной инфекции у детей
Гемолитико-уремический синдром (ГУС) хорошо известен многим педиатрам и в типичном случае проявляется остро развившейся диареей (гемоколит наблюдается у 75% больных), на фоне которой остро возникает состояние, сопровождающееся.
Гемолитико-уремический синдром (ГУС) хорошо известен многим педиатрам и в типичном случае проявляется остро развившейся диареей (гемоколит наблюдается у 75% больных), на фоне которой остро возникает состояние, сопровождающееся:
Восстановление почечной функции в периоде выздоровления отмечается лишь у 70% больных, и связано это, прежде всего, с глубиной повреждения почечной ткани вследствие разнообразия причинно-значимых, провоцирующих факторов. Так, плохой прогноз имеют атипичные семейные (наследственные) и спорадические случаи ГУС, не ассоциированные с диареей, 25% этих больных погибают в острой фазе заболевания, у 50% прогрессирует отек-набухание головного мозга.
Этиология
Типичный ГУС вызывается шигаподобным токсином Stx1 Shigella disenteria и шигаподобным токсином Stx2 Escherichia coli O157:Н7. Цитопатический эффект шигаподобного токсина обнаружен на вероклетках почек африканских зеленых мартышек. У серотипа E. coli O157 имеются уникальные биохимические свойства — отсутствие ферментации сорбитола. Однако некоторые другие серотипы эшерихий способны вызывать диарею, ассоциированную с ГУС, у детей — О26, О145, О121, О103, О111, О113 и др. Они продуцируют другие токсины, отличные от шигаподобных токсинов своими субъединицами, аминокислотными последовательностями и молекулярным весом.
Классификация тромботических микроангиопатий (представлена Европейской педиатрической группой, 2006 г.).
С учетом этиологии:
Нарушения обмена веществ:
Не полностью установленная этиология:
Установлено, что в основе не ассоциированного с диареей ГУС (non-Stx-HUS) имеет место генетическое нарушение — низкий уровень третьего компонента комплемента в сыворотке и нарушение его регуляции. Выявлены генетические маркеры, которые приводят к атипичному ГУС у больных с наследственной предрасположенностью. В настоящее время обнаружено более 50 мутаций в гене фактора НF1, кодирующих систему активации комплемента. В развитых странах такие больные проходят генетическое тестирование, а также определение уровня аутоантител. Так как атипичный ГУС протекает неблагоприятно с формированием в 50% случаев хронической почечной недостаточности (ХПН) или необратимого повреждения головного мозга, генетическое тестирование важно для решения вопроса о возможности успешной трансплантации почек таким пациентам [2].
Заболеваемость и факторы передачи
В Африке, Азии при бактериологическом исследовании кала от больных ГУС чаще высеваются серотипы шигелл, выделяющие Stx1, после его воздействия у 38–60% детей развивается гемоколит. В США ежегодно регистрируется до 70 тыс. заболевших эшерихиозом и примерно 60 летальных исходов. В Аргентине, Уругвае эшерихиоз эндемичен. Заболеваемость диареей, ассоциированной с ГУС, составляет 10 на 100 тыс. детей в год. Частое возникновение эшерихиоза связывают с традиционным употреблением мясных продуктов из телятины: до 40% молодых животных длительно выделяют в стуле Stx2 E. coli O157:Н7.
В России не ведется анализ заболеваемости диареей, ассоциированной с ГУС, у детей. Публикации скудны, осуществляются в основном реаниматологами. Диарея, ассоциированная с ГУС, этиологически редко расшифровывается. Врачи не диагностируют признаков тяжелого бактериального токсикоза в начальном периоде заболевания. Происходит недооценка степени тяжести состояния больных, соответственно, запоздалая адекватная терапия и неблагоприятные исходы.
Патогенез
Таким образом, в детском возрасте у большинства детей встречается типичный или постдиарейный ГУС, который вторичен по отношению к острым кишечным инфекциям (ОКИ), а центральную роль в патогенезе почечных поражений, гемолиза и тромбоцитопении играет повреждение эндотелиальных клеток. В основе повреждения почек при ГУС лежит гломерулярная тромботическая микроангиопатия — утолщение стенки сосудов с отеком эндотелия и накоплением белков и клеточного детрита в субэндотелиальном слое в результате воздействия одного или нескольких повреждающих факторов. Кроме этого гистопатологические варианты ГУС включают в себя ишемию клубочков, которая в сочетании с тромбозом в последующем может приводить к многоочаговому или диффузному некрозу клубочков (коркового вещества), окклюзии клубочков фибриновыми тромбами.
Нормальный эндотелий обеспечивает эукоагуляционную ситуацию. Это поддерживается продукцией антитромбина III, простациклина, оксида азота, эндотелийзависимого релаксирующего фактора и т. д. При повреждении эндотелия его поверхность приобретает прокоагулянтные свойства, что в свою очередь способствует локальной активации свертывающей системы крови с внутрисосудистой коагуляцией, отложению фибрина в стенках и просвете капилляров. Это приводит к сужению или облитерации просвета капилляров клубочков, снижению скорости клубочковой фильтрации и уменьшению перфузии почечных канальцев с их вторичной дисфункцией или некрозом [5]. При ОКИ, осложненных ГУС, наиболее часто страдают внутриклубочковые сосуды, поражение которых возникает на ранних стадиях заболевания.
Генез тромбоцитопении при ГУС связан с усилением внутрипочечной агрегации тромбоцитов, при этом повышается уровень 3-тромбоглобулина и тромбофактора-4 — специфических тромбоцитарных белков, количество которых в плазме нарастает при активации тромбоцитов и снижении гломерулярной фильтрации [6]. Тромбоцитопении также способствует повышенное их потребление в тромбы. Кроме того, экспериментально показано, что после проведенной двусторонней нефрэктомии уровень тромбоцитов достаточно быстро восстанавливается. Это подтверждает причастность почек к данному лабораторному симптому.
Другим удивительным фактом является значимое снижение продукции эндотелиальными клетками простациклина (PGJ2) у некоторых больных с ГУС и членов их семей. Это предполагает наличие генетического дефекта, который может привести к развитию семейных случаев ГУС, при условии воздействия этиологического фактора на эндотелий сосудов.
Таким образом, при ГУС, обусловленным шигаподобным токсином, изменения наблюдаются непосредственно в клубочках и канальцах почек. Однако нефробиопсия, проведенная через несколько месяцев после заболевания, показывает, что большая часть клубочков сохраняет нормальное строение и только 15–20% склерозированы. Поэтому исходы ОКИ, осложненных ГУС, как правило, благоприятны, если своевременно купируется ОПН.
Основные клинические признаки (ОКИ + ГУС):
Дополнительные симптомы ОКИ + ГУС:
Лечение больных с ГУС проводится исключительно симптоматическое, поддерживающее, поскольку патогенетической терапии с доказанной эффективностью в настоящее время не существует.
Ниже представлены рекомендации по ведению пациентов с ГУС, опубликованные Европейской педиатрической исследовательской группой [3] и в Консенсусе исследовательской группы по печеночно-почечной трансплантации при ГУС.
Лечение:
Нами проводилось изучение клинического профиля, спектра функциональных нарушений, прогностических факторов и исходов у 25 детей с ОКИ, осложненными гемолитико-уремическим синдромом, которые находились на лечении в МУЗ ДГКБ № 3 Новосибирска в период с 1991 по 2010 гг.
Наибольшее количество случаев (16 из 25 больных) ГУС наблюдалось у детей в возрасте до трех лет, что согласуется с данными литературы [1, 3]. В 1,3 раза чаще заболевание развивалось у девочек, такое соотношение встречается не везде, например, в Непале мальчики болеют в 3 раза чаще, чем девочки [4].
В первые трое суток от начала ОКИ ГУС развился у 13 больных, что составило 52% больных, до 5 дней — у 7 (28%) больных, и от 6 до 8 дней — у 5 (20%) детей. Таким образом, острое начало ГУС отмечалось только у половины, а у остальных больных проходило некоторое время от начала диареи, болезнь манифестировала клиникой гастроэнтероколита, поэтому терапия продолжалась на участке и была неадекватной степени тяжести. При этом длительно использовались сорбенты, не назначались антибактериальные препараты, либо использовался фуразолидон без эффекта, и терапия не менялась до появления клинических симптомов ГУС.
Результаты бактериологических исследований кала были положительны лишь у 8 больных. Так, в периоде диареи у двух пациентов в копрокультуре отмечался высев шигелл Флекснера; у одного — Salmonella typhy murium; у двух — E. coli O26; у трех — E. coli O157. Сложность верификации E. coli O157, выделяющей Stx2, обусловлена уникальным свойством ферментации бактерий данного серотипа на средах, содержащих сорбитол.
Развернутая клиническая картина в начале заболевания включала лихорадку, рвоту, абдоминальные боли, одышку, при этом колит отмечался у всех 100% заболевших, а гемоколит — только у пяти больных. Мочевой синдром в виде макрогематурии в острой фазе болезни имел место у двух детей.
Поражение центральной нервной системы (ЦНС) диагностировано у 14 детей (оглушение, сопор, судороги, кома), что было расценено нами как проявление токсикоза, гипергидратации, метаболических изменений (ацидоза), электролитных нарушений — гиперкальциемии, гипокалиемии (гиперкалиемия выявлялась редко), гипонатриемии, нарушение осмолярности плазмы. Гипонатриемия была связана как с потерей этого электролита с кишечником, так и почками. На фоне олигурии экскреция натрия усиливается за счет торможения реабсорбции в канальцах. Начальные признаки поражения ЦНС — повышенная возбудимость, беспокойство, затем прогрессирующая вялость, затем больные впадали в кому. Нарушение сознания проявлялось в основном у детей первых лет жизни.
Анемия — основной симптом ГУС, который во многом предопределяет степень тяжести ГУС, но не коррелирует с глубиной поражения почек. Анемия характеризуется как гиперрегенераторная, поэтому в общем анализе крови много ретикулоцитов за счет активной пролиферации в костном мозге. Бледность кожи — важнейший признак бактериального токсикоза, развивающийся уже в начале болезни, в динамике нарастала за счет гемолиза эритроцитов, падения уровня гемоглобина. В результате гемоглобинурии у некоторых больных отмечался темно-коричневый или черный цвет мочи. Родители указывали на данный симптом участковому педиатру, но ему не уделяли должного внимания. Так, больная Б., 1,5 лет жизни, после появления гемоглобинурии еще на сутки была оставлена дома и поступила с ошибочным диагнозом «вирусный гепатит», когда появилась желтуха на фоне восковидной бледности кожи. Массивный острый гемолиз характеризовался критическими цифрами гемоглобина ( 3 ) выявлялась у всех детей, в трех случаях уровень тромбоцитов снижался до единичных клеток. Количество тромбоцитов в периферической крови, как правило, коррелировало с темпом диуреза, повышение их количества в динамике болезни предшествовало восстановлению диуреза, что является благоприятным лабораторным признаком.
Основные показатели системы гемостаза, за исключением тромбоцитопении, изменялись незначительно. Это свидетельствовало о том, что в патогенезе ГУС отсутствует системное тромбообразование (ДВС-синдром (диссеминированное внутрисосудистое свертывание)), а тромбоз сосудов осуществляется преимущественно на уровне почек. Возможно, у детей и есть период диссеминированного свертывания крови, но факторы, потребляемые в этот период заболевания, быстро восстанавливаются до нормы. Рекомендуется поддерживать нормальный уровень фибриногена, факторов свертывания введением свежезамороженной плазмы, где они содержатся в большом количестве. Так, у наших больных время свертывания, АЧТВ (активированное частичное тромбопластиновое время), уровень фибриногена, количество РФМК (растворимых фибрин-мономерных комплексов), как правило, соответствовало контрольным значениям.
Однако кровотечения отмечались у двух больных. В 1997 г. мы наблюдали случай ГУС у ребенка Р. 3 лет с шигеллезом Флекснера и язвенно-некротическим поражением толстого кишечника. В данном случае отмечался тяжелый гемоколит с периодическими кишечными кровотечениями в течение 12 дней. Предпринимались попытки коррекции гемостаза путем введения большого количества свежезамороженной плазмы, но у больного развился парез кишечника, который определил наступление летального исхода. В 2003 г. у больной К. 6 лет наблюдалось массивное кровотечение из толстого кишечника, использование препарата NovoSeven — рекомбинантного фактора свертывания крови VIIa позволило остановить кровотечение, в последующем наступило выздоровление. Тромбомасса вводилась некоторым больным с критическими цифрами, но только при кровотечениях, поскольку срок жизни тромбоцитов ограничен.
Значения сывороточного уровня мочевины и креатинина в остром периоде болезни значительно превышали контрольные возрастные показатели (в среднем в 1,5–2 раза и более). Тяжесть ГУС обусловливает глубина поражения почек, соответственно, состояние больного и исход зависят от снижения почечных функций. Как известно, длительность анурии предопределяет прогноз — чем дольше она продолжается, тем вероятность восстановления почечной функции меньше и чаще наблюдается переход в ХПН [3]. При сохранении водовыделительной функции почек (так называемая неолигурическая ОПН), даже при высоких цифрах мочевины, прогноз, как правило, благоприятен. Для олигоанурической стадии ГУС не характерны отеки в связи с потерями жидкости со стулом и перспирацией. Протеинурия встречалась у 38% и микрогематурия — у 70% больных.
Варианты заместительной почечной терапии
Плазмообмен — первый уровень терапии, он выполнялся всем 25 больным в объеме 1,5–2 объема циркулирующей плазмы. Это коррекция плазменных факторов, осуществлялась в остром периоде ежедневно, в дальнейшем по необходимости. Острый период ГУС у всех детей протекал по-разному — обычно в течение 2–5 дней наблюдались токсикоз, тромбоцитопенические сыпи, тромбозы катетеров. Если за это время не восстанавливался диурез, больному устанавливали перитонеальный катетер и проводили перитонеальный диализ от 2 до 6 недель.
Перитонеальный диализ выполнялся шести больным (четырем в сочетании с гемодиализом и двум — с гемодиафильтрацией). Есть больные без тяжелого токсикоза и выраженных электролитных нарушений, которым можно проводить только перитонеальный диализ, и они поправляются. Перитонеальный диализ — щадящая заместительная терапия, при которой медленно происходит обмен жидкости через брюшину, он может использоваться длительно, до восстановления функции почек.
С 1991 по 2003 г. плазмообмен в сочетании с гемодиализом был выполнен 14 (56%) больным. С 2008 г. для стабилизации гомеостаза в стационаре осуществляется гемодиафильтрация в сочетании с перитонеальным диализом (использовалась в лечении трем больным). Принцип гемодиафильтрации — замена интерстициальной жидкости на специальные растворы, которые полностью, кроме белков, соответствуют составу плазмы. При гемодиафильтрации плазмообмен осуществляется аппаратным способом, это многочасовая процедура, иногда она длится сутки, при этом диализирующая жидкость вводится со скоростью 70 мл/мин. Этот метод терапии более эффективен при SIRS-синдроме. Гемодиализ показан больным с нарушением азото- и водовыделительных функций почек без симптомов воспаления, снижает уровень азотемии, нормализует гомеостаз за 3–4 часа, поток диализирующего раствора по фильтру составляет 500 мл/мин.
В нашем наблюдении олиго/анурия у трех больных отсутствовала, а в остром периоде болезни доминировали симптомы гемолиза, у трех пациентов олиго/анурия сохранялась до трех суток, у 8 детей — до 8 суток, у шести человек до 15 суток и у двух — до 20 и более. Так, у пациента с длительностью олигурической стадии ОПН 28 дней, которому проводилась почечная заместительная терапия, полностью восстановились функции почек. У другой больной, после 42 дней заместительной почечной терапии, развилась ХПН.
Литература
Е. И. Краснова, доктор медицинских наук, профессор
С. А. Лоскутова, доктор медицинских наук, доцент
О. В. Гайнц
НГМУ, МУЗ ДГКБ № 3, Новосибирск