Гемофильная инфекция чем лечить
Гемофильная инфекция чем лечить
Гемофильная инфекция – группа острых инфекционных болезней, вызванных гемофильной палочкой.
Повышение заболеваемости отмечается в конце зимы и весной.
Гемофильная инфекция характеризуется поражением:
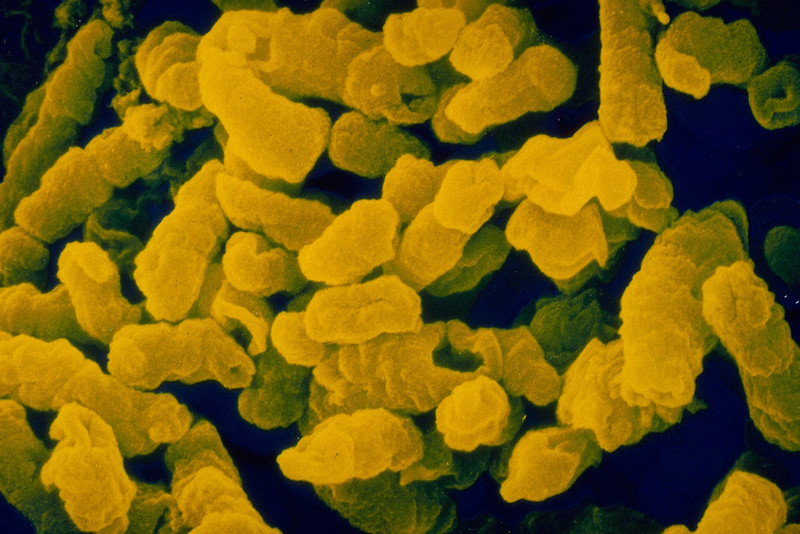
Возбудитель инфекции – Haemophilus influenzaе (палочка Пфайффера).
Возбудитель инфекции локализуется на слизистой оболочке верхних дыхательных путей.
В связи с высокой устойчивостью возбудителя гемофильная инфекция плохо поддается антибиотикотерапии.
Здоровое носительство может продолжаться от нескольких дней до нескольких месяцев. Носительство может сохраняться даже при назначении антибактериальных препаратов. Возбудитель начинает поражать организм в момент его ослабленного состояния.
Источник и резервуар инфекции – только человек.
Путь распространения инфекции – воздушно-капельный (от зараженного человека здоровому), также передача инфекции возможна при контакте с инфицированным материалом, как от бессимптомных носителей, так и от больных.
Кто наиболее подвержен заражению данной инфекцией?
Группы риска:
Поражает гемофильная инфекция любые органы. Первым делом она поражает дыхательную систему.
Заболевания органов дыхания:
Заболевания, развивающиеся в следствие поражения других органов:
Заражение гемофильной инфекцией беременной женщины приводит к развитию патологи плода или к его смерти.
В детском возрасте гемофильная инфекция протекает часто с поражением верхних дыхательных путей, нервной системы, во взрослом чаще встречается пневмония, вызванная гемофильной палочкой.
Некоторые симптомы гемофильной инфекции:
Симптомы при поражении нервной системы – гемофильная инфекция в виде менингита.
По данным Всемирной организации здравоохранения (ВОЗ), менингит составляет около 50% среди всех случаев инвазивных форм гемофильной инфекции типа b.
слабость, повышение температуры тела, боль в горле, насморк
многократная рвота, спутанность сознания, бред, судороги, бессознательное состояние, сыпь, положение тела характерно для менингита (голова запрокинута назад, ноги приведены к животу)
Пневмония, вызванная гемофильной палочкой:
Артрит, вызванный гемофильной палочкой:
Набухание суставов, покраснение, болезненные движения.
Осложнения после перенесенной гемофильной инфекции.
Осложнения менингита, вызванного гемофильной палочкой:
Осложнения после гемофильной пневмонии:
Гемофильный сепсис приводит к летальному исходу.
Гнойные артриты часто сопровождаются остеомиелитом.
Осложнением эпиглоттита является обструкция дыхательных путей, вызывающая в 5-10% летальный исход.
Профилактика гемофильной инфекции.
Единственным надежным средством профилактики группы заболеваний, вызванных гемофильной инфекцией типа b, является вакцинация.
Вакцинация против гемофильной инфекции проводится в соответствии с Приказом Министерства здравоохранения РФ от 21 марта 2014 г. № 125н «Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям» детям, относящимся к группам риска, а также на основании Методических рекомендаций МР 3.3.1.0001-10 «Эпидемиология и вакцинопрофилактика инфекции, вызываемой Haemophilus influenzaе типа b», утвержденных Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека 31.03.2010 г.
Первая вакцинация детей групп риска проводится в возрасте 3 месяцев, вторая в 4,5 месяцев, третья – 6 месяцев. Ревакцинация проводится детям в возрасте 18 месяцев.
Haemophilus influenzae
Автор: Трубачева Е.С., врач – клинический фармаколог
Сегодняшняя тема касается очередного представителя нормальной микрофлоры, который в определенных условиях способен вызывать тяжелейшие заболевания, как в детском, так и во взрослом возрасте. Речь пойдет о Haemophilus influenzae, проще говоря, о гемофиле.
Начнем традиционно с микробиологических аспектов
Откуда взялось название микроорганизма? Дело в том, что этим маленьким бактериям необходимы факторы, присутствующие в крови (факторы X — гемин и V — никотинамид-аденин-динуклеотид) для роста на шоколадном агаре, поэтому они называются гемоглобинофильными бактериями или гемофилами.
H.influenzae является грамм-отрицательной коккоподобной бактерией, колонизирующей верхние дыхательные пути. Выделяют шесть типов гемофил, обозначаемых буквами от a до f, которые различаются по наличию или отсутствию наружной капсулы. У H.influenzae типа b (Hib) капсула имеется и представляет собой полимерную структуру, состоящую из рибозы и рибитола, скрепленных фосфорной кислотой. Эта капсула является основным фактором патогенности, так как благодаря ей микроорганизм способен эффективно обороняться от фагоцитоза и активации системы комплемента, тем самым обеспечивая свою выживаемость. Поэтому H.influenzae типа b являются самыми инвазивными из всех типов гемофил.
H.influenzae способны к образованию биопленок, которые способствуют выживанию целых колоний, а не только отдельных микроорганизмов, так как еще активнее противодействуют факторам иммунитета. О том, что такое биопленки, мы рассказывали здесь.
При всем вышеописанном гемофилы, в том числе и типа b, являются компонентами нормальной микрофлоры носоглотки. После рождения носоглотка колонизируется бескапсульными H.influenzae, и далеко не всегда эта колонизация ведет к развитию заболеваний. Затем при встрече с носителем Hib подселяются еще и они. Дальнейшее развитие событий будет зависеть от состояния слизистой носоглотки.
Эпидемиологические аспекты
H.influenzae крайне нестойки во внешней среде, любой дезинфектант убивает их мгновенно, поэтому источником заболеваний является только человек — больной или носитель, а механизм передачи исключительно воздушно-капельный, так как возбудители в больших количествах концентрируются в секретах верхних дыхательных путей. И если больных не изолировать (или как минимум не надеть на них маску), то довольно быстро перезаражаются все вокруг.
Особенно много возбудителей скапливается в слюне и слизистом отделяемом больных детей, что указывает на острую их заразность (ничего не напоминает?). А учитывая моду последних лет приводить больных детей (ну подумаешь, сопли и кашляет) в организованные коллективы и отсутствие обязательной Hib-вакцинации, можно получить массовую вспышку в детском саду. Литературные источники говорят о том, что в России до 40% менингитов у детей в возрасте до 5 лет вызваны Hib при летальности в районе 5–10% и тяжелых осложнениях в пределах 40%. При этом носительство H.influenzae типа b среди детей разного возраста для России составляет 35–78%. Помимо этого на первом году жизни могут выделяться нетипируемые штаммы гемофил, способствующие высокому риску развития острого среднего отита. И так как, по понятным причинам, мы не можем рекомендовать расформирование детсадовских групп для уменьшения частоты носительства гемофил, то остается только один выход – вакцинация, которая у нас до сих пор необязательна, а при наличии Hib-компонента в вакцинах, он порой вводится только под нажимом родителей, так как медсестра о его наличии в коробочке может просто не догадываться (этот вопрос очень ярко обсудил в своем блоге врач – педиатр Сергей Бутрий, и не смотря на то, что пост написан для родителей, врачам тоже не мешает помнить, что их назначения могут быть прочитаны, мягко говоря, неоднозначно). И не пора ли энергию, затрачиваемую на борьбу с золотистым стафилококком в носах и кале детей, переключить на выявление и санацию гемофил типа b в этом же возрасте? И дело полезное будет сделано, и от неповинного стафилококка отстанем.
Отдельно стоит отметить, что в странах с преобладающим чернокожим населением (мы уже даже представить не можем, где нас еще могут читать) предрасположенность к носительству и развитию заболеваний, вызванных H.influenzae, а также к смертности детей от гемофильного менингита, еще выше ввиду вероятной генетической предрасположенности.
Клинические аспекты
Все заболевания, вызванные H.influenzae, можно разделить на инвазивные и неинвазивные. Инвазивные заболевания вызываются капсульными H.influenzae типа b, и к ним относятся пневмонии, менингиты, сепсисы, артриты, эпиглотиты и целлюлиты. Важно запомнить, что сдерживающим фактором для капсульных H.influenzae является наличие слизи на поверхности дыхательных путей, и как только она, по каким либо причинам, исчезает, гемофилы тут же закрепляются на эпителии, а так как они не подвергаются процессу фагоцитоза из-за наличия капсулы, то довольно быстро проникают под эпителий, минуют лимфоидный барьер и попадают в кровь, вызывая вышеперечисленные заболевания.
Неинвазивные заболевания, вызванные H.influenzae, возникают как следствие распространения по слизистым оболочкам дыхательных путей нетипируемых бескапсульных гемофил и являются осложнениями ОРВИ, которые смогли понизить местный иммунный ответ. Внимание педиатрам – не стафилококк, с которым некоторые отчаянно воюют, а гемофила вызывает вторичные бактериальные осложнения, если они вдруг возникают.
Когда мы должны подумать о H.influenzae?
Наиболее предрасположены к развитию гемофильных инфекций:
— то есть это будут больные, у которых изначально имеются состояния, способствующие ослаблению иммунной системы, в том числе локальных ее ответов (н-р, нарушение мукоциллиарного клиренса у курильщиков), ведущих к раскрытию входных ворот для гемофил.
После перенесенной гемофильной инфекции, вызванной Hib, формируется очень стойкий иммунитет с высоким содержанием антител. При этом дети до двух месяцев редко болеют, так как в этот момент имеют материнские антитела.
Гемофильные менингиты в возрасте до 5 лет в 90% случаев вызваны H.influenzae типа b, при этом 60% случаев приходится на возраст до 2 лет, и протекают в виде сепсиса с поражением не только мозговых оболочек, но и суставов, среднего уха, легких и т. д.
Вторым крайне грозным детским гемофильным заболеванием, которое в течение нескольких часов может привести к летальному исходу, является острый эпиглотит, он же «круп», способный вызвать полную обструкцию дыхательных путей. Причиной оного так же является H.influenzae типа b.
Острый средний отит, как у детей, так и у взрослых, в большинстве случаев также вызывается H.influenzae — в основном, нетипируемыми штаммами.
У часто болеющих острыми респираторными заболеваниями детей причиной вторичных бактериальных осложнений чаще всего выступает бескапсульная H.influenzae.
Кроме того, не стоит забывать и о внутрибольничном инфицировании и развитии гемофильных вентилятор-ассоциированных пневмоний у пациентов, имеющих свои колонии в носоглотке, либо заражение путем немытых рук и носов сотрудников реанимационной бригады. В этом случае разовьется ранняя (в пределах 2 – 4 суток) вентилятор-ассоциированная пневмония.
Диагностические аспекты
Микробиологическая диагностика играет основную роль в терапии заболеваний, вызванных H.influenzae. Какими методами и средствами мы можем воспользоваться?
Чем лечить?
Главную роль в лечении играют возраст пациента и локализация процесса. Кроме того, необходимо помнить о том, что гемофилы, как и пневмококки, умеют вырабатывать пенициллиназы, чем почти полностью исключают из использования незащищенные формы природных и синтетических пенициллинов, если пациент использовал оные в течение ближайшего полугодия.
Неопасные для жизни инфекции у взрослых, такие как острый средний отит, обострение хронического бронхита или синусит можно лечить по следующим схемам:
Длительность лечения составляет:
Менингиты у взрослых (только антибактериальная терапия)
Менингиты у детей (схемы для недоношенных смотрим в соответствующей литературе, либо в инструкции к использованию упомянутых препаратов)
Тяжелые жизнеугрожающие инфекции у взрослых, такие как пневмония, тяжелый целлюлит, септический артрит:
В заключение нашего разговора хотелось бы еще раз отметить, что основой профилактики тяжелых и жизнеугрожающих гемофильных инфекций первых лет жизни является использование H.influenzae тип b — вакцин и введение оных в национальный календарь прививок, а пока этого нет — проведение разъяснительной работы с родителями (вместо запугивания страшным золотистым стафилококком).
Диагностика и лечение гемофилии
Общая информация
Краткое описание
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ по ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ГЕМОФИЛИИ
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Таблица 1. Классификация гемофилии по степени тяжести
Около 60-70% всех диагностированных случаев гемофилии составляют тяжелые формы заболевания, для которых характерны спонтанные геморрагические эпизоды (преимущественно гемартрозы и гематомы мягких тканей различных локализаций). Степень тяжести нарушений свертывания крови и клинических проявлений при гемофилии зависит, как правило, от уровня активности фактора в крови, однако в клинической практике не всегда существует прямая корреляция между лабораторным и клиническим фенотипами заболевания [2, 3].
Клиническая картина
Cимптомы, течение
Таблица 2. Клинические проявления гемофилии
Диагностика
При сборе анамнеза заболевания и семейного анамнеза пациента рекомендуется выяснять наличие проявлений геморрагического синдрома: жалоб на легко появляющиеся экхимозы и гематомы в раннем детстве; возникновение спонтанных кровотечений (особенно в суставы, мышцы и мягкие ткани); длительных кровотечений после травм или хирургического вмешательства [3].
Данные семейного анамнеза примерно у 2/3 больных содержат указания на геморрагические проявления у близких родственников по материнской линии (у мужчин, реже у женщин). Данные персонального анамнеза могут содержать информацию о геморрагических проявлениях у пациента. При сборе анамнеза заболевания необходимо обращать внимание на наличие геморрагических проявлений в неонатальном периоде в виде кефалогематом, внутричерепных кровоизлияний, кровоточивости и длительном заживлении пупочной ранки; у грудных детей – экхимозов, не связанных со значимой травмой, гематом мягких тканей после незначительных ушибов или спонтанных. У некоторых детей кровотечения могут отсутствовать на первом году жизни до тех пор, пока ребенок не начнет ходить [2]. Важно обращать внимание на несоответствие выраженности геморрагических проявлений тяжести предшествовавшей травмы, на рецидивы кровотечений после первичной остановки, не связанные с повторной травмой, массивные и (или) множественные гематомы, системность геморрагических проявлений (проявления различной локализации), «спонтанные геморрагические проявления». При легкой форме гемофилии кровотечения могут отсутствовать до первой травмы или хирургического вмешательства. Сбор жалоб и анамнеза позволит определить объем обследования пациента.
При проведении физикального осмотра рекомендуется обращать внимание на наличие кожного геморрагического синдрома различной выраженности в виде множественных экхимозов и гематом, возможных при тяжѐлой и среднетяжелой форме гемофилии [4]. Высоковероятно выявление признаков поражения суставов в виде деформации, отека и локального повышения температуры кожи (острый гемартроз) и/или признаков нарушения подвижности, объема движений суставов, гипотрофии мышц конечности на стороне поражѐнного сустава, нарушение походки (деформирующая артропатия).
Диагноз устанавливается при наличии как минимум двух из трех критериев.
Инструментальная диагностика позволяется визуализировать кровотечения/кровоизлияния различных локализаций, а также выявить осложнения, развившиеся вследствие геморрагических проявлений. По показаниям проводятся следующие обследования:
эзофагогастродуоденоскопия;
Лечение
Рекомендуется отдавать предпочтение тому препарату, который при равной эффективности лучше всего переносится пациентом, имеет лучшие фармакокинетические индивидуальные показатели и наиболее удобен в использовании, исходя из конкретных условий [4, 7, 9]. Смена МНН у конкретного пациента при отсутствии зарегистрированных нежелательных явлений на введение используемого препарата и удовлетворительном клиническом ответе на терапию возможна после 100 экспозиционных дней введения концентратов факторов свертывания крови.
Существует два вида специфической терапии – лечение по факту возникновения кровотечений (по требованию) и профилактическая терапия [4].
Таблица 3. Рекомендуемые уровни фактора и продолжительность терапии при различных видах кровотечений 
Расчет дозы концентрата FVIII у пациентов старше 1 года проводится следующим образом: доза (МЕ) = масса тела (кг) х (требуемая активность – базальная активность) х 0,5.
Учитывая вариабельность фармакокинетических показателей у каждого конкретного пациента заместительная терапия требует клинического и, при необходимости, лабораторного контроля. Клинический контроль должен проводиться гематологом при обращении пациента, родителями и самим пациентом постоянно. В основе клинического контроля лежит оценка динамики геморрагических проявлений и ее сопоставление с проводимой заместительной терапией. Лабораторный контроль включает определение активности дефицитного фактора в крови, тест восстановления, оценку фармакокинетической кривой (с расчетом периода полувыведения). Для оценки результативности гемостатической терапии возможно проведение интегральных тестов: тромбоэластография, тест генерации тромбина, тромбодинамика в динамическом наблюдении [8].
Таблица 4. Виды профилактики при гемофилии
** Переход к следующему шагу при развитии спонтанного гемартроза.
При клиническом контроле решение о недостаточной эффективности профилактической терапии принимается в следующих случаях: более двух эпизодов спонтанных гемартрозов в год, появление признаков хронического синовиита или артропатии, возникновение спонтанных геморрагических проявлений другой локализации. Лабораторный контроль заключается в определении остаточной активности фактора перед следующим введением (должна быть не ниже 1%), контроле наличия ингибитора, и, по возможности, в проведении фармакокинетического исследования [12].
При наличии клинических или лабораторных данных о неэффективности профилактической терапии принимается решение о повышении дозы или кратности введения препарата. Учитывая, что основная задача профилактической заместительной терапии – сохранение качества жизни пациента, у пациентов с высоким уровнем физической активности допустимо повышение стандартных доз или увеличение кратности введения препарата.
Особенности проведения гемостатической терапии в зависимости от локализации кровотечения
Реабилитационные мероприятия и ЛФК целесообразно начинать после прекращения болевого синдрома с учетом состояния места повреждения. Если пациент не получает постоянное профилактическое лечение, после купирования кровотечения показана кратковременная профилактика, особенно на время реабилитации [4, 6, 9].
После кровоизлияния в ЦНС рекомендована обязательная профилактическая терапия в течение 3—6 месяцев.
Помимо заместительной терапии, рекомендовано соблюдение постельного режима и проведение гидратации (3 л/м2) в первые 48 часов. Не рекомендуется применение ингибиторов фибринолиза. Дополнительное возможно назначение преднизолона. Пациентам, у которых развилось почечное кровотечение, необходимы консультация уролога и урологическое обследование. [3, 4, 8, 14]
При тяжелой форме гемофилии появление ингибитора не влияет на количество и локализацию кровотечений. Но поскольку при появлении ингибиторов заместительная терапия факторами становится неэффективной, риск тяжелых осложнений и даже смерти от кровотечения у этих больных выше.
При ингибиторной ГВ до 50% пациентов могут иметь тяжелые аллергические реакции, в том числе анафилаксию, при применении FIX. Такие реакции часто бывают первым симптомом развития ингибитора [15].
Подтверждение наличия ингибитора и определение его титра выполняется в коагулологической лаборатории. У детей оценка наличия ингибитора должна проводиться каждые 5 дней первые 20 ДВ, каждые 10 дней с 21 до 50-й ДВ, а затем не менее 2 раз в год до 100 ДВ. У пациентов с более чем 100 ДВ препарата оценка наличия ингибитора должна проводиться 1 раз в год и дополнительно в следующих ситуациях: снижение эффективности заместительной терапии факторами при введении адекватных доз, появление или увеличение количества кровотечений на профилактической терапии, отсутствие достаточного повышения уровня фактора в крови после введения препарата. Кроме того, диагностика ингибитора также должна проводиться в следующих ситуациях:
— при смене препарата (через 10-20 ДВ и через 6 месяцев терапии);
— перед хирургическими вмешательствами и после операции при отсутствии адекватного повышения уровня фактора в крови после введения препарата;
— через 4 недели после окончания проведения интенсивной терапии.
Существуют различные протоколы проведения ИИТ (табл.6). Оптимального режима проведения ИИТ нет. Для пациентов с высокореагирующим ингибитором, независимо от титра ингибитора на момент начала ИИТ, рекомендована начальная схема 100 – 150 МЕ/кг FVIII каждые 12 часов. Для пациентов с низкореагирующим ингибитором рекомендовано начинать ИИТ по схеме 50 – 100 МЕ/кг FVIII ежедневно или каждый второй день.
Таблица 6. Протоколы проведения ИИТ
Таблица 7. Критерии эффективности ИИТ
Опыт проведения ИИТ у пациентов с ингибиторной ГB ограничен. Это обусловлено очень низкой эффективностью и наличием аллергических реакций.
У большинства пациентов с гемофилией вследствие рецидивирующих гемартрозов формируются различные повреждения опорно-двигательного аппарата.
Диагностика включает выявление клинических признаков, УЗИ и/или МРТ суставов. Терапия проводится совместно с ортопедами, имеющими опыт лечения больных гемофилией. При сохранении признаков воспаления показана терапия нестероидными противовоспалительными препаратами (ингибиторами COX-2).
При недостаточной эффективности заместительной терапии возможно проведение курса пункций сустава с введением стероидных противовоспалительных препаратов (на первом этапе); далее вариантами выбора являются химическая или эндоскопическая синовэктомия, а при их недостаточной эффективности – хирургическая коррекция.
Основой профилактики развития хронической артропатии является адекватная постоянная профилактическая заместительная терапия. Своевременное лечение синовиита также необходимо для предотвращения развития артропатии. Диагностика артропатии основана на выявлении клинических признаков и на результатах инструментальных исследований: УЗИ, КТ, МРТ [8].
Целью лечения уже развившейся хронической артропатии является улучшение функционирования сустава и уменьшение болевого синдрома. Для борьбы с болевым синдромом оптимально использовать ингибиторы COX-2. Для восстановления функции сустава, состояния мышц проводят курсы ЛФК и физиотерапии. В ряде случаев эффективно использование тренажеров. На начальных этапах восстановительного лечения показано проведение курсов препаратов гиалуроновой кислоты. При недостаточной эффективности консервативной терапии показано хирургическое лечение, которое должно проводиться врачами, имеющими опыт лечения пациентов с гемофилией.