Гемофагоцитарный синдром что это
Гемофагоцитарный синдром что это
Первое сообщение о гемофагоцитарном синдроме, ассоциированном с инфекцией, относится к 1979 г. В этом году R. J. Risdall сообщил о 19 пациентах, у которых развился сходный симптомокомплекс, состоящий из лихорадки, гепатоспленомегалии и панцитопении на фоне вирусной инфекции.
Из 19 больных 14 получали иммуносупрессивную терапию после трансплантации почки, у пяти заболевание развилось вне связи с предшествовавшим иммунодефицитным состоянием.
У 13 больных удалось установить роль в развитии болезни вирусов из семейства герпес-вирусов и аденовирусов. Этот клинико-морфологический синдром был обозначен как «вирусассоциированный гемофагоцитарный синдром».
В дальнейшем термин «вирусассоциированный гемофагоцитарный синдром» получил широкое распространение, но по мере накопления клинических наблюдений стало ясно, что бактериальные, грибковые и паразитарные инфекции также могут запускать патологическую лимфогистиоцитарную реакцию, поэтому в современной литературе широко используется термин «гемофагоцитарный синдром, ассоциированный с инфекцией» (ИАГС).
Микроорганизмы, ассоциированные с гемофагоцитарным синдромом
| Вирусы | Бактерии | Грибы | Простейшие |
| Вирус Эпштейна—Барр Цитомегаловирус Герпес простой Герпес зостер Герпес типа 6 Герпес типа 8 ВИЧ Аденовирусы Вирусы гепатита: А В С Парвовирус В19 Краснуха (у взрослых) Грипп А Парагрипп тип III Денге | Brucella melitensis Chromobacterium violaceum Chlamydia psittaci Coxiella burnetti (лихорадка Q) Ehrlichia Mycoplasma pneumonia Salmonella typhii Rickettsia Mycobacterium avium/intracellulare Mycobacterium tuberculosis Borrelia burgdorferi (болезнь Лайма) Leptospira Spirocheta pallidum (врожденный сифилис) | Aspergillus С. albicans Criptococcus Histoplasma capsulatum Penicillium marneffei P. carinii Trychophyton beigelii | Leishmania Babesia P. falciparum Toxoplasma gondii |
Эпидемиология гемофагоцитарного синдрома ассоциированного с инфекцией
С известной степенью уверенности можно утверждать, что вторичный гемофагоцитарный синдром достаточно редко осложняет течение инфекций. Данные мировой литературы позволяют предполагать более высокую частоту гемофагоцитарного синдрома ассоциированного с инфекцией в азиатской популяции, чем среди выходцев из Европы: более 50 % случаев приходится на Японию, Китай и Тайвань.
Распределение больных по полу и возрасту равномерно, а представление о более высокой частоте гемофагоцитарного синдрома ассоциированного с инфекцией в педиатрической популяции связано с невозможностью в ряде случаев доказать наследственную природу лимфогистиоцитоза.
Спектр возбудителей, ассоциированных с развитием гемофагоцитарных синдромов, весьма широк и включает представителей основных классов патогенных микроорганизмов: вирусов, бактерий, грибов и простейших. При большинстве инфекций гемофагоцитарный синдром — исключительно редкое осложнение, наиболее частыми «виновниками» оказываются представители семейства герпес-вирусов, особенно вирус Эпштейна—Барр; не является казуистикой гемофагоцитарного синдрома ассоциированного с инфекцией при висцеральном лейшманиозе, милиарном туберкулезе, бруцеллезе.
Иммунный статус пациентов гемофагоцитарным синдромом ассоциированным с инфекцией. Гемофагоцитарный синдром тесно связан с дефектами клеточного иммунитета, в первую очередь с нарушениями механизмов клеточной цитотоксичности.
Иммунодефицит может быть следствием ятрогенной иммуносупрессии (реципиенты солидных органов, ГСК, больные с аутоиммунными заболеваниями), ВИЧ-инфекции, а в педиатрической популяции — наследственных дефектов иммунной системы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гемофагоцитарный лимфогистиоцитоз у детей. Клинические рекомендации.
Гемофагоцитарный лимфогистиоцитоз у детей
Оглавление
Ключевые слова
Трансплантация гемопоэтических стволовых клеток
Всего 10-15 ключевых слов
Список сокращений
ГЛГ – гемофагоцитарный лимфогистиоцитоз
ВГЛГ – вторичный гемофагоцитарный лимфогистиоцитоз
ТГСК – трансплантация гемопоэтических стволовых клеток
НК – натуральные киллеры
АЛТ- аланиновая аминотрансфераза
АСТ – аспарагиновая аминотрансфераза
КТ – компьютерная томография
МРТ – магнитно-резонансная томография
УЗИ – ультразвуковое исследование
ВИЧ – вирус иммунодефицита человека
ПЦР – полимеразная цепная реакция
ЭБВ – вирус Эпштейн-Барр
Термины и определения
Гемофагоцитарный лимфогистиоцитоз – врожденное или приобретенное заболевание, проявляющееся лихорадкой, спленомегалией, панцитопенией, коагулопатией и неврологическим дефицитом вследствие системного воспалительного ответа и повреждения органов активированными макрофагами и цитотоксическими Т лимфоцитами.
Гемофагоцитоз – феномен фагоцитоза форменных элементов крови макрофагами, выявляемый при цитоморфологическом или гистологическом исследовании образцов тканей или биологических жидкостей
Первичный гемофагоцитарный лимфогистиоцитоз (ПГЛГ) – форма ГЛГ, обусловленная наследуемым генетическим дефектом механизмов клеточной цитотоксичности и иных механизмов негативной регуляции иммунного ответа
Вторичный гемофагоцитарный лимфогистиоцитоз (ВГЛГ) – форма ГЛГ, обусловленная нарушением регуляции иммунного ответа в контексте верифицированного онкологического, аутоиммунного или инфекцинонного процесса, и не имеющая в основе наследуемого генетического дефекта
1. Краткая информация
1.1 Определение
Гемофагоцитарный лимфогистиоцитоз – заболевание, обусловленное дефицитом негативной регуляции иммунного ответа, сопровождающееся неконтролируемой активацией цитотоксических Т-лимфоцитов и макрофагов, аккумуляцией их в пораженных органах и развитием системного воспалительного ответа.
1.2 Этиология и патогенез
Вторичный гемофагоцитарный синдром развивается вследствие нарушения регуляции иммунного ответа, развивающегося в контексте аутоиммунных, онкологических и инфекционных заболеваний. Независимо от пусковых механизмов, общим патологическим механизмом первичного и вторичного гемофагоцитарного синдрома является гиперпродукция провоспалительных цитокинов, активация моноцитов/макрофагов и мультиорганное воспалительное повреждение [1]
1.3 Эпидемиология
Данные о заболеваемости и распространенности ПГЛГ в России ограничены, экстраполяция международных данных дает заболеваемость 1 на 106 детского населения в год. Достоверных оценок заболеваемости и распространенности ВГЛГ нет.
1.4 Кодирование по МКБ-10
D76.1 – гемофагоцитарный лимфогистиоцитоз
D76.2 – гемофагоцитарный синдром, связанный с инфекцией
D76.3 – другие гистиоцитозные синдромы
1.5 Классификация
Гемофагоцитарный лимфогистиоцитоз отнесен к группе “H” в современной классификации гистиоцитозов. Выделяют первичные формы гемофагоцитарного лимфогистиоцитоза, обусловленные известным генетическим дефектом, и вторичные, не связанные с наследуемым генетическим дефектом. Полная классификация гемофагоцитарного лимфогистиоцитоза в соответствии с приведена ниже [2].
Первичный гемофагоцитарный лимфогистиоцитоз: наследственные заболевания, ведущие к развитию ГЛГ
ГЛГ, ассоциированный с дефектами цитотоксичности лимфоцитов
Синдром Грисселли типа (RAB27A)
Синдром Чедиак-Хигаши (LYST)
ГЛГ, ассоциированный с аномалиями активации инфламмасомы
ГЛГ, ассоциированный с наследственными болезнями, влияющими на воспаление
Лизинурия/интолерантность к белку (SLC7A7)
Семейные формы ГЛГ с неустановленным генетическим дефектом
Вторичный гемофагоцитарный лоимфогистиоцитоз
Ассоциированный с инфекцией
ГЛГ, ассоциированный с бактериальной инфекцией
ГЛГ, ассоциированный с грибковой инфекцией
ГЛГ, ассоциированный с паразитарной инфекцией
Ассоциированный со злокачественными новообразованиями
ГЛГ, ассоциированный с химиотерапией (не связанный с первичной презентацией опухоли)
Ассоциированный с ревматологическими заболеваниями
ГЛГ, ассоциированный с трансплантацией
ГЛГ, ассоциированный с иатрогенной активацией иммунной системы
ГЛГ, ассоциированный с иатрогенной иммуносупрессией
2. Диагностика
2.1 Жалобы и анамнез
Увеличение объёма живота
Ребенок раннего возраста
Беременность и роды без патологии
Смерть сиблингов со сходной клинической презентацией
Указания на Х-сцепленную патологию в семейном анамнезе
2.2 Физикальное обследование
Геморрагии на слизистых
2.3 Лабораторная диагностика
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано выполнение:
Автоматического анализа крови с лейкоцитарной формулой
Биохимического анализа крови
Исследования спинномозговой жидкости
Иммунофенотипирование лимфоцитов периферической крови
Определение экспрессии белков перфорин, SAP и XIAP в НК-клетках и Т-лимфоцитах
Исследования концентрации иммуноглобулинов сыворотки
Детекции вирусных геномов методом ПЦР в крови (цитомегаловирус, вирус Эпштейн-Барр, ВИЧ, герпес симплекс 1 и 2 типа, парвовирус В19)
Исследования концентрации растворимого sCD25;
Тканевого типирования пациента и потенциальных доноров
Микробиологического исследования крови (гемокультура)
Микробиологического исследования ликвора
Молекулярно-генетического исследования – прямое секвенирование генов PRF1, UNC13D, STX11, STXBP, SH2D1A, RAB27
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
2.4 Инструментальная диагностика
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано проведение:
2.4.1 МРТ головного мозга Т1, Т2, FLAIR, c контрастированием гадолинием
2.4.2 УЗИ брюшной полости
2.4.3 Рентгенографии грудной клетки
2.4.4 КТ легких
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
2.5 Иная диагностика
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано проведение:
2.5.1 Биопсии лимфатического узла с морфологическим и иммуногистохимическим исследованием
2.5.2 Биопсии кожи с морфологическим и иммуногистохимическим исследованием
2.5.3 Биопсии печени с морфологическим и иммуногистохимическим исследованием
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: Диагностика ГЛГ включает два этапа: 1) установление диагноза ГЛГ и 2) верификация природы ГЛГ (первичный или вторичный).
На первом этапе диагноз ГЛГ устанавливается на основании набора диагностических критериев:
лихорадка > 38оС > 7 дней
спленомегалия > 3 см из-под реберной дуги
Снижение цитотоксичности НК?клеток (или )
Гемофагоцитоз (в костном мозге, ликворе, лимфатических узлах, ином субстрате)
Клинический диагноз ГЛГ устанавливается при выполнении 5 из 8 критериев и отсутствии морфологических признаков злокачественной опухоли в исследуемом субстрате. Диагностические критерии могут выявляться асинхронно.
Второй этап – дифференциальный диагноз между первичными и вторичными формами ГЛГ. Диагноз ПГЛГ устанавливается при 1) выявлении биаллельной мутации в одном из известных генов ГЛГ; 2) при семейном анамнезе, подтверждающем наследственный характер заболевания; 3) при сохранении дефекта клеточной цитотоксичности НК клеток после остановки терапии в ремиссии заболевания. Диагноз ВГЛГ устанавливают при отсутствии признаков ПГЛГ и подтверждают установлением основного диагноза в соответствии с принципами диагностики соответствующей нозологии.
3. Лечение
3.1 Консервативное лечение
Цель консервативного лечения – подавление системного воспалительного ответа, восстановление функции органов и (при ПГЛГ) подготовка и выполнение трансплантации гемопоэтических стволовых клеток. ТГСК – единственный куративный метод лечения при ПГЛГ. Терапия ГЛГ осуществляется в соответствии со следующими принципами: 1) при установлении клинического диагноза ГЛГ назначается программная иммуносупрессивная химиотерапия (состав приведен ниже); 2) при верификации первичной формы ГЛГ пациенту показано выполнение трансплантации гемопоэтических стволовых клеток от аллогенного донора; 3) на всех этапах назначается многокомпонентная сопроводительная терапия, направленная на профилактику и лечение оппортунистических инфекций, замещение функции костного мозга (компонентная гемотерапия) и контроль осложнений иммуносупрессивной химиотерапии. Порядок назначения препаратов в программе иммуносупрессивной химиотерапии:
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано:
Фазу инициальной терапии рекомендовано проводить по схеме:
3.1.1 Этопозид в дозе 150 мг/м2 внутривенно капельно в дни 1,4,8,12,15,22,29,36,43,50,57
3.1.2 Дексаметазон в дозе 10 мг/м2 внутрь или внутривенно в дни 1-14, в дозе 5 мг/м2 в дни 15-28, в дозе 2,5 мг/м2 в дни 29-42, в дозе 1,25 мг/м2 в дни 43-56.
3.1.3 Циклоспорин А в стартовой дозе 5 мг/кг внутрь с дня 14 постоянно, целевая концентрация То-100-150 нг/мл.
3.1.4 Метотрексат (интратекально) в возрастной дозе (см. комментарий); вводится в дни 15,22,29,36 только при сохранении плеоцитоза или прогрессии неврологической симптоматики после двух недель системной терапии.
3.1.5 Преднизолон (интратекально) в возрастной дозе (см. комментарий); вводится в дни 15,22,29,36 только при сохранении плеоцитоза или прогрессии неврологической симптоматики после двух недель системной терапии.
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
фазу поддерживающей терапии рекомендовано проводить по схеме:
3.1.6 Этопозид в дозе 150 мг/м2 внутривенно капельно 1 раз в две недели в альтернирующем режиме с дексаметазоном
3.1.7 Дексаметазон в дозе 10 мг/м2 внутрь или внутривенно в течение трех дней с интервалом в две недели в альтернирующем режиме с этопозидом
3.1.8 Циклоспорин А в стартовой дозе 5 мг/кг внутрь с дня 14 постоянно, целевая концентрация То-100-150 нг/мл.
терапия второй линии
3.1.9 Антитимоцитарный глобулин (кроличий) в курсовой дозе 25 мг/кг
3.1.10 Метилпреднизолон в дозе 5 мг/кг/сутки в течение 5 дней
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарий: Возрастная доза метотрексата для интратекального введения: 3 лет – 12 мг; Возрастная доза преднизолона для интратекального введения: 3 лет – 10 мг. При ПГЛГ поддерживающая терапия продолжается до выполнения ТГСК.
3.3 Хирургическое лечение
Хирургическое пособие не применяется в терапии ГЛГ
3.4 Иное лечение
Сопроводительная антимикробная и трансфузионная терапия проводятся в соответствии с действующими клиническими рекомендациями
4. Реабилитация
Реабилитация и диспансерное наблюдение пациентов с ПГЛГ осуществляются в соответствии с принципами, принятыми для реципиентов аллогенной трансплантации гемопоэтических стволовых клеток.
5. Профилактика и диспансерное наблюдение
Пациентам с гемофагоцитарным лимфогистиоцитозом рекомендовано:
5.1 Пренатальная диагностика и репродуктивное планирование, включая прерывание беременности по медицинским показаниям, на основании установления диагноза у плода
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
5.2 Выполнение ТГСК у пациентов с верифицированным генетическим диагнозом ПГЛГ до клинической манифестации заболевания
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
6. Дополнительная информация, влияющая на течение и исход заболевания
6.1 Выбор донора для выполнения ТГСК от аллогенного донора (в порядке приоритета)
полностью совместимый сиблинг (включая пуповинную кровь)
полностью совместимый неродственный донор
частично совместимый (гаплоидентичный) родственный донор
неродственная пуповинная кровь
6.2 Срок выполнения ТГСК
ТГСК при ПГЛГ должна быть выполнена в наиболее ранний срок, до 6 месяцев от манифестации заболевания
поиск неродственного донора должен быть инициирован в момент верификации генетической природы ПГЛГ
При выполнении трансплантации от совместимого сиблинга необходимо исключить ПГЛГ у донора на основании генетического или, при неустановленном генетическом дефекте, функционального тестирования.
Критерии оценки качества медицинской помощи
Критерии качества
Уровень достоверности доказательств
Уровень убедительности рекомендаций
Выполнено определение концентрации ферритина, фибриногена, триглицеридов при подозрении на ГЛГ
Выполнена пункция костного мозга с подсчетом миелограммы при подозрении на ГЛГ
Выполнено молекулярно-генетическое исследование при установлении клинического диагноза ГЛГ
Проведена иммуносупрессивная химиотерапия (с началом терапии не позднее 24 часов от установления диагноза ГЛГ)
Направление документов пациента в центр трансплантации костного мозга в течение 7 дней от верификации первичной формы ГЛГ
Список литературы
Приложение А1. Состав рабочей группы
Конфликт интересов отсутствует
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
Педиатрия 31.08.19
Таблица П1 – Уровни достоверности доказательств
Уровень достоверности
Источник доказательств
Проспективные рандомизированные контролируемые исследования
Достаточное количество исследований с достаточной мощностью, с участием большого количества пациентов и получением большого количества данных
Как минимум одно хорошо организованное рандомизированное контролируемое исследование
Репрезентативная выборка пациентов
II (2)
Проспективные с рандомизацией или без исследования с ограниченным количеством данных
Несколько исследований с небольшим количеством пациентов
Хорошо организованное проспективное исследование когорты
Мета-анализы ограничены, но проведены на хорошем уровне
Результаты не презентативны в отношении целевой популяции
Хорошо организованные исследования «случай-контроль»
III (3)
Нерандомизированные контролируемые исследования
Исследования с недостаточным контролем
Рандомизированные клинические исследования с как минимум 1 значительной или как минимум 3 незначительными методологическими ошибками
Ретроспективные или наблюдательные исследования
Серия клинических наблюдений
Противоречивые данные, не позволяющие сформировать окончательную рекомендацию
IV (4)
Мнение эксперта/данные из отчета экспертной комиссии, экспериментально подтвержденные и теоретически обоснованные
Таблица П2 – Уровни убедительности рекомендаций
Уровень убедительности
Описание
Расшифровка
Рекомендация основана на высоком уровне доказательности (как минимум 1 убедительная публикация I уровня доказательности, показывающая значительное превосходство пользы над риском)
Метод/терапия первой линии; либо в сочетании со стандартной методикой/терапией
Рекомендация основана на среднем уровне доказательности (как минимум 1 убедительная публикация II уровня доказательности, показывающая значительное превосходство пользы над риском)
Метод/терапия второй линии; либо при отказе, противопоказании, или неэффективности стандартной методики/терапии. Рекомендуется мониторирование побочных явлений
Рекомендация основана на слабом уровне доказательности (но как минимум 1 убедительная публикация III уровня доказательности, показывающая значительное превосходство пользы над риском) или
нет убедительных данных ни о пользе, ни о риске)
Нет возражений против данного метода/терапии или нет возражений против продолжения данного метода/терапии
Рекомендовано при отказе, противопоказании, или неэффективности стандартной методики/терапии, при условии отсутствия побочных эффектов
Отсутствие убедительных публикаций I, II или III уровня доказательности, показывающих значительное превосходство пользы над риском, либо убедительные публикации I, II или III уровня доказательности, показывающие значительное превосходство риска над пользой
Порядок обновления клинических рекомендаций – пересмотр 1 раз в год.
Приложение Б. Алгоритмы ведения пациента
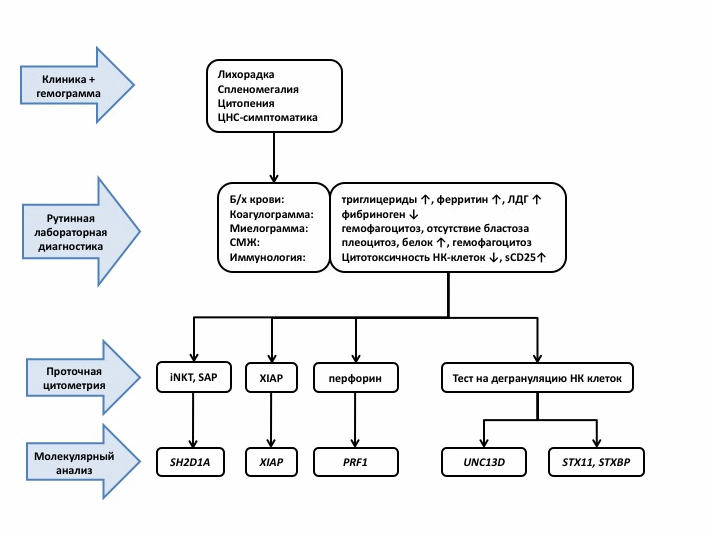
Алгоритм клинической и лабораторной диагностики гемофагоцитарного лимфогистиоцитоза
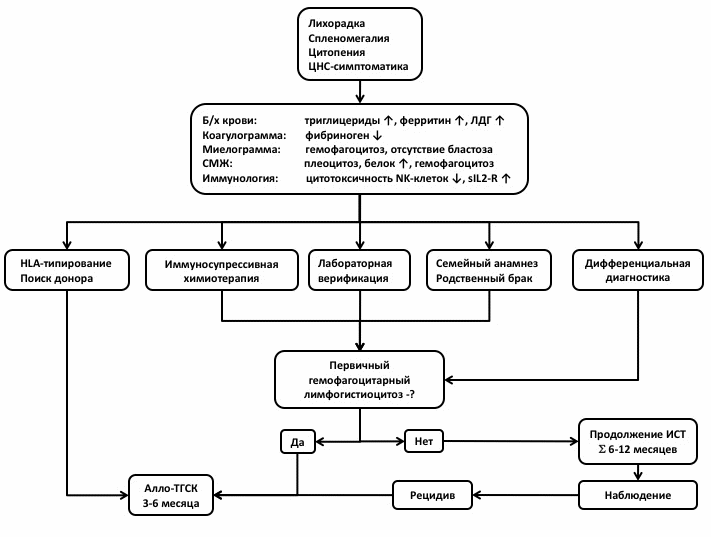
Алгоритм ведения пациентов с гемофагоцитарным лимфогистиоцитозом
Приложение В. Информация для пациентов
Гемофагоцитарный лимфогистиоцитоз – редкое заболевание, причиной которого является нарушение в работе иммунной системы. В результате этого нарушения происходит избыточная активация и размножение некоторых видов лейкоцитов, которые в результате вызывают тяжелое повреждение органов. Наиболее часто нарушается работа костного мозга, печени, селезенки и головного мозга.
Основными проявлениями заболевания являются высокая температура, увеличение размеров печени и селезенки, изменения в анализах крови в виде снижения основных показателей – гемоглобина, лейкоцитов, тромбоцитов и свертываемости, а также нарушения сознания и поведения, обусловленные повреждением головного мозга.
Причиной заболевания может быть наследственный (генетический) дефект в работе иммунной системы, в этом случае говорят о первичном гемофагоцитарном лимфогистиоцитозе, или сбой, обусловленный другим тяжелым заболеванием, в этом случае говорят о вторичном гемофагоцитарном лимфогистиоцитозе. Наиболее часто вторичный гемофагоцитарный лимфогистиоцитоз встречается при ревматических заболеваниях, опухолях и инфекциях, вызванных вирусами семейства герпес-вирусов.
Для установления диагноза необходимо выполнение большого количества исследований крови, а также пункции костного мозга и спинномозговой жидкости. При подозрении на гемофагоцитарный лимфогистиоцитоз обследование должно быть проведено быстро, в течении нескольких дней. Для подтверждения диагноза наследственной формы гемофагоцитарного лимфогистиоцитоза необходимо выполнение молекулярно-генетического исследования.
Гемофагоцитарный лимфогистиоцитоз – тяжелое заболевание, которое, при отсутствии лечения, приводит к смерти пациента.
Лечение гемофагоцитарного лимфогистиоцитоза состоит из двух этапов. На первом этапе назначают химиотерапию, подавляющую функцию иммунной системы. Эта терапия состоит из трех основных препаратов: этопозид, дексаметазон и циклоспорин А. Некоторым пациентам для контроля поражения головного мозга необходимо введение химиопрепаратов в спинномозговой канал. Целью иммуносупрессивной терапии является установление контроля над активацией иммунной системы и нормализация работы пораженных органов. Интенсивная фаза лечения длится два месяци и, как правило, требует пребывания в стационаре. Для лечения необходимо установить центральный венозный катетер, через который вводят лекарства и делают забор крови на исследование.
Для пациентов с первичным гемофагоцитарным лимфогистиоцитозом вторым этапом лечения является трансплантация гемопоэтических стволовых клеток. Трансплантация является необходимым этапом терапии, без которого излечение пациента с гемофагоцитарным лимфогистиоцитозом невозможно. Трансплантация гемопоэтических стволовых клеток (костного мозга) – сложная медицинская процедура, состоящая из нескольких этапов. Трансплантацию проводят в специализированном отделении. Очено важно выполнить трансплантацию вовремя, через 2-6 месяцев от начала иммуносупрессивной терапии. Для того, чтобы выполнение трансплантации стало возможным, вскоре после установления диагноза необходимо начать поиск донора. Донором может быть полностью или частично совместимый родственник (брат, сестра, мать, отец) или полностью совместимый неродственный донор. Выбор донора зависит от множества дополнительных показателей и осуществляется в центре трансплантации.